Giuseppina Rinaudo - Didattica della Fisica Corso SIS Indirizzo fisico-matematico - a.a. 2006/07
|
|
|
- Giacinto Grande
- 7 anni fa
- Visualizzazioni
Transcript
1 Giuseppina Rinaudo - Didattica della Fisica Corso SIS Indirizzo fisico-matematico - a.a. 006/07 rinaudo@ph.unito.it; Fisica nucleare 10.1 Come partire da problemi di attualità: il polonio e il caso Litvinenko, l Iran e gli impianti per la produzione di energia nucleare, l uranio impoverito Valenze didattiche: si tratta di tipici problemi di Fisica-scienza e società, dai quali si può partire per affrontare argomenti di fisica nucleare, ma anche di relatività, fisica quantistica, probabilità e statistica. L idea alla base è di arrivare a essere in grado di valutare gli aspetti tecnici del problema, raccogliere documentazione affidabile, capire il significato di rischio associato a certi fenomeni o attività. Un questionario per riflettere: 1) Che cosa avete capito sul problema del Po 10 : spiegate in poche righe perché è letale. Quali sono state le fonti principali di informazione (media, internet, testi universitari, ecc.) che avete usato per documentarvi? Come avete valutato l affidabilità delle fonti? ) Che cosa avete capito sul problema del divieto dato all Iran di procedere nel dotarsi di impianti nucleari: spiegate in poche righe qual è il rischio potenziale. Quali sono state le fonti principali di informazione (media, internet, testi universitari, ecc.) che avete usato per documentarvi? Come avete valutato l affidabilità delle fonti? 3) Che cosa avete capito sul problema dell uso di uranio impoverito nelle testate di missili convenzionali: spiegate in poche righe come è stato usato e qual è il rischio potenziale. Quali sono state le fonti principali di informazione (media, internet, testi universitari, ecc.) che avete utilizzato per documentarvi? Come avete valutato l affidabilità delle fonti? Risposte: 1) Il Po 84 è l ultimo anello in una catena di prodotti di decadimenti radioattivi. Decade alfa in Pb 8, che è stabile e non ha decadimenti radiativi di tipo gamma, che possono essere rivelati anche a distanza. Poiché la radiazione alfa del polonio lascia una traccia di pochi micron nella materia, il Po in pratica non lascia tracce rivelabili con strumenti ordinari di misura di radioattività, ma si può solo determinare il residuo di Pb. ) Perché reattori e armi nucleari sono legati? Nel funzionamento di reattori nucleari convenzionali, basati cioè su U 35, si producono molti isotopi altamente radioattivi, come il Pu 39, che non possono sostenere una reazione a catena controllata, come quella che avviene nel reattore all U 35, ma possono innescare facilmente una reazione incontrollata come quella che serve in una esplosione nucleare. Inoltre l impianto di arricchimento dell U 35, che porta la frazione di U 35 dallo 0,7% presente nell uranio naturale al -3% necessario per far funzionare un reattore nucleare convenzionale, implica lo sviluppo di tecnologie e know-how che possono essere impiegate per lo sviluppo di armi nucleari. 3) L'uranio impoverito è costituito prevalentemente da U 38 che è radioattivo. Nella fabbricazione del proiettile, l'u 38 viene inserito in una certa frazione nella lega usata nella punta del proiettile per indurirla, dato che l uranio è molto pesante e aumenta la forza d urto e di penetrazione del proiettile. A livello della testata del proiettile la radioattività rilevata è trascurabile (rientra nei livelli normali). Quando il proiettile si disintegra, l'u 38 forma un ossido volatile che può essere 1
2 inspirato con l'aria: questo ossido, depositandosi sulle pareti dei polmoni e di altre parti delle vie respiratorie può dare rischi da radioattività che, secondo alcune indagini, sono significativi. 10. Nuclei concettuali importanti di fisica nucleare a) Forze nucleari: scoperta della radioattività da parte di Becquerel (1896) b) Instabilità nucleare: scoperta delle catene di decadimento radioattivo (Becquerel, Curie, ecc.) c) Energia nucleare: massa ed energia, relatività di Einstein (1905) d) Isotopi, energia di legame nel nucleo e sua dipendenza dal numero di massa e) Decadimenti radioattivi dei nuclei, in particolare dell'u 38 f) Legge esponenziale del decadimento radioattivo g) Conteggi di eventi stocastici e statistica di Poisson h) Effetti delle radiazioni: unità dosimetriche, rischi da radiazione i) Reazione a catena, funzionamento del reattore nucleare e delle armi nucleari j) Prospettive e sviluppi possibili dell uso pacifico dell energia nucleare Per una discussione più dettagliata, esaminare il sito web Energia nucleare e relatività Equivalenza massa-energia. In relatività la relazione fra quantità di moto p e velocità v è la seguente:?x?x p = m = γ m = γ m v (1)? τ?t dove τ è il tempo proprio e t è il tempo nel sistema di riferimento in cui viene misurato lo spazio percorso x e quindi la velocità v. Confrontando questa relazione con la relazione della meccanica classica, p=mv, si vede che tutto succede come se la massa inerziale m fosse moltiplicata per il c fattore di dilatazione relativistica γ, γ =. Il significato del prodotto γ m, cioè c v dell inerzia relativistica, si capisce esaminando la quantità E = γ m c, che, dimensionalmente, ma anche effettivamente, è una energia. Se il corpo ha una velocità molto minore di c, possiamo usare lo sviluppo di γ in serie di Taylor, valido per piccole velocità: 1 v 1 E = γ m c = mc = mc 1 + = mc + mv c v 1 c 1 Nell espressione E = mc + mv riconosciamo chiaramente il secondo termine, che è l energia cinetica, mentre il primo termine rappresenta l energia di massa, cioè quella energia che rimane anche quando il corpo è fermo, cioè la sua energia cinetica è nulla: energia di massa 1 E + mv = mc () energia cinetica Essendoci quindi energia associata alla massa, essa si può trasformare in altre forme di energia, ad esempio in energia cinetica, il che è appunto ciò che avviene in modo vistoso in una reazione
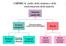
3 nucleare. Se volessimo dare una rappresentazione pittorica della storica reazione di decadimento α dell uranio 38, scoperta da Bequerel nel 1897, potremmo immaginarla come nella figura seguente: 9U Th 34 + e 4 prima.. dopo p e e 4 9U 38 90Th 34 p Th Dall uranio 38, che è fermo, si stacca un gruppetto di quattro nucleoni, cioè la particella α, mentre il resto del nucleo, che, avendo perso due protoni e due neutroni, è diventato torio 34, rincula in senso opposto. Scriviamo la legge di conservazione della quantità di moto p: p U = p Th + p α Poiché l uranio era inizialmente fermo, p U =0, quindi p Th = - p α, cioè il torio e l alfa rinculano uno contro l altro, in direzione opposta, con quantità di moto uguale e contraria: tutto avviene come in una bomba che scoppia da ferma, i cui i frammenti schizzano in direzioni varie e la somma vettoriale delle quantità di moto è nulla. Il fatto che l alfa e il torio siano prodotti nella reazione con una quantità di moto non nulla, implica anche che essi hanno un energia cinetica non nulla: da dove proviene, visto che l uranio era fermo e quindi la sua energia cinetica era nulla? ccorre tenere conto dell energia di massa, cioè riferire la legge di conservazione dell energia alle energie totali relativistiche, che, a piccole velocità, si possono scrivere, secondo l'eq., come somma dell energia di massa e di quella cinetica: 1 1 m c = m c + m v + m c m v (3) U Th Th Th α + Si vede subito che, essendo le energie cinetiche del torio e dell alfa quantità positive, la massa dell uranio deve essere maggiore della somma delle masse del torio e dell alfa: quindi la massa non si conserva nelle reazioni nucleari 1, anzi nella reazione avviene una trasformazione di energia di massa dell uranio in energia cinetica del torio e dell alfa. α α 1 In realtà la massa non si conserva rigorosamente neppure nelle reazioni chimiche: ad esempio, in una reazione chimica esotermica come la combustione del metano in presenza di ossigeno, il calore che si sviluppa nella reazione non è altro che energia cinetica disordinata delle molecole prodotte che, a sua volta deriva dalla trasformazione di una piccolissima parte dell energia di massa delle molecole iniziali. Tuttavia, nelle reazioni chimiche, la parte di energia di massa che si trasforma è meno di una parte in un miliardo e quindi non può essere rivelata neppure con la più sofisticata delle bilance analitiche: aveva pertanto pienamente ragione Lavoisier quando enunciò la sua legge della 3
4 Non è tuttavia così facile trasformare energia di massa in altre forme di energia, perché la frazione di energia che si trasforma, in una singola reazione, è sempre molto piccola, come si intuisce anche solo guardando l equazione scritta sopra, dato che la maggior parte dell energia di massa dell'uranio rimane ancora, dopo il decadimento, sotto forma di energia di massa del torio e dell alfa. Ciò è dovuto alla legge di conservazione del numero di "nucleoni" (protoni o neutroni): poiché i nucleoni debbono restare tutti e nessuno può scomparire, anche la massa dei nuclei prodotti nella reazione non potrà scendere al di sotto di un valore minimo, ed è questo fatto che garantisce la stabilità sostanziale della materia, cioè il fatto che non corriamo nessun rischio di vedere tutta la materia trasformarsi in energia cinetica e quindi scomparire! Anziché pensare in termini di energia di massa possiamo pensare in termini di energia nucleare, così come, per spiegare una reazione chimica, abbiamo ragionato in termini di energia chimica. La trasformazione di energia può quindi essere rappresentata con lo schema seguente, in cui appare evidente che si tratta di una trasformazione di energia nucleare in energia cinetica. E energia alla quale i nucleoni non sono legati nel nucleo B U 9 e + Th 90 0 energia cinetica energia nucleare Esaminiamo da vicino che cosa è l energia di massa di un nucleo. gni nucleo ha una sua propria massa caratteristica, che viene misurata con apparati di misura particolari, detti spettrometri di massa : i primi spettrometri di massa furono sviluppati intorno 190 proprio per misurare le masse dei nuclei. Ad esempio un nucleo come l isotopo 1 del carbonio, 6 C 1, che è particolarmente interessante perché è preso come riferimento per esprimere le masse dei nuclei. Il carbonio 1, 6 C 1, è formato da sei protoni e sei neutroni, verrebbe perciò spontaneo pensare che la sua massa debba essere pari alla somma della massa dei sei protoni e dei sei neutroni, invece è minore: la differenza si chiama difetto di massa. Il difetto di massa è piccolo, rispetto alla massa totale, ma non è trascurabile: nel riquadro che segue trovate il calcolo dettagliato, che per il 6 C 1 è particolarmente semplice. La sua massa infatti è stata presa come riferimento per la definizione dell unità di massa atomica: essa è, per definizione, esattamente 1 u.m.a., mentre le masse degli altri nuclei sono invece, in generale, multipli non interi dell u.m.a., proprio perché ogni nucleo ha un suo caratteristico difetto di massa. Il difetto di massa viene generalmente riferito al singolo nucleone, cioè a una particella fittizia, la cui massa ha un valore medio fra la massa del protone e quella del neutrone, quindi, per un nucleo di numero di massa A, viene espresso come A D m, dove D m è il difetto di massa per nucleone: ciò renderà possibile apprezzare meglio le differenze effettive fra i diversi nuclei, che sono dovute non solo al fatto che varia A ma anche al fatto che varia D m. conservazione della massa nelle reazioni chimiche, perché la legge, anche se non è esatta, è comunque valida con altissima precisione. Nelle reazioni nucleari, l effetto è invece del tutto evidente. 4
5 neutrone m n = 1, kg protone m p = 1, kg nucleone m N = 1, kg massa attesa per 1 nucleoni = 1 1, kg massa del 6 C 1 = 1 1, kg difetto di massa medio per ogni nucleone del 6 C 1 D m = 0, kg difetto di massa totale del 6 C 1 1 D m = 0, kg Ci si può chiedere come può un nucleone avere, dentro il nucleo, una massa minore della sua massa reale. Per capirlo occorre ricorrere alla teoria della relatività e ragionare non più in termini di massa, ma di energia di massa. Se il nucleone fosse libero, cioè fuori del nucleo, la minima energia che dovrebbe avere sarebbe proprio quella dovuta alla sua massa: questo se fosse fermo, perché, se fosse in moto, avrebbe in più dell energia cinetica. Dentro il nucleo ha invece una energia minore dell energia di massa, cioè gli manca dell energia per diventare libero: questa energia mancante è quindi l energia di legame, E B, cioè l energia che occorrerebbe dargli per estrarlo dal nucleo. Per calcolarla, basta moltiplicare il difetto di massa, D m, per la velocità della luce c al quadrato, secondo la relazione di Einstein: E B = D m c (4) È inoltre conveniente esprimere l energia di legame non nelle unità di misura del SI, ma nelle unità usate nella fisica nucleare, cioè i MeV (megaelettronvolt): 1 ev è l energia che acquista un elettrone, che ha una carica elettrica pari a 1, coulomb quando è accelerato da una differenza di potenziale elettrico di 1 V, quindi il fattore di conversione da J a MeV vale: 1 J = (1/ 1, ) ev = 0, ev = 0, MeV (10) 5
6 Il calcolo dell energia di legame del 6 C 1 è riassunto nel riquadro: come si vede ogni nucleone ha una energia di legame di circa 8 MeV, per cui l energia totale che tiene insieme il 6 C 1 è pari a 1 volte questa energia, cioè 96 MeV, dato che ogni nucleone contribuisce per 8 MeV. energia di legame media per nucleone del 6 C 1 E B = D m c E B = 0, J = (0, , ) MeV 8 MeV energia di legame totale del 6 C 1 1 E B 96 MeV L energia di legame totale del 6C 1 è l energia che occorrerebbe spendere per disfare completamente il 6 C 1, cioè per separare i 1 nucleoni e lasciarli tutti completamente liberi di andare per la loro strada. Per calcolare l energia che si sviluppa in una reazione nucleare, dobbiamo conoscere quanto vale E B nei vari nuclei, perché, in una reazione nucleare non succede mai che un nucleo si disfi completamente e tutti i nucleoni se ne vadano via liberi, ma i nucleoni semplicemente si riaggregano in modo diverso a formare nuovi nuclei e quel che conta è l energia di legame E B che si trovano ad avere nel nuovo nucleo. Infatti E B non ha sempre lo stesso valore, ma varia da nucleo a nucleo. I motivi sono diversi e alquanto complessi. Per i nuclei piccoli, E B cresce al crescere del numero di massa. La forza nucleare agisce infatti come una forte colla che tende a fare restare attaccati insieme i nucleoni: se immaginiamo delle palline coperte di colla, si può intuire che è più facile liberare una pallina se è incollata solo a un altra pallina anziché se è incollata a sei altre palline! Nella figura è mostrato, come esempio, una rappresentazione pittorica di quello che potrebbe essere un nucleo di deuterio, che è un isotopo dell idrogeno, con due soli nucleoni, un protone e un neutrone, mentre a fianco c è un nucleo di 3 Li 7, che ha 3 protoni e 4 neutroni: ci sono chiaramente molti più legami nel caso del 3 Li 7, semplicemente perché ci sono più nucleoni e ognuno di essi stabilisce legami con gli altri. 1 3Li 7 L effetto colla, tuttavia, non può continuare a crescere all infinito, perché, a un certo punto, ci sono troppi protoni nella zona ristretta del volume del nucleo ed essi si respingono tra di loro a causa della carica elettrica, che è di segno positivo per tutti. L energia di legame raggiunge perciò un valore massimo, pari a circa 9 MeV, per nuclei che hanno A prossimo a 60, come il ferro o il nichel, e poi diminuisce gradualmente. Per l uranio 38 E B vale circa 7,5 MeV, come si può apprezzare dalla figura. 6
7 Possiamo ora fare il calcolo dell energia che si libera nel decadimento α dell uranio 38. Dal grafico della figura si vede infatti che, rispetto all uranio, l energia di legame è leggermente maggiore per il torio (circa 0,018 MeV per nucleone), mentre è più piccola per l alfa (circa 0,5 MeV per nucleone). Nel decadimento, quindi, i 34 nucleoni del torio contribuiscono positivamente per circa 34*0,018 MeV, mentre i 4 nucleoni dell elio contribuiscono negativamente per 4*0,5 MeV: in totale l energia E che si libera vale: E = 34 * 0,018 4*0,5 MeV MeV Questa energia viene ripartita sotto forma di energia cinetica fra il torio e l elio, ma è l elio a fare la parte del leone, dato che ha massa molto minore. Valori di alcuni MeV sono tipici dell energia di particelle α emesse nei decadimenti radioattivi: l energia è sufficientemente elevata perché la particella possa percorrere un tratto abbastanza lungo da poter essere rivelata prima di perdere tutta la sua energia negli urti con le molecole del materiale che incontra, come si può vedere dall esempio della figura. Nella figura sono mostrate tracce lasciate da particelle α emesse da una sorgente radioattiva in una camera a nebbia : la camera è piena di vapori sovrasaturi, al passaggio delle particelle α, si creano dei nuclei di condensazione lungo i percorsi delle particelle che permettono di visualizzarli. La sorgente è posta in basso rispetto alla camera. 7
8 10.4 Radiazioni ionizzanti e il rischio nucleare Il rischio nucleare è appunto legato all alta energia che si libera nella singola interazione, che può recare danno alle cellule se supera una soglia di tolleranza (vedi tabella sui rischi della vita quotidiana ). Confrontiamo ad esempio l energia che si libera in una tipica reazione chimica fortemente esotermica come la combustione del metano. Il metano è formato da un atomo di carbonio e 4 atomi di idrogeno (formula chimica C4); in presenza di ossigeno (), si forma anidride carbonica (C) e acqua (). C4 + C + C + C + Anche in una reazione di questo tipo c è una trasformazione di energia di legame (in questo caso il legame è chimico) in energia cinetica delle molecole: le molecole di metano e di ossigeno hanno piccola energia di legame e piccola energia cinetica, quelle di anidride carbonica e acqua prodotte nella reazione hanno alta energia cinetica (termica) e sono molto legate. Tenendo conto che l energia di legame è negativa, ciò è in accordo con la legge di conservazione dell energia. L energia che si sviluppa in una reazione di questo tipo è di qualche ev. Queste energie sono circa un milione di volte minore dell energia che si sviluppa in una reazione nucleare, che, come visto sopra, è tipicamente dell ordine del MeV (mega elettronvolt). Con energie così elevate è facile rilevare la singola interazione radiazione-materia, ad esempio con un semplice contatore geiger, oppure rivelare la traccia della singola particella, come avvenne appunto nello storico esperimento di Becquerel Meccanica quantistica Un decadimento come quello dell'u 38 Th 34 +e 4 non può essere descritto classicamente; quantisticamente viene descritto come possibilità dell'e 4 e del Th 34 di essere presenti in una "sovrapposizione di stati": cioè sia come stati all'interno della buca di potenziale nucleare dell'u 38, sia come "stati liberi" all'esterno del nucleo. Inizialmente, l'e 4 e il Th 34 hanno una probabilità molto più alta di trovarsi nello stato in cui sono all'interno del nucleo, legati fra di loro dalla forza di attrazione nucleare, ma hanno anche una probabilità non nulla di trovarsi nello stato in cui sono fuori del nucleo: se i nuclei si trovano in tale stato, essendo abbastanza lontani, la repulsione coulombiana prevale sull attrazione nucleare e i nuclei si allontanano conservando energia e quantità di moto 3. La probabilità di decadimento per unità di tempo è appunto la probabilità di "passaggio" dallo stato in cui l'e 4 e il Th 34 sono all interno del nucleo allo stato in cui sono fuori, passaggio che avviene stocasticamente nel tempo. Non è infatti possibile prevedere in quale istante l U 38 Dello stesso ordine di grandezza è l energia emessa in una transizione atomica che produce luce visibile, come si calcola facilmente dalla relazione di Planck, E = hf = hc/λ, con, ad esempio, λ 600 nm. Ne segue che parte dell energia chimica non si trasforma in energia cinetica dell intera molecola, ma in energia di eccitazione degli elettroni atomici, che, diseccitandosi, emettono luce: la fiamma infatti appare luminosa e colorata. 3 In principio c è la stessa probabilità che avvenga la reazione opposta se i due nuclei vengono a trovarsi a una distanza ravvicinata e con quantità di moto ed energie cinetiche tali da poter ricostruire l energia di massa dell Uranio. In meccanica quantistica vale la piena reversibilità temporale. 8
9 deciderà di decadere (indeterminismo non epistemico), però si può calcolare (e misurare) la probabilità che decada in un certo intervallo di tempo e questa probabilità è uguale per tutti i nuclei di U Sorgenti di radiazione e unità di misura dosimetriche Sorgenti naturali di radiazione: - raggi cosmici - radionuclidi presenti nell ambiente (uranio, radon) - radionuclidi presenti nel corpo (40K, 14C) Unità dosimetriche Sono state introdotte per valutare gli effetti sul un corpo dell assorbimento di energia dovuta alle radiazioni di origine nucleare ( ionizzanti ). Unità di misura: - attività bequerel (Bq): numero di particelle ionizzanti che colpisce il corpo; l unità storica, peraltro ancora usata, è il curie (Ci), che è pari a 3, Bq - dose assorbita gray (Gy): energia depositata per kg di peso; 1Gy = 1J/kg - dose equivalente sievert (Sv): dose assorbita per il fattore di qualità della radiazione (alto per neutroni e nuclei pesanti, =1 per elettroni e gamma); - esposizione roengten (R): è una unità di misura storica, peraltro ancora usata, ed è la carica elettrica, di ambo i segni, che si sviluppa nello sciame prodotto al passaggio in aria della particella ionizzante (1R=, C/kg). Tipicamente - la radiazione cosmica è circa 0,3 msv/anno al livello del mare (circa il doppio a 1000 m) - i radionuclidi presenti nel corpo umano producono una dose di circa 0,3 msv/anno - la radioattività ambientale varia molto da zona a zona Radioattività ambientale in alcune città italiane Ancona 0.85 Napoli.13 Aosta 0.49 Palermo 0.90 Bari 0.83 Perugia 0.86 Bologna 0.80 Potenza 1.31 Cagliari 0.86 Reggio Cal. 1.8 Campobasso 0.69 Roma 1.58 Firenze 0.77 Torino 0.86 Genova 0.75 Trento 0.84 L Aquila 0.8 Trieste 0.76 Milano 0.8 Venezia 0.77 Limite raccomandato di esposizione: 15 msv/anno Dose letale :,5-3 Sv Per tipici contatori geiger usati per la didattica si può stimare: - una massa di circa 1 g nella zona sensibile - energia media depositata dalla singola particella circa J (0,5 MeV) - fattore di qualità circa 1 (i nuclei pesanti vengono bloccati dalla finestra di protezione del tubo geiger) Per passare da Bq (conteggio medio al secondo) a msv/anno: 1 Bq 107 conteggi/anno (1 anno= 365 giorni * 4 h/giorno * 3600 s/h) 1 conteggio nel contatore J/10-3 g = Sv 9
10 10 7 conteggi/anno 10-3 Sv/anno = 1 msv/anno 10.7 The risks of daily life Activities carrying an average risk of death of one part per million Activity Ionizing radiation ne chest X ray at a good hospital Traveling cross-country once by jet Living 1 week in a building Living 5 weeks outdoors Living months in Denver Living 5 years next to nuclear power plant Living 50 yrs within 5 mi of nuclear power plant Internal consumption Smoking 1.4 cigarettes Living months with a cigarette smoker Drinking 0.5 liters of wine Normal consumption of tap water for 1 year Drinking 30 1-ounce cans of diet soda Eating 40 tablespoons of peanut butter Eating l00 charcoal broiled steaks Travel 3 miles by motorcycle 10 miles by bicycle 30 miles by car 800 miles by train 1000 miles by commerciai airplane 6000 miles (cross-country) by jet Work Spending 1 hour in a coal mine Spending 3 hours in a coal mine ther Living days in New York or Boston Cause(s) of death Cancer from ionizing radiation Cancer from cosmic ionizing radiation Cancer from indoor radon Cancer from outdoor radon Cancer from cosmic ionizing radiation Cancer from ionizing radiation Cancer and heart disease Cancer and heart disease Cirrhosis of the liver Cancer from chloroform Cancer from saccharin Liver cancer from aflatoxin B Cancer from benzopyrene Cancer from cosmic ionizing radiation Black lung disease Air pollution SURCE: Richard Wilson, "Comparing Risks..' Physics and Society. ctober pp Energia nucleare: uso, problemi, sviluppo Si rimanda al seminario Energia nucleare oggi, scaricabile dal sito Esercizi 1. Calcoli su un fenomeno di fisica nucleare (obbligatorio): realizzate un calcolo realistico e significativo su un fenomeno di fisica nucleare.. Per un tipico problema di fisica nucleare preparate una scheda didattica ad uso dell'allievo indicando - contesto, prerequisiti, - inserimento a grandi linee nel curriculum, con indicazioni della scaletta dei tempi, - scelta degli argomenti specifici da trattare e loro sviluppo, - modalità di conduzione. 10
10. Fisica nucleare e il problema dell'uranio impoverito
 Giuseppina Rinaudo - Didattica della Fisica Corso SIS Indirizzo fisico-matematico - a.a. 005/06 rinaudo@ph.unito.it; http://www.iapht.unito.it/fsis 10. Fisica nucleare e il problema dell'uranio impoverito
Giuseppina Rinaudo - Didattica della Fisica Corso SIS Indirizzo fisico-matematico - a.a. 005/06 rinaudo@ph.unito.it; http://www.iapht.unito.it/fsis 10. Fisica nucleare e il problema dell'uranio impoverito
Le radiazioni e la loro misura
 Le radiazioni e la loro misura Le radiazioni e le radiazioni ionizzanti Nuclei, radioattività, reazioni nucleari Einstein, la legge E = mc 2 e l'energia nucleare Uso degli strumenti di misura Che cosa
Le radiazioni e la loro misura Le radiazioni e le radiazioni ionizzanti Nuclei, radioattività, reazioni nucleari Einstein, la legge E = mc 2 e l'energia nucleare Uso degli strumenti di misura Che cosa
Il nucleare non è il diavolo
 05 Anno Mondiale della Fisica Il nucleare non è il diavolo Progetto di monitoraggio della radioattività ambientale nelle scuole Sezione di Torino dell INFN e Dipartimenti di Fisica dell Università di Torino
05 Anno Mondiale della Fisica Il nucleare non è il diavolo Progetto di monitoraggio della radioattività ambientale nelle scuole Sezione di Torino dell INFN e Dipartimenti di Fisica dell Università di Torino
Decadimento a. E tipico dei radioisotopi con Z > 82 (Pb), nei quali il rapporto tra il numero dei neutroni e quello dei protoni è troppo basso.
 Decadimento a Nel decadimento vengono emesse particelle formate da 2 protoni e 2 neutroni ( = nuclei di 4He) aventi velocità molto elevate (5-7% della velocità della luce) E tipico dei radioisotopi con
Decadimento a Nel decadimento vengono emesse particelle formate da 2 protoni e 2 neutroni ( = nuclei di 4He) aventi velocità molto elevate (5-7% della velocità della luce) E tipico dei radioisotopi con
Il Nucleo. Dimensioni del nucleo dell'ordine di 10. m Il raggio nucleare R = R 0 -15
 Il Nucleo Nucleo e' costituito da nucleoni (protoni e neutroni). Mentre i neutroni liberi sono abbastanza instabili tendono a decadere in un protone ed un elettrone (t 1/2 circa 900 s), i protoni sono
Il Nucleo Nucleo e' costituito da nucleoni (protoni e neutroni). Mentre i neutroni liberi sono abbastanza instabili tendono a decadere in un protone ed un elettrone (t 1/2 circa 900 s), i protoni sono
Radioattività. 1. Massa dei nuclei. 2. Decadimenti nucleari. 3. Legge del decadimento XVI - 0. A. Contin - Fisica Generale Avanzata
 Radioattività 1. Massa dei nuclei 2. Decadimenti nucleari 3. Legge del decadimento XVI - 0 Nucleoni Protoni e neutroni sono chiamati, indifferentemente, nucleoni. Il numero di protoni (e quindi di elettroni
Radioattività 1. Massa dei nuclei 2. Decadimenti nucleari 3. Legge del decadimento XVI - 0 Nucleoni Protoni e neutroni sono chiamati, indifferentemente, nucleoni. Il numero di protoni (e quindi di elettroni
Energia nucleare oggi
 Ciclo di Conferenze del premio Antonicelli Liceo Scientifico Gramsci - Ivrea, 11 Novembre 2006 Energia nucleare oggi Giuseppina Rinaudo Dipartimento di Fisica Sperimentale - Università di Torino sito web:
Ciclo di Conferenze del premio Antonicelli Liceo Scientifico Gramsci - Ivrea, 11 Novembre 2006 Energia nucleare oggi Giuseppina Rinaudo Dipartimento di Fisica Sperimentale - Università di Torino sito web:
Distaccamento Volontari Caselle Torinese 5) RADIOATTIVITA. Testi, immagini ed argomenti trattati a cura del Comando Provinciale di Torino
 5) RADIOATTIVITA 5.1 Radioattività Parlando di radioattività bisogna partire dai concetti introduttivi di fisica nucleare. 5.1.1 L atomo L atomo può essere definito la più piccola parte di un elemento
5) RADIOATTIVITA 5.1 Radioattività Parlando di radioattività bisogna partire dai concetti introduttivi di fisica nucleare. 5.1.1 L atomo L atomo può essere definito la più piccola parte di un elemento
La Radioattività. da:ispra istituto superiore per la ricerca e protezione ambientale
 La Radioattività da:ispra istituto superiore per la ricerca e protezione ambientale Isotopi: Nuclei diversi del medesimo elemento chimico Vi sono elementi con atomi che, a parità di numero di protoni,
La Radioattività da:ispra istituto superiore per la ricerca e protezione ambientale Isotopi: Nuclei diversi del medesimo elemento chimico Vi sono elementi con atomi che, a parità di numero di protoni,
La radioattività. La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle e/ radiazioneni elettromagnetiche.
 La radioattività La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle e/ radiazioneni elettromagnetiche. La radioattività: isotopi. Il numero totale di protoni
La radioattività La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle e/ radiazioneni elettromagnetiche. La radioattività: isotopi. Il numero totale di protoni
ELEMENTI di CHIMICA NUCLEARE. La FISSIONE NUCLEARE
 ELEMENTI di CHIMICA NUCLEARE La FISSIONE NUCLEARE Lo scienziato Otto Hahn nel 938 scoprì che l'uranio 35 9U è fissile. La fissione è una rottura dei nuclei pesanti e può avvenire quando un neutrone lento
ELEMENTI di CHIMICA NUCLEARE La FISSIONE NUCLEARE Lo scienziato Otto Hahn nel 938 scoprì che l'uranio 35 9U è fissile. La fissione è una rottura dei nuclei pesanti e può avvenire quando un neutrone lento
Il numero di protoni presenti in un atomo si chiama numero atomico = Z elemento differisce per il numero Z. H deuterio (6000 volte abbondante)
 Il numero di protoni presenti in un atomo si chiama numero atomico = Z elemento differisce per il numero Z ogni ISOTOPI atomi di uno stesso elemento ma con un N di neutroni x es. 14 C e 12 C l H ha 3 isotopi:
Il numero di protoni presenti in un atomo si chiama numero atomico = Z elemento differisce per il numero Z ogni ISOTOPI atomi di uno stesso elemento ma con un N di neutroni x es. 14 C e 12 C l H ha 3 isotopi:
DOSE DI RADIAZIONE IONIZZANTE PERICOLO DA RADIAZIONI IONIZZANTI DOSE ASSORBITA D =!E AREA CONTROLLATA. energia assorbita nell'unità di massa
 DOSE DI RADIAZIONE IONIZZANTE PERICOLO DA RADIAZIONI IONIZZANTI DOSE ASSORBITA AREA CONTROLLATA D =!E!m energia assorbita nell'unità di massa 2 UNITA' DI MISURA dose assorbita D =!E!m dimensioni [D] =
DOSE DI RADIAZIONE IONIZZANTE PERICOLO DA RADIAZIONI IONIZZANTI DOSE ASSORBITA AREA CONTROLLATA D =!E!m energia assorbita nell'unità di massa 2 UNITA' DI MISURA dose assorbita D =!E!m dimensioni [D] =
Lo strofinio di qualsiasi oggetto provoca la comparsa su di esso di una carica elettrica che può attrarre piccoli oggetti.
 1. La natura elettrica della materia Lo strofinio di qualsiasi oggetto provoca la comparsa su di esso di una carica elettrica che può attrarre piccoli oggetti. La carica elettrica può essere positiva o
1. La natura elettrica della materia Lo strofinio di qualsiasi oggetto provoca la comparsa su di esso di una carica elettrica che può attrarre piccoli oggetti. La carica elettrica può essere positiva o
La relatività ristretta. Lezioni d'autore
 La relatività ristretta Lezioni d'autore Superquark-Albert Einstein Relatività (prima parte) VIDEO Superquark-Albert Einstein Relatività (seconda parte) VIDEO Materia e antimateria (a cura dell'agenzia
La relatività ristretta Lezioni d'autore Superquark-Albert Einstein Relatività (prima parte) VIDEO Superquark-Albert Einstein Relatività (seconda parte) VIDEO Materia e antimateria (a cura dell'agenzia
CAPITOLO 20 LA CHIMICA NUCLEARE
 CAPITOLO 20 LA CHIMICA NUCLEARE 20.5 (a) La soma dei numeri atomici e la somma dei numeri di massa, da entrambi i lati dell equazione nucleare, deve coincidere. Dalla parte sinistra di questa equazione
CAPITOLO 20 LA CHIMICA NUCLEARE 20.5 (a) La soma dei numeri atomici e la somma dei numeri di massa, da entrambi i lati dell equazione nucleare, deve coincidere. Dalla parte sinistra di questa equazione
Lezione 20: Atomi e molecole
 Lezione 20 - pag.1 Lezione 20: Atomi e molecole 20.1. Il punto della situazione Abbiamo visto, nella lezione precedente, come il modello atomico sia in grado di spiegare la grande varietà di sostanze che
Lezione 20 - pag.1 Lezione 20: Atomi e molecole 20.1. Il punto della situazione Abbiamo visto, nella lezione precedente, come il modello atomico sia in grado di spiegare la grande varietà di sostanze che
Cenni di fisica moderna
 Cenni di fisica moderna 1 fisica e salute la fisica delle radiazioni è molto utilizzata in campo medico esistono applicazioni delle radiazioni non ionizzanti nella terapia e nella diagnosi (laser per applicazioni
Cenni di fisica moderna 1 fisica e salute la fisica delle radiazioni è molto utilizzata in campo medico esistono applicazioni delle radiazioni non ionizzanti nella terapia e nella diagnosi (laser per applicazioni
LA STRUTTURA DELL ATOMO
 Capitolo 4 LA STRUTTURA DELL ATOMO N.B I concetti proposti sulle slide, in linea di massima seguono l ordine e i contenuti del libro, ma!!!! Ci possono essere delle variazioni Prof. Vincenzo Leo - Chimica
Capitolo 4 LA STRUTTURA DELL ATOMO N.B I concetti proposti sulle slide, in linea di massima seguono l ordine e i contenuti del libro, ma!!!! Ci possono essere delle variazioni Prof. Vincenzo Leo - Chimica
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 7 Le particelle dell atomo 3 Sommario (I) 1. La natura elettrica della materia 2. La scoperta delle proprietà elettriche 3. Le
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 7 Le particelle dell atomo 3 Sommario (I) 1. La natura elettrica della materia 2. La scoperta delle proprietà elettriche 3. Le
Esercizi su Chimica Nucleare e Nucleogenesi
 Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi su Chimica Nucleare e Nucleogenesi Prof. Dipartimento CMIC Giulio Natta http://chimicaverde.vosi.org/citterio/it//
Insegnamento di Chimica Generale 083424 - CCS CHI e MAT A.A. 2015/2016 (I Semestre) Esercizi su Chimica Nucleare e Nucleogenesi Prof. Dipartimento CMIC Giulio Natta http://chimicaverde.vosi.org/citterio/it//
La radioattività può avere un origine sia artificiale che naturale.
 http://www.isprambiente.gov.it/it/temi/radioattivita-e-radiazioni/ radioattivita/radioattivita-naturale-e-artificiale La radioattività può avere un origine sia artificiale che naturale. La radioattività
http://www.isprambiente.gov.it/it/temi/radioattivita-e-radiazioni/ radioattivita/radioattivita-naturale-e-artificiale La radioattività può avere un origine sia artificiale che naturale. La radioattività
Uomo, ambiente e radiazioni
 Uomo, ambiente e radiazioni Natura delle radiazioni 76 Le radiazioni di cui si tratta parlando di tecnologia nucleare sono le radiazioni ionizzanti Natura delle radiazioni Cosa sono le radiazioni ionizzanti?
Uomo, ambiente e radiazioni Natura delle radiazioni 76 Le radiazioni di cui si tratta parlando di tecnologia nucleare sono le radiazioni ionizzanti Natura delle radiazioni Cosa sono le radiazioni ionizzanti?
L unità di misura della dose nel S.I. è il Gray
 LA LA DOSE DOSE DA DA RADIAZIONE Le radiazioni (particelle, raggi gamma ) quando interagiscono con un mezzo cedono (tutta o parte) della loro energia al mezzo stesso. Si definisce allora la dose assorbita
LA LA DOSE DOSE DA DA RADIAZIONE Le radiazioni (particelle, raggi gamma ) quando interagiscono con un mezzo cedono (tutta o parte) della loro energia al mezzo stesso. Si definisce allora la dose assorbita
Chimica Nucleare. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Chimica Nucleare Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. 1 Riassunto Numero Atomico (Z) = numero di protoni nel nucleo Numero di Massa (A) = numero di
Chimica Nucleare Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. 1 Riassunto Numero Atomico (Z) = numero di protoni nel nucleo Numero di Massa (A) = numero di
Fisica del VITA MEDIA o <<TEMPO SCALA>> di una stella. RISERVA ENERGETICA (masse delle particelle) POTENZA IRRADIATA
 Bollitore tibetano Fisica del 1900 VITA MEDIA o di una stella RISERVA ENERGETICA (masse delle particelle) POTENZA IRRADIATA M i c h e l s o n In Fisica oramai, è soltanto questione di mettere
Bollitore tibetano Fisica del 1900 VITA MEDIA o di una stella RISERVA ENERGETICA (masse delle particelle) POTENZA IRRADIATA M i c h e l s o n In Fisica oramai, è soltanto questione di mettere
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 7 Le particelle dell atomo 1. La natura elettrica della materia 2. Le particelle fondamentali
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 7 Le particelle dell atomo 1. La natura elettrica della materia 2. Le particelle fondamentali
Interazione radiazione materia Dott.ssa Alessandra Bernardini
 Interazione radiazione materia Dott.ssa Alessandra Bernardini 1 Un po di storia Lo studio delle radiazioni ionizzanti come materia di interesse nasce nel novembre del 1895 ad opera del fisico tedesco Wilhelm
Interazione radiazione materia Dott.ssa Alessandra Bernardini 1 Un po di storia Lo studio delle radiazioni ionizzanti come materia di interesse nasce nel novembre del 1895 ad opera del fisico tedesco Wilhelm
Un po' di fisica nucleare: La radioattività
 Un po' di fisica nucleare: La radioattività at e ve de n d o.. = La radioattività La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle. La radioattività non
Un po' di fisica nucleare: La radioattività at e ve de n d o.. = La radioattività La radioattività è il fenomeno per cui alcuni nuclei si trasformano in altri emettendo particelle. La radioattività non
Unità didattica 10. Decima unità didattica (Fisica) 1. Corso integrato di Matematica e Fisica per il Corso di Farmacia
 Unità didattica 10 Radioattività... 2 L atomo... 3 Emissione di raggi x... 4 Decadimenti nucleari. 6 Il decadimento alfa.... 7 Il decadimento beta... 8 Il decadimento gamma...... 9 Interazione dei fotoni
Unità didattica 10 Radioattività... 2 L atomo... 3 Emissione di raggi x... 4 Decadimenti nucleari. 6 Il decadimento alfa.... 7 Il decadimento beta... 8 Il decadimento gamma...... 9 Interazione dei fotoni
Esercizi. 1. Fotoni, elettroni. 2. Struttura della materia. 3. Nuclei, radioattività. 4. Produzione e consumo di energia E-X - 0
 Esercizi 1. Fotoni, elettroni 2. Struttura della materia 3. Nuclei, radioattività 4. Produzione e consumo di energia E-X - 0 Calcolare il flusso di fotoni supposti monocromatici a lunghezza d onda di 450
Esercizi 1. Fotoni, elettroni 2. Struttura della materia 3. Nuclei, radioattività 4. Produzione e consumo di energia E-X - 0 Calcolare il flusso di fotoni supposti monocromatici a lunghezza d onda di 450
Peso Atomico. Tre problemi da risolvere!! (2) Quale unità di misura conviene adottare?
 Peso Atomico Tre problemi da risolvere!! (1) Difetto di massa (2) Quale unità di misura conviene adottare? (3) Come tener conto della miscela isotopica naturale per ciascun elemento? Il difetto di massa
Peso Atomico Tre problemi da risolvere!! (1) Difetto di massa (2) Quale unità di misura conviene adottare? (3) Come tener conto della miscela isotopica naturale per ciascun elemento? Il difetto di massa
A 2 Z A 2 Z. PROTONI: carica +e, massa 1840 m e NEUTRONI: carica nulla, massa 1842 m e
 PROTONI: carica +e, massa 1840 m e NEUTRONI: carica nulla, massa 184 m e Z = numero atomico = numero dei protoni (elettroni) proprietà chimiche A = numero di massa = numero dei protoni + neutroni massa
PROTONI: carica +e, massa 1840 m e NEUTRONI: carica nulla, massa 184 m e Z = numero atomico = numero dei protoni (elettroni) proprietà chimiche A = numero di massa = numero dei protoni + neutroni massa
Il modello strutturale dell atomo
 Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Teoria Atomica di Dalton
 Teoria Atomica di Dalton Il concetto moderno della materia si origina nel 1806 con la teoria atomica di John Dalton: Ogni elementoè composto di atomi. Gli atomi di un dato elemento sono uguali. Gli atomi
Teoria Atomica di Dalton Il concetto moderno della materia si origina nel 1806 con la teoria atomica di John Dalton: Ogni elementoè composto di atomi. Gli atomi di un dato elemento sono uguali. Gli atomi
COME E FATTA LA MATERIA
 ENERGIA NUCLEARE COME E FATTA LA MATERIA La Materia è composta di mattoni chiamati Atomi Tanti Atomi assieme compongono una Molecola Il nostro corpo e tutti gli oggetti sono fatti di Molecole, ovvero di
ENERGIA NUCLEARE COME E FATTA LA MATERIA La Materia è composta di mattoni chiamati Atomi Tanti Atomi assieme compongono una Molecola Il nostro corpo e tutti gli oggetti sono fatti di Molecole, ovvero di
Radiazione: propagazione di energia senza che vi sia né. Radiazioni ionizzanti radiazioni che hanno energia sufficiente per produrre la ionizzazione.
 Radiazioni Radiazione: propagazione di energia senza che vi sia né trasporto di quantità macroscopiche di materia, né necessità di un substrato materiale per la propagazione. L energia viene ceduta quando
Radiazioni Radiazione: propagazione di energia senza che vi sia né trasporto di quantità macroscopiche di materia, né necessità di un substrato materiale per la propagazione. L energia viene ceduta quando
Cenni di Fisica del Nucleo
 Capitolo 8 Cenni di Fisica del Nucleo 8.1 Proprietà generali dei nuclei In questo capitolo affrontiamo lo studio dei nuclei. Un nucleo è un insieme di neutroni e protoni legati insieme ( incollati ) dalla
Capitolo 8 Cenni di Fisica del Nucleo 8.1 Proprietà generali dei nuclei In questo capitolo affrontiamo lo studio dei nuclei. Un nucleo è un insieme di neutroni e protoni legati insieme ( incollati ) dalla
ATOMI E MOLECOLE. Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti).
 1 ATOMI E MOLECOLE Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti). Un elemento (es. il mercurio) è una sostanza che non può
1 ATOMI E MOLECOLE Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti). Un elemento (es. il mercurio) è una sostanza che non può
2 HCl. H 2 + Cl 2 ATOMI E MOLECOLE. Ipotesi di Dalton
 Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
RADIAZIONI IONIZZANTI
 RADIAZIONI IONIZZANTI PREMESSA Le radiazioni ionizzanti sono quelle radiazioni dotate di sufficiente energia da poter ionizzare gli atomi (o le molecole) con i quali vengono a contatto. La caratteristica
RADIAZIONI IONIZZANTI PREMESSA Le radiazioni ionizzanti sono quelle radiazioni dotate di sufficiente energia da poter ionizzare gli atomi (o le molecole) con i quali vengono a contatto. La caratteristica
Capitolo 2. Cenni alla Composizione e Struttura dell atomo
 Master in Verifiche di qualità in radiodiagnostica, medicina nucleare e radioterapiar Capitolo 2 Cenni alla Composizione e Struttura dell atomo 24 Atomi, Molecole,, e Ioni L idea di Atomo è antica come
Master in Verifiche di qualità in radiodiagnostica, medicina nucleare e radioterapiar Capitolo 2 Cenni alla Composizione e Struttura dell atomo 24 Atomi, Molecole,, e Ioni L idea di Atomo è antica come
CHIMICA: studio della struttura e delle trasformazioni della materia
 CHIMICA: studio della struttura e delle trasformazioni della materia 1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
CHIMICA: studio della struttura e delle trasformazioni della materia 1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
Corso di CHIMICA INORGANICA
 Corso di CHIMICA INORGANICA Lezione Seconda La teoria atomica La massa atomica e il concetto di Isotopi Dentro l atomo, le particelle subatomiche La Tavola Periodica degli Elementi 2 Gli atomi di un certo
Corso di CHIMICA INORGANICA Lezione Seconda La teoria atomica La massa atomica e il concetto di Isotopi Dentro l atomo, le particelle subatomiche La Tavola Periodica degli Elementi 2 Gli atomi di un certo
LA STRUTTURA DELLE MOLECOLE. Orbitali molecolari e legame chimico
 LA STRUTTURA DELLE MOLECOLE Orbitali molecolari e legame chimico GLI ORBITALI MOLECOLARI Quando degli atomi collidono tra di loro i loro nuclei ed elettroni vengono a trovarsi in prossimità influenzandosi
LA STRUTTURA DELLE MOLECOLE Orbitali molecolari e legame chimico GLI ORBITALI MOLECOLARI Quando degli atomi collidono tra di loro i loro nuclei ed elettroni vengono a trovarsi in prossimità influenzandosi
Capitolo 3 LA RADIOATTIVITA AMBIENTALE
 Capitolo 3 LA RADIOATTIVITA AMBIENTALE La radioattività (o decadimento radioattivo) Ogni elemento X viene rappresentato dal numero atomico Z, pari al numero di protoni, e dal numero di massa A, uguale
Capitolo 3 LA RADIOATTIVITA AMBIENTALE La radioattività (o decadimento radioattivo) Ogni elemento X viene rappresentato dal numero atomico Z, pari al numero di protoni, e dal numero di massa A, uguale
Fenomeni quantistici
 Fenomeni quantistici 1. Radiazione di corpo nero Leggi di Wien e di Stefan-Boltzman Equipartizione dell energia classica Correzione quantistica di Planck 2. Effetto fotoelettrico XIII - 0 Radiazione da
Fenomeni quantistici 1. Radiazione di corpo nero Leggi di Wien e di Stefan-Boltzman Equipartizione dell energia classica Correzione quantistica di Planck 2. Effetto fotoelettrico XIII - 0 Radiazione da
Principi della RadioDatazione
 Principi della RadioDatazione Datazione di un manufatto contenente Smalto a base di Ossido di Uranio Lodovico Lappetito RadioDatazione - 14/07/2015 Pag. 1 Sommario Uranio... 3 RadioDatazione mediante confronto
Principi della RadioDatazione Datazione di un manufatto contenente Smalto a base di Ossido di Uranio Lodovico Lappetito RadioDatazione - 14/07/2015 Pag. 1 Sommario Uranio... 3 RadioDatazione mediante confronto
Istituzioni di Fisica Nucleare e Subnucleare Prof. A. Andreazza. Lezione 10. Fusione nucleare
 Istituzioni di Fisica Nucleare e Subnucleare Prof. A. Andreazza Lezione 10 Fusione nucleare Fusione nucleare (Das-Ferbel, cap. 5.3) Abbiamo già accennato alla fusione nucleare che costituisce la sorgente
Istituzioni di Fisica Nucleare e Subnucleare Prof. A. Andreazza Lezione 10 Fusione nucleare Fusione nucleare (Das-Ferbel, cap. 5.3) Abbiamo già accennato alla fusione nucleare che costituisce la sorgente
Camera a Ioni. Misure di Radon. Sistema Theremino Rev.1. Sistema Theremino IonChamber_ITA - 22/06/2015 Pag. 1
 Camera a Ioni Misure di Radon Sistema Theremino Rev.1 Sistema Theremino IonChamber_ITA - 22/06/2015 Pag. 1 Sommario Misure con Camera a Ioni... 3 Teoria... 3 Apparecchiature... 3 Radon in abitazione -
Camera a Ioni Misure di Radon Sistema Theremino Rev.1 Sistema Theremino IonChamber_ITA - 22/06/2015 Pag. 1 Sommario Misure con Camera a Ioni... 3 Teoria... 3 Apparecchiature... 3 Radon in abitazione -
Cos è. la Chimica? G. Micera Chimica Generale e Inorganica
 Cos è la Chimica? La Chimica descrive la materia, le sue proprietà, le trasformazioni che essa subisce, e le variazioni di energia associate Materia è tutto ciò che ha massa e volume Energia è la capacità
Cos è la Chimica? La Chimica descrive la materia, le sue proprietà, le trasformazioni che essa subisce, e le variazioni di energia associate Materia è tutto ciò che ha massa e volume Energia è la capacità
Parte I - LE RADIAZIONI IONIZZANTI E LE GRANDEZZE FISICHE DI INTERESSE IN DOSIMETRIA
 INDICE Parte I - LE RADIAZIONI IONIZZANTI E LE GRANDEZZE FISICHE DI INTERESSE IN DOSIMETRIA Capitolo 1 Le radiazioni ionizzanti 19 1.1 Introduzione 19 1.2 Il fondo naturale di radiazione 21 1.2.1 La radiazione
INDICE Parte I - LE RADIAZIONI IONIZZANTI E LE GRANDEZZE FISICHE DI INTERESSE IN DOSIMETRIA Capitolo 1 Le radiazioni ionizzanti 19 1.1 Introduzione 19 1.2 Il fondo naturale di radiazione 21 1.2.1 La radiazione
CORSO DI PERFEZIONAMENTO
 UNIVERSITÀ DEGLI STUDI DI SIENA DIPARTIMENTO DI FISICA CORSO DI PERFEZIONAMENTO PERCORSI DIDATTICI DI FISICA E MATEMATICA: MODELLI, VERIFICHE SPERIMENTALI, STATISTICA ATOMI E CARICA ELETTRICA: PROPOSTA
UNIVERSITÀ DEGLI STUDI DI SIENA DIPARTIMENTO DI FISICA CORSO DI PERFEZIONAMENTO PERCORSI DIDATTICI DI FISICA E MATEMATICA: MODELLI, VERIFICHE SPERIMENTALI, STATISTICA ATOMI E CARICA ELETTRICA: PROPOSTA
La fusione. Lezioni d'autore. di Claudio Cigognetti
 La fusione Lezioni d'autore di Claudio Cigognetti La bomba H (da Ulisse Rai) VIDEO VIDEO Il plasma costituito da un gas di ioni, elettroni, atomi o molecole complessivamente neutro in esso dominano gli
La fusione Lezioni d'autore di Claudio Cigognetti La bomba H (da Ulisse Rai) VIDEO VIDEO Il plasma costituito da un gas di ioni, elettroni, atomi o molecole complessivamente neutro in esso dominano gli
Particelle Subatomiche
 GLI ATOMI Particelle Subatomiche ELEMENTI I diversi atomi sono caratterizzati da un diverso numero di protoni e neutroni; il numero di elettroni è sempre uguale al numero dei protoni (negli atomi neutri)
GLI ATOMI Particelle Subatomiche ELEMENTI I diversi atomi sono caratterizzati da un diverso numero di protoni e neutroni; il numero di elettroni è sempre uguale al numero dei protoni (negli atomi neutri)
Corso di tecnologia Scuola media a.s PROF. NICOLA CARIDI
 Corso di tecnologia Scuola media a.s. 2008-2009 PROF. NICOLA CARIDI ARGOMENTI TRATTATI: CHE COS E L ENERGIA NUCLEARE MOLECOLE ATOMO L EQUAZIONE DI EINSTEIN URANIO FISSIONE FUSIONE CENTRALI NUCLEARI CHE
Corso di tecnologia Scuola media a.s. 2008-2009 PROF. NICOLA CARIDI ARGOMENTI TRATTATI: CHE COS E L ENERGIA NUCLEARE MOLECOLE ATOMO L EQUAZIONE DI EINSTEIN URANIO FISSIONE FUSIONE CENTRALI NUCLEARI CHE
L energia assorbita dall atomo durante l urto iniziale è la stessa del fotone che sarebbe emesso nel passaggio inverso, e quindi vale: m
 QUESITI 1 Quesito Nell esperimento di Rutherford, una sottile lamina d oro fu bombardata con particelle alfa (positive) emesse da una sorgente radioattiva. Secondo il modello atomico di Thompson le particelle
QUESITI 1 Quesito Nell esperimento di Rutherford, una sottile lamina d oro fu bombardata con particelle alfa (positive) emesse da una sorgente radioattiva. Secondo il modello atomico di Thompson le particelle
Capitolo 8 I LEGAMI CHIMICI Aspetti elettrostatici ed energetici dei legami chimici
 Capitolo 8 I LEGAMI CHIMICI 8.1. Aspetti elettrostatici ed energetici dei legami chimici Le forze di attrazione che tengono uniti gli atomi in una molecola sono dette legami chimici N.B I concetti proposti
Capitolo 8 I LEGAMI CHIMICI 8.1. Aspetti elettrostatici ed energetici dei legami chimici Le forze di attrazione che tengono uniti gli atomi in una molecola sono dette legami chimici N.B I concetti proposti
Sm, T 1/ 2. Il decadimento alfa
 Il decadimento alfa L emissione di particelle α da parte di vari radionuclidi rappresenta una delle prime scoperte della fisica moderna: nel 1908 utherford dimostrò che tale radiazione è costituita da
Il decadimento alfa L emissione di particelle α da parte di vari radionuclidi rappresenta una delle prime scoperte della fisica moderna: nel 1908 utherford dimostrò che tale radiazione è costituita da
I LEGAMI CHIMICI. I legami chimici si formano quando gli atomi cedono, acquistano oppure mettono in comune
 I LEGAMI CHIMICI I legami chimici si formano quando gli atomi cedono, acquistano oppure mettono in comune alcuni elettroni con altri atomi, per completare il guscio elettronico più esterno. 1. LEGAME IONICO
I LEGAMI CHIMICI I legami chimici si formano quando gli atomi cedono, acquistano oppure mettono in comune alcuni elettroni con altri atomi, per completare il guscio elettronico più esterno. 1. LEGAME IONICO
Misura del coefficiente di assorbimento di vari materiali in funzione dell'energia del fascio dei fotoni incidenti
 materiali in funzione dell'energia del fascio dei fotoni Esperto Qualificato LNF - INFN Interazioni delle particelle indirettamente ionizzanti con la materia Le particelle indirettamente ionizzanti, principalmente
materiali in funzione dell'energia del fascio dei fotoni Esperto Qualificato LNF - INFN Interazioni delle particelle indirettamente ionizzanti con la materia Le particelle indirettamente ionizzanti, principalmente
Le particelle dell atomo
 La carica elettrica I fenomeni elettrici sono noti fin dall antichità: gli antichi Greci usavano la parola elektron per spiegare il fenomeno dell elettrizzazione dell ambra. I Greci sapevano che strofinando
La carica elettrica I fenomeni elettrici sono noti fin dall antichità: gli antichi Greci usavano la parola elektron per spiegare il fenomeno dell elettrizzazione dell ambra. I Greci sapevano che strofinando
Esercitazioni di Elementi di Chimica. Modulo 2 Struttura della Materia
 Esercitazioni di Elementi di Chimica Modulo 2 Struttura della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Qual è lo stato fisico
Esercitazioni di Elementi di Chimica Modulo 2 Struttura della Materia Esempi di quiz a risposta multipla e questionari a completamento L esame finale sarà composto da problemi simili Qual è lo stato fisico
E = MC². È: Una forma di energia che deriva da profonde modificazioni della struttura stessa della materia. ENERGIA NUCLEARE
 ENERGIA NUCLEARE È: Una forma di energia che deriva da profonde modificazioni della struttura stessa della materia. La materia Può trasformarsi in energia secondo la legge fisica, scoperta dallo scienziato
ENERGIA NUCLEARE È: Una forma di energia che deriva da profonde modificazioni della struttura stessa della materia. La materia Può trasformarsi in energia secondo la legge fisica, scoperta dallo scienziato
Theory Italiano (Italy)
 Q3-1 Large Hadron Collider (10 punti) Prima di iniziare questo problema, leggi le istruzioni generali nella busta a parte. In questo problema è discussa la fisica dell acceleratore di particelle del CERN
Q3-1 Large Hadron Collider (10 punti) Prima di iniziare questo problema, leggi le istruzioni generali nella busta a parte. In questo problema è discussa la fisica dell acceleratore di particelle del CERN
15/04/2014. Serway, Jewett Principi di Fisica IV Ed. Capitolo 8. Generalizziamo, considerando due particelle interagenti.
 Serway, Jewett Principi di Fisica IV Ed. Capitolo 8 Esempio arciere su una superficie ghiacciata che scocca la freccia: l arciere (60 kg) esercita una forza sulla freccia 0.5 kg (che parte in avanti con
Serway, Jewett Principi di Fisica IV Ed. Capitolo 8 Esempio arciere su una superficie ghiacciata che scocca la freccia: l arciere (60 kg) esercita una forza sulla freccia 0.5 kg (che parte in avanti con
Fisica atomica. Marcello Borromeo corso di Fisica per Farmacia - Anno Accademico
 Fisica atomica Nel 1905 Einstein sostiene che la luce viaggia in pacchetti di energia, chiamati fotoni Ogni fotone ha energia proporzionale alla propria frequenza E = hν: h = 6.626 10 34 J s è chiamata
Fisica atomica Nel 1905 Einstein sostiene che la luce viaggia in pacchetti di energia, chiamati fotoni Ogni fotone ha energia proporzionale alla propria frequenza E = hν: h = 6.626 10 34 J s è chiamata
La fisica del XX secolo ovvero la tecnologia consente di eseguire esperimenti sempre più spinti e. tutto deve essere messo in discussione
 ovvero la tecnologia consente di eseguire esperimenti sempre più spinti e. tutto deve essere messo in discussione The fundamental cause of the trouble is that in the modern world the stupid are cocksure
ovvero la tecnologia consente di eseguire esperimenti sempre più spinti e. tutto deve essere messo in discussione The fundamental cause of the trouble is that in the modern world the stupid are cocksure
NATURA DELL ENERGIA. L energia è tutta intorno a noi!
 NATURA DELL ENERGIA L energia è tutta intorno a noi! Si può ascoltare l'energia come suono Si può vedere l'energia come luce Si può sentire l energia come vento NATURA DELL ENERGIA Utilizzi l energia quando:
NATURA DELL ENERGIA L energia è tutta intorno a noi! Si può ascoltare l'energia come suono Si può vedere l'energia come luce Si può sentire l energia come vento NATURA DELL ENERGIA Utilizzi l energia quando:
Elementi sistemati nella TAVOLA PERIODICA DEGLI ELEMENTI in base al numero atomico crescente O, H, N, C (+ del 96% della materia vivente)
 OVERVIEW Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi
OVERVIEW Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi
Sulla superficie interna del guscio sferico (induzione totale) si avrà la carica indotta q distribuita uniformemente, quindi
 1) Una sfera conduttrice di raggio r = 5 cm possiede una carica q = 10 8 C ed è posta nel centro di un guscio sferico conduttore, di raggio interno R = 20 cm, posto in contatto con la terra (a massa).
1) Una sfera conduttrice di raggio r = 5 cm possiede una carica q = 10 8 C ed è posta nel centro di un guscio sferico conduttore, di raggio interno R = 20 cm, posto in contatto con la terra (a massa).
INTERAZIONI DELLE RADIAZIONI CON LA MATERIA
 M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna mario.marengo@unibo.it Si definiscono radiazioni ionizzanti tutte le
M. Marengo INTERAZIONI DELLE RADIAZIONI CON LA MATERIA Servizio di Fisica Sanitaria Ospedale Policlinico S.Orsola - Malpighi, Bologna mario.marengo@unibo.it Si definiscono radiazioni ionizzanti tutte le
Le sostanze chimiche
 Le sostanze chimiche Ingredienti base della materia La materia si presenta con diverse forme. Accade perché esistono moltissimi «ingredienti di base» che mescolandosi tra loro danno innumerevoli combinazioni.
Le sostanze chimiche Ingredienti base della materia La materia si presenta con diverse forme. Accade perché esistono moltissimi «ingredienti di base» che mescolandosi tra loro danno innumerevoli combinazioni.
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni
 CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni composto materia sostanza pura miscela omogenea elemento eterogenea Elementi, Composti e Miscele Miscela eterogenea
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni composto materia sostanza pura miscela omogenea elemento eterogenea Elementi, Composti e Miscele Miscela eterogenea
Radioattività artificiale Origine e impieghi
 ORIGIE DELL RDIOTTIVIT Radioattività naturale Raggi cosmici (primari e secondari) Radionuclidi primordiali (isolati) Famiglie radioattive naturali Radioattività artificiale Origine e impieghi L L RDIOTTIVIT
ORIGIE DELL RDIOTTIVIT Radioattività naturale Raggi cosmici (primari e secondari) Radionuclidi primordiali (isolati) Famiglie radioattive naturali Radioattività artificiale Origine e impieghi L L RDIOTTIVIT
L abbondanza degli elementi nell universo
 L abbondanza degli elementi nell universo Abbondanze nel sistema solare Abbondanze fotosferiche e meteoriche Abbondanze cosmiche Chi da dove? a)nucleosisntesi primordiale b)nucleosintesi stellare fino
L abbondanza degli elementi nell universo Abbondanze nel sistema solare Abbondanze fotosferiche e meteoriche Abbondanze cosmiche Chi da dove? a)nucleosisntesi primordiale b)nucleosintesi stellare fino
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
LE ONDE E I FONDAMENTI DELLA TEORIA QUANTISTICA
 LE ONDE E I FONDAMENTI DELLA TEORIA QUANTISTICA I PROBLEMI DEL MODELLO PLANETARIO F Secondo Rutherford l elettrone si muoverebbe sulla sua orbita in equilibrio tra la forza elettrica di attrazione del
LE ONDE E I FONDAMENTI DELLA TEORIA QUANTISTICA I PROBLEMI DEL MODELLO PLANETARIO F Secondo Rutherford l elettrone si muoverebbe sulla sua orbita in equilibrio tra la forza elettrica di attrazione del
Bilancio di energia: il Primo Principio della Termodinamica. Termodinamica dell Ingegneria Chimica
 Bilancio di energia: il Primo Principio della Termodinamica Termodinamica dell Ingegneria Chimica 1 I Sistemi termodinamici Un sistema è definito da una superficie di controllo, reale o immaginaria, che
Bilancio di energia: il Primo Principio della Termodinamica Termodinamica dell Ingegneria Chimica 1 I Sistemi termodinamici Un sistema è definito da una superficie di controllo, reale o immaginaria, che
CORSO DI LAUREA IN OTTICA E OPTOMETRIA
 CORSO DI LAUREA IN OTTICA E OPTOMETRIA Anno Accademico 007-008 CORSO di FISCA ED APPLICAZIONE DEI LASERS Questionario del Primo appello della Sessione Estiva NOME: COGNOME: MATRICOLA: VOTO: /30 COSTANTI
CORSO DI LAUREA IN OTTICA E OPTOMETRIA Anno Accademico 007-008 CORSO di FISCA ED APPLICAZIONE DEI LASERS Questionario del Primo appello della Sessione Estiva NOME: COGNOME: MATRICOLA: VOTO: /30 COSTANTI
CAMERA A NEBBIA. Cos è una camera a nebbia? Una foto famosa: CAMERA A NEBBIA e scoperta del POSITRONE
 Cos è una camera a nebbia? CAMERA A NEBBIA UN ESEMPIO «STORICO» E UN UTILIZZO DI CAMERA A NEBBIA «HOME MADE» PER LA VISUALIZZAZIONE DI RADIAZIONE ALFA, BETA E DI RAGGI COSMICI Una camera a nebbia è un
Cos è una camera a nebbia? CAMERA A NEBBIA UN ESEMPIO «STORICO» E UN UTILIZZO DI CAMERA A NEBBIA «HOME MADE» PER LA VISUALIZZAZIONE DI RADIAZIONE ALFA, BETA E DI RAGGI COSMICI Una camera a nebbia è un
Le leggi di conservazione nei decadimenti radioattivi: gli isotopi e il numero di massa
 Le leggi di conservazione nei decadimenti radioattivi: gli isotopi e il numero di massa A questo punto è necessario aprire una parentesi sulla struttura interna dei nuclei. Oggi noi sappiamo che i nuclei
Le leggi di conservazione nei decadimenti radioattivi: gli isotopi e il numero di massa A questo punto è necessario aprire una parentesi sulla struttura interna dei nuclei. Oggi noi sappiamo che i nuclei
RIFERIMENTI NORMATIVI E LINEE GUIDA NAZIONALI PER I CONTROLLI RADIOMETRICI SULLE ACQUE POTABILI
 RIFERIMENTI NORMATIVI E LINEE GUIDA NAZIONALI PER I CONTROLLI RADIOMETRICI SULLE ACQUE POTABILI Elena Caldognetto Osservatorio Agenti Fisici ARPAV Verona LA RADIOATTIVITÀ NELLE ACQUE POTABILI DEL VENETO
RIFERIMENTI NORMATIVI E LINEE GUIDA NAZIONALI PER I CONTROLLI RADIOMETRICI SULLE ACQUE POTABILI Elena Caldognetto Osservatorio Agenti Fisici ARPAV Verona LA RADIOATTIVITÀ NELLE ACQUE POTABILI DEL VENETO
L2 - Completa la seguente frase: "L'auto sta al telaio come il corpo sta..."
 Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come continua questa serie di numeri? 3-4 - 6-9 - 13-18 -... a) 21 b) 22 c) 23 d) 24 L2 - Completa
Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come continua questa serie di numeri? 3-4 - 6-9 - 13-18 -... a) 21 b) 22 c) 23 d) 24 L2 - Completa
Elettricità e Fisica Moderna
 Esercizi di fisica per Medicina C.Patrignani, Univ. Genova (rev: 9 Ottobre 2003) 1 Elettricità e Fisica Moderna 1) Una candela emette una potenza di circa 1 W ad una lunghezza d onda media di 5500 Å a)
Esercizi di fisica per Medicina C.Patrignani, Univ. Genova (rev: 9 Ottobre 2003) 1 Elettricità e Fisica Moderna 1) Una candela emette una potenza di circa 1 W ad una lunghezza d onda media di 5500 Å a)
Radioattivita (radiazioni ionizzanti) e salute. 1a parte
 Radioattivita (radiazioni ionizzanti) e salute Cristiana Peroni Dipartimento di Fisica Sperimentale dell Universita di Torine e Istituto Nazionale di Fisica Nucleare 1a parte 4/11/2005 C.Peroni 1 Che cosa
Radioattivita (radiazioni ionizzanti) e salute Cristiana Peroni Dipartimento di Fisica Sperimentale dell Universita di Torine e Istituto Nazionale di Fisica Nucleare 1a parte 4/11/2005 C.Peroni 1 Che cosa
p e c = ev Å
 Corso di Introduzione alla Fisica Quantistica (f) Soluzioni Esercizi: Giugno 006 * Quale la lunghezza d onda di de Broglie di un elettrone che ha energia cinetica E 1 = KeV e massa a riposo m 0 = 9.11
Corso di Introduzione alla Fisica Quantistica (f) Soluzioni Esercizi: Giugno 006 * Quale la lunghezza d onda di de Broglie di un elettrone che ha energia cinetica E 1 = KeV e massa a riposo m 0 = 9.11
4. Lo spettro discreto: emissione e assorbimento di luce da parte di atomi stato fondamentale stati eccitati
 4. Lo spettro discreto: emissione e assorbimento di luce da parte di atomi Accanto allo spettro continuo che i corpi emettono in ragione del loro stato termico, si osservano spettri discreti che sono caratteristici
4. Lo spettro discreto: emissione e assorbimento di luce da parte di atomi Accanto allo spettro continuo che i corpi emettono in ragione del loro stato termico, si osservano spettri discreti che sono caratteristici
E= mc2 Nel 1905 Einistein enunciò la sua teoria tra energia e materia, espressa dalla formula E=mc2
 ENERGIA NUCLEARE URANIO L uranio è un metallo di colore bianco argenteo che pesa più del doppio del ferro. si ricava dall uranite. E un minerale che contiene due tipi di elementi 1. Uranio 238 non fissile
ENERGIA NUCLEARE URANIO L uranio è un metallo di colore bianco argenteo che pesa più del doppio del ferro. si ricava dall uranite. E un minerale che contiene due tipi di elementi 1. Uranio 238 non fissile
Chimica. 1) Il simbolo del Carbonio è: A) C B) Ca. C) Ce D) Cu. 2) Secondo il principio della conservazione della materia:
 Chimica 1) Il simbolo del Carbonio è: A) C B) Ca C) Ce D) Cu 2) Secondo il principio della conservazione della materia: A) Durante le reazioni chimiche il numero totale di atomi di ciascun elemento chimico
Chimica 1) Il simbolo del Carbonio è: A) C B) Ca C) Ce D) Cu 2) Secondo il principio della conservazione della materia: A) Durante le reazioni chimiche il numero totale di atomi di ciascun elemento chimico
Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm].
![Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm]. Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm].](/thumbs/62/47096832.jpg) Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm]. Esercizio9: un fotone gamma sparisce formando una coppia
Esercizio8: il lavoro di estrazione per il tungsteno é 4.49 ev. Calcolare la lunghezza d onda massima per ottenere effetto fotoelettrico [275.6 nm]. Esercizio9: un fotone gamma sparisce formando una coppia
Fisica delle Apparecchiature per Radioterapia, lez. III RADIOTERAPIA M. Ruspa 1
 RADIOTERAPIA 14.01.11 M. Ruspa 1 Con il termine RADIOTERAPIA si intende l uso di radiazioni ionizzanti altamente energetiche (fotoni X o gamma, elettroni, protoni) nel trattamento dei tumori. La radiazione
RADIOTERAPIA 14.01.11 M. Ruspa 1 Con il termine RADIOTERAPIA si intende l uso di radiazioni ionizzanti altamente energetiche (fotoni X o gamma, elettroni, protoni) nel trattamento dei tumori. La radiazione
LA FISICA DELLE RADIAZIONI IONIZZANTI
 LA FISICA DELLE RADIAZIONI IONIZZANTI MINISTERO DELL INTERNO Dipartimento dei Vigili del Fuoco, del Soccorso Pubblico e della Difesa Civile Ispettorato Nazionale del Corpo Militare della Croce Rossa Italiana
LA FISICA DELLE RADIAZIONI IONIZZANTI MINISTERO DELL INTERNO Dipartimento dei Vigili del Fuoco, del Soccorso Pubblico e della Difesa Civile Ispettorato Nazionale del Corpo Militare della Croce Rossa Italiana
P. Sapia Università della Calabria. a.a. 2009/10
 FISICA PER I BENI CULTURALI Ii MATERIA E INTERAZIONE CON LA RADIAZIONE P. Sapia Università della Calabria a.a. 2009/10 Interazioni fondamentali Gravitazionale Debolmente attrattiva, tra tutte le particelle
FISICA PER I BENI CULTURALI Ii MATERIA E INTERAZIONE CON LA RADIAZIONE P. Sapia Università della Calabria a.a. 2009/10 Interazioni fondamentali Gravitazionale Debolmente attrattiva, tra tutte le particelle
Struttura e dimensione della materia La radioattività
 Struttura e dimensione della materia La radioattività Docente: Ing. Mauro Malizia Comandante Provinciale comando.ascolipiceno@vigilfuoco.it Via del Commercio, 48 Ascoli Piceno Tel. 0736 3531 www.vigilfuoco.it/sitivvf/ascolipiceno
Struttura e dimensione della materia La radioattività Docente: Ing. Mauro Malizia Comandante Provinciale comando.ascolipiceno@vigilfuoco.it Via del Commercio, 48 Ascoli Piceno Tel. 0736 3531 www.vigilfuoco.it/sitivvf/ascolipiceno
Stabilita' dei nuclei
 Il Nucleo Nucleo e' costituito da nucleoni (protoni e neutroni). Mentre i neutroni liberi sono abbastanza instabili tendono a decadere in un protone ed un elettrone (t1/2 circa 900 s), i protoni sono stabili.
Il Nucleo Nucleo e' costituito da nucleoni (protoni e neutroni). Mentre i neutroni liberi sono abbastanza instabili tendono a decadere in un protone ed un elettrone (t1/2 circa 900 s), i protoni sono stabili.
FORMULE DI USO CORRENTE PER I CALCOLI NEGLI INTERVENTI IN PRESENZA DI SOSTANZE RADIOATTIVE
 FORMULE DI USO CORRENTE PER I CALCOLI NEGLI INTERVENTI IN PRESENZA DI SOSTANZE RADIOATTIVE Misura dell'attività della sorgente L'attività della sorgente si valuta mediante il numero di disintegrazioni
FORMULE DI USO CORRENTE PER I CALCOLI NEGLI INTERVENTI IN PRESENZA DI SOSTANZE RADIOATTIVE Misura dell'attività della sorgente L'attività della sorgente si valuta mediante il numero di disintegrazioni
A1.1 Elettrostatica. Particella Carica elettrica Massa. Elettrone 1,602 x C 9,108 x kg. Protone 1,602 x C 1,672 x kg
 A1.1 Elettrostatica Nell affrontare lo studio dell elettrotecnica si segue di solito un percorso che vede, in successione, lo studio dell elettrostatica (campo elettrico), quindi della corrente elettrica,
A1.1 Elettrostatica Nell affrontare lo studio dell elettrotecnica si segue di solito un percorso che vede, in successione, lo studio dell elettrostatica (campo elettrico), quindi della corrente elettrica,
DISTRIBUZIONI DISTRIBUZIONE DI GAUSS
 DISTRIBUZIONI ESPERIENZA a: DISTRIBUZIONE DI GAUSS SCOPO: Costruzione di una distribuzione di Gauss dai valori di una grandezza fisica ottenuti da una misura dominata da errori casuali. Studio dell influenza
DISTRIBUZIONI ESPERIENZA a: DISTRIBUZIONE DI GAUSS SCOPO: Costruzione di una distribuzione di Gauss dai valori di una grandezza fisica ottenuti da una misura dominata da errori casuali. Studio dell influenza
Esame svizzero di maturità Estate 2014 SCIENZE SPERIMENTALI FISICA
 Esame svizzero di maturità Estate 2014 Cognome e nome:... Gruppo e numero:... SCIENZE SPERIMENTALI FISICA Argomenti proposti Problema 1: un urto molto classico Problema 2: pressione idrostatica, energia
Esame svizzero di maturità Estate 2014 Cognome e nome:... Gruppo e numero:... SCIENZE SPERIMENTALI FISICA Argomenti proposti Problema 1: un urto molto classico Problema 2: pressione idrostatica, energia
