L Atomo e le Molecole
|
|
|
- Bruno Albano Angeli
- 7 anni fa
- Visualizzazioni
Transcript
1 L Atomo e le Molecole
2 L atomo L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime: i protoni, i neutroni e gli elettroni.
3 Protoni e Neutroni I protoni e i neutroni formano insieme quello che possiamo definire il cuore dell'atomo: il nucleo.
4 Protoni e Neutroni Queste due particelle hanno più o meno la stessa massa, cioè sono formate da una quantità di materia quasi uguale. Il protone, però, è diverso dal neutrone perché ha una proprietà, chiamata carica elettrica positiva, che il neutrone non possiede.
5 Intorno al nucleo si muovono rapidissimamente altre particelle: gli elettroni. Gli elettroni
6 Gli elettroni Essi hanno una massa così piccola che ne servono 1836 per uguagliare la massa di un protone. Anche gli elettroni hanno una carica elettrica, ma essa è diversa da quella del protone: è una carica elettrica negativa.
7 L atomo neutro In un atomo in condizioni normali il numero degli elettroni è sempre uguale a quello dei protoni: a un certo numero di cariche positive corrisponde un ugual numero di cariche negative. L'atomo, dunque, risulta neutro, né positivo né negativo.
8 Gli atomi sono tutti uguali tra loro? Pur essendo tutti formati dalle stesse particelle, gli atomi non sono tutti uguali tra loro: alcuni sono più piccoli, altri più grandi. La piccolezza o la grandezza di un atomo dipende dal numero di protoni del suo nucleo.
9 Gli atomi sono tutti uguali tra loro? L'atomo più piccolo ha il nucleo composto da un solo protone; il più grande in natura possiede ben 92 protoni.
10 Gli atomi sono tutti uguali tra loro? Questi atomi hanno un diverso numero atomico, termine che indica quanti protoni sono presenti nel nucleo: il primo ha numero atomico 1 perché ha un solo protone e l ultimo ha numero atomico 92 perché ha 92 protoni.
11 Gli atomi hanno un nome? Il numero atomico permette di distinguere un atomo da un altro: questo consente anche di dare un nome a ciascuno di essi.
12 Gli atomi hanno un nome? L'atomo più piccolo, quello con un solo protone, è l'idrogeno; il più grande in natura si chiama uranio e ha 92 protoni. L'atomo che possiede 7 protoni è quello dell'azoto, una sostanza presente nell'aria; l'atomo con numero atomico 8, cioè con 8 protoni, è l'ossigeno, il gas che ci permette di respirare.
13 Gli atomi hanno un nome? Imparerai il nome di molti altri atomi: carbonio, rame, ferro, oro, argento, sodio, cloro... Essi si definiscono elementi chimici.
14 I simboli degli elementi chimici Ogni elemento chimico, per brevità, è indicato con un simbolo, che deriva dal nome dell'atomo. Ogni simbolo è formato dalla prima o dalle prime due lettere del nome dell'atomo, per non creare confusione tra atomi i cui nomi hanno la stessa iniziale.
15 I simboli degli elementi chimici Per esempio il simbolo del carbonio è C (si legge ci), quello del calcio è Ca (si legge ci-a) e quello del cloro è Cl (si legge cielle). Ci sono poi alcuni elementi il cui simbolo è molto diverso da quello del loro nome.
16 I simboli degli elementi chimici Così il simbolo dell'oro è Au, perché è ricavato dal termine latino aurum; quello del rame è Cu, perché gli antichi romani chiamavano il rame cuprum.
17 La Tavola degli Elementi La tavola periodica degli elementi è lo schema col quale vengono ordinati gli atomi sulla base del loro numero atomico. Ideata dal chimico russo Mendeleev nel 1869, inizialmente contava numerosi spazi vuoti, previsti per gli elementi che sarebbero stati scoperti in futuro, taluni nella seconda metà del
18 La Tavola degli Elementi
19 Quando gli atomi si uniscono: La Molecola Gli atomi hanno la capacità di unirsi tra loro formando le molecole. Ma che cos'è una molecola? La molecola è la più piccola particella di una sostanza che ne conserva tutte le proprietà.
20 Quando gli atomi si uniscono: La Molecola Un esempio di molecola è la molecola dell'acqua. Se potessimo spezzare questa particella, i suoi frammenti non sarebbero più acqua ma altre sostanze. La molecola dell'acqua è infatti costituita da tre atomi: due atomi di idrogeno (H) e uno di ossigeno (0) legati tra loro.
21 Quando gli atomi si uniscono: La Molecola Così accade per tutte le sostanze. La molecola dell'ammoniaca, cioè la più piccola quantità di materia che ha le caratteristiche di questa sostanza, per esempio, è formata da un atomo di azoto (N) e tre di idrogeno (H) tra loro uniti; la molecola dell'ossigeno, il gas che respiriamo, è formata da due atomi di ossigeno (0) legati tra loro.
22 Le Formule Chimiche Per indicare le molecole si usano segni convenzionali: si scrivono i simboli degli atomi che le costituiscono e in basso a destra di ogni simbolo si indica un numero, che corrisponde al numero di atomi di quell'elemento presenti nella molecola stessa.
23 Le Formule Chimiche
24 Elementi e Composti Osservando gli atomi che compongono una molecola possiamo distinguere tutte le sostanze in due grandi gruppi: Gli Elementi I Composti
25 Elementi Gli elementi sono sostanze la cui molecola è costituita da atomi tutti uguali tra loro. L'ossigeno che respiriamo, per esempio, è un elemento, perché la sua molecola è formata da due atomi di ossigeno. Anche il rame è un elemento, perché è costituito da molecole formate ognuna da un atomo di rame.
26 Composti I composti sono sostanze la cui molecola è costituita da atomi tra loro diversi. Il sale da cucina (o cloruro di sodio), in cui sono presenti atomi di cloro e atomi di sodio, è appunto un composto, e così l acqua e tante altre.
27 Un po di Storia Fin dall'antichità l'uomo si è chiesto quali fossero gli elementi fondamentali che costituivano tutto il mondo naturale.
28 Un po di Storia Che cosa poteva osservare se non il vento che soffiava, l'acqua che dava la vita, la terra che faceva germogliare le piante, il fuoco che bruciava...?
29 A questa concezione oppose le proprie idee il filosofo greco Democrito, il primo che anni fa introdusse il termine di atomo. Un po di Storia
30 Un po di Storia Secondo Democrito tutto è formato da atomi, particelle piccolissime diverse solo per forma e grandezza. Essi si muovono e si combinano dando origine a tutte le cose, anche all'anima dell'uomo!
31 Un po di Storia Ma la teoria atomica della natura trovò molti oppositori, tra cui il grande filosofo Aristotele, che ritornò alla concezione basata sui quattro elementi.
32 Un po di Storia La grandezza dei pensiero di Aristotele fu tale che le sue idee non vennero quasi mai contestate, anche quando erano evidentemente sbagliate. E fu così che di atomi non si parlò più per quasi 2000 anni.
33 Fine
L Atomo e le Molecole
 L Atomo e le Molecole L atomo L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime:
L Atomo e le Molecole L atomo L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime:
L Atomo e le Molecole
 L Atomo e le Molecole L atomo L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime:
L Atomo e le Molecole L atomo L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime:
Le sostanze chimiche
 Le sostanze chimiche Ingredienti base della materia La materia si presenta con diverse forme. Accade perché esistono moltissimi «ingredienti di base» che mescolandosi tra loro danno innumerevoli combinazioni.
Le sostanze chimiche Ingredienti base della materia La materia si presenta con diverse forme. Accade perché esistono moltissimi «ingredienti di base» che mescolandosi tra loro danno innumerevoli combinazioni.
Corso di CHIMICA INORGANICA
 Corso di CHIMICA INORGANICA Lezione Seconda La teoria atomica La massa atomica e il concetto di Isotopi Dentro l atomo, le particelle subatomiche La Tavola Periodica degli Elementi 2 Gli atomi di un certo
Corso di CHIMICA INORGANICA Lezione Seconda La teoria atomica La massa atomica e il concetto di Isotopi Dentro l atomo, le particelle subatomiche La Tavola Periodica degli Elementi 2 Gli atomi di un certo
2 HCl. H 2 + Cl 2 ATOMI E MOLECOLE. Ipotesi di Dalton
 Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Ipotesi di Dalton ATOMI E MOLECOLE 1.! Un elemento è formato da particelle indivisibili chiamate atomi. 2.! Gli atomi di uno specifico elemento hanno proprietà identiche. 3.! Gli atomi si combinano secondo
Struttura dell'atomo a cura di Petr Ushakov
 Struttura dell'atomo a cura di Petr Ushakov Struttura dell'atomo Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: protone, neutrone e elettrone. particelle elementari
Struttura dell'atomo a cura di Petr Ushakov Struttura dell'atomo Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: protone, neutrone e elettrone. particelle elementari
Fenomeno fisico. Le trasformazioni che la materia subisce senza modificare la sua composizione e che sono reversibili si chiamano fenomeni fisici
 Atomi e molecole Fenomeno fisico Le trasformazioni che la materia subisce senza modificare la sua composizione e che sono reversibili si chiamano fenomeni fisici Fenomeno chimico Le trasformazioni che
Atomi e molecole Fenomeno fisico Le trasformazioni che la materia subisce senza modificare la sua composizione e che sono reversibili si chiamano fenomeni fisici Fenomeno chimico Le trasformazioni che
PROF. ALFONSO ANGUILLA ELEMENTI DI CHIMICA: I MATTONI DELLA MATERIA
 http://www.youtube.com/watch?v=q4ki1fa4yj0 PROF. ALFONSO ANGUILLA ELEMENTI DI CHIMICA: I MATTONI DELLA MATERIA 1 Gli elettroni ruotano intorno al nucleo, trattenuti dalla loro carica elettrica negativa,
http://www.youtube.com/watch?v=q4ki1fa4yj0 PROF. ALFONSO ANGUILLA ELEMENTI DI CHIMICA: I MATTONI DELLA MATERIA 1 Gli elettroni ruotano intorno al nucleo, trattenuti dalla loro carica elettrica negativa,
ATOMI E MOLECOLE. Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti).
 1 ATOMI E MOLECOLE Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti). Un elemento (es. il mercurio) è una sostanza che non può
1 ATOMI E MOLECOLE Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti). Un elemento (es. il mercurio) è una sostanza che non può
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni
 CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni composto materia sostanza pura miscela omogenea elemento eterogenea Elementi, Composti e Miscele Miscela eterogenea
CHIMICA: studio della composizione e della struttura della materia e delle sue trasformazioni composto materia sostanza pura miscela omogenea elemento eterogenea Elementi, Composti e Miscele Miscela eterogenea
L Atomo e le Molecole
 L Atomo e le Molecole LA MATERIA TUTTO CIO CHE OCCUPA UNO SPAZIO Ha una MASSA (Kg) Occupa un VOLUME (m 3 ) FORMATA DA MOLECOLE FORMATE DA ATOMI Tutte le sostanze sono fatte di MOLECOLE MOLECOLA: la più
L Atomo e le Molecole LA MATERIA TUTTO CIO CHE OCCUPA UNO SPAZIO Ha una MASSA (Kg) Occupa un VOLUME (m 3 ) FORMATA DA MOLECOLE FORMATE DA ATOMI Tutte le sostanze sono fatte di MOLECOLE MOLECOLA: la più
Chimica. 1) Il simbolo del Carbonio è: A) C B) Ca. C) Ce D) Cu. 2) Secondo il principio della conservazione della materia:
 Chimica 1) Il simbolo del Carbonio è: A) C B) Ca C) Ce D) Cu 2) Secondo il principio della conservazione della materia: A) Durante le reazioni chimiche il numero totale di atomi di ciascun elemento chimico
Chimica 1) Il simbolo del Carbonio è: A) C B) Ca C) Ce D) Cu 2) Secondo il principio della conservazione della materia: A) Durante le reazioni chimiche il numero totale di atomi di ciascun elemento chimico
CHIMICA: studio della struttura e delle trasformazioni della materia
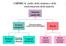 CHIMICA: studio della struttura e delle trasformazioni della materia 1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
CHIMICA: studio della struttura e delle trasformazioni della materia 1 Materia (materali) Sostanze (omogenee) Processo fisico Miscele Elementi (atomi) Reazioni chimiche Composti (molecole) Miscele omogenee
Classe4:chimicaStrutturaAtomica1. Controlla se sai definire i seguenti termini: teoria atomica di Dalton (atomo di Dalton),
 Classe4:chimicaStrutturaAtomica1. Controlla se sai definire i seguenti termini: teoria atomica di Dalton (atomo di Dalton), particelle subatomiche, protone, neutrone, elettronie, nucleo. 2. Decidi se tra
Classe4:chimicaStrutturaAtomica1. Controlla se sai definire i seguenti termini: teoria atomica di Dalton (atomo di Dalton), particelle subatomiche, protone, neutrone, elettronie, nucleo. 2. Decidi se tra
I LEGAMI CHIMICI. Configurazione elettronica stabile: è quella in cui tutti i livelli energetici dell atomo sono pieni di elettroni
 I LEGAMI CIMICI In natura sono pochi gli elementi che presentano atomi allo stato libero. Gli unici elementi che sono costituiti da atomi isolati si chiamano gas nobili o inerti, formano il gruppo VIII
I LEGAMI CIMICI In natura sono pochi gli elementi che presentano atomi allo stato libero. Gli unici elementi che sono costituiti da atomi isolati si chiamano gas nobili o inerti, formano il gruppo VIII
Cos è un trasformazione chimica?
 Chimica Lezione 1 Cos è un trasformazione chimica? Una reazione chimica è una trasformazione della materia che avviene senza variazioni misurabili di massa, in cui uno o più reagenti iniziali modificano
Chimica Lezione 1 Cos è un trasformazione chimica? Una reazione chimica è una trasformazione della materia che avviene senza variazioni misurabili di massa, in cui uno o più reagenti iniziali modificano
Tracce di energia. viaggio dentro l atomo
 Tracce di energia viaggio dentro l atomo Di cosa è fatta la torre Eiffel? di 10.000 tonnellate di ferro ovvero 10.000.000.000 di grammi di ferro miliardi Ogni grammo di ferro, a sua volta, è composto da
Tracce di energia viaggio dentro l atomo Di cosa è fatta la torre Eiffel? di 10.000 tonnellate di ferro ovvero 10.000.000.000 di grammi di ferro miliardi Ogni grammo di ferro, a sua volta, è composto da
LA STRUTTURA DELL ATOMO
 Capitolo 4 LA STRUTTURA DELL ATOMO N.B I concetti proposti sulle slide, in linea di massima seguono l ordine e i contenuti del libro, ma!!!! Ci possono essere delle variazioni Prof. Vincenzo Leo - Chimica
Capitolo 4 LA STRUTTURA DELL ATOMO N.B I concetti proposti sulle slide, in linea di massima seguono l ordine e i contenuti del libro, ma!!!! Ci possono essere delle variazioni Prof. Vincenzo Leo - Chimica
Capitolo 2. Cenni alla Composizione e Struttura dell atomo
 Master in Verifiche di qualità in radiodiagnostica, medicina nucleare e radioterapiar Capitolo 2 Cenni alla Composizione e Struttura dell atomo 24 Atomi, Molecole,, e Ioni L idea di Atomo è antica come
Master in Verifiche di qualità in radiodiagnostica, medicina nucleare e radioterapiar Capitolo 2 Cenni alla Composizione e Struttura dell atomo 24 Atomi, Molecole,, e Ioni L idea di Atomo è antica come
Il modello strutturale dell atomo
 Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Sommario della lezione 4. Proprietà periodiche. Massa atomica e massa molecolare. Concetto di mole. Prime esercitazioni
 Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
Sommario della lezione 4 Proprietà periodiche Massa atomica e massa molecolare Concetto di mole Prime esercitazioni Proprietà periodiche Il raggio atomico è definito come la metà della distanza minima
Classificazione della materia 3 STATI DI AGGREGAZIONE
 Classificazione della materia MATERIA spazio massa Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (Volume e forma propri) LIQUIDO (Volume definito e forma indefinita) GASSOSO
Classificazione della materia MATERIA spazio massa Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (Volume e forma propri) LIQUIDO (Volume definito e forma indefinita) GASSOSO
Chimica. Lezione 1 La materia
 Chimica Lezione 1 La materia Materia Tutte le sostanze che costituiscono l universo Infinita varietà di forme Classificazione a seconda dello stato FISICO (solido, liquido, gassoso) o della COMPOSIZIONE
Chimica Lezione 1 La materia Materia Tutte le sostanze che costituiscono l universo Infinita varietà di forme Classificazione a seconda dello stato FISICO (solido, liquido, gassoso) o della COMPOSIZIONE
Esercizi di. Stechiometria dei composti. mercoledì 9 dicembre 2015
 Esercizi di Stechiometria dei composti mercoledì 9 dicembre 2015 Il cloro ha due isotopi stabili contenenti rispettivamente 18 e 20 neutroni. Utilizzando la tavola periodica degli elementi, scrivere i
Esercizi di Stechiometria dei composti mercoledì 9 dicembre 2015 Il cloro ha due isotopi stabili contenenti rispettivamente 18 e 20 neutroni. Utilizzando la tavola periodica degli elementi, scrivere i
Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe
 1 Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe 21) Quanti neutroni, protoni ed elettroni ha l elemento con numero atomico Z = 23 e numero di massa A = 51? P=23,
1 Verifica di chimica su: Atomo, tavola periodica, legame chimico Nome cognome data classe 21) Quanti neutroni, protoni ed elettroni ha l elemento con numero atomico Z = 23 e numero di massa A = 51? P=23,
Unità Didattica La TAVOLA PERIODICA
 SSIS 2006/2007. VII Ciclo. Classe A059 Scienze Integrate Unità Didattica La TAVOLA PERIODICA a cura di Maddalena Galli Università degli Studi di Ferrara Facciamo ordine tra gli elementi chimici! Fino al
SSIS 2006/2007. VII Ciclo. Classe A059 Scienze Integrate Unità Didattica La TAVOLA PERIODICA a cura di Maddalena Galli Università degli Studi di Ferrara Facciamo ordine tra gli elementi chimici! Fino al
CONFIGURAZIONE ELETTRONICA DEGLI ELEMENTI
 CONFIGURAZIONE ELETTRONICA DEGLI ELEMENTI SOSTANZE: ELEMENTI E COMPOSTI Si definisce sostanza la materia che ha sempre la stessa composizione. Ogni campione di una sostanza ha le stesse propietà chimiche
CONFIGURAZIONE ELETTRONICA DEGLI ELEMENTI SOSTANZE: ELEMENTI E COMPOSTI Si definisce sostanza la materia che ha sempre la stessa composizione. Ogni campione di una sostanza ha le stesse propietà chimiche
Struttura dell atomo atomo particelle sub-atomiche - protoni positiva - neutroni } nucleoni - elettroni negativa elemento
 Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
Struttura dell atomo L atomo è la più piccola parte dell elemento che conserva le proprietà dell elemento Negli atomi ci sono tre diverse particelle sub-atomiche: - protoni (con carica positiva unitaria)
I LEGAMI CHIMICI. I legami chimici si formano quando gli atomi cedono, acquistano oppure mettono in comune
 I LEGAMI CHIMICI I legami chimici si formano quando gli atomi cedono, acquistano oppure mettono in comune alcuni elettroni con altri atomi, per completare il guscio elettronico più esterno. 1. LEGAME IONICO
I LEGAMI CHIMICI I legami chimici si formano quando gli atomi cedono, acquistano oppure mettono in comune alcuni elettroni con altri atomi, per completare il guscio elettronico più esterno. 1. LEGAME IONICO
Capitolo 9 Il sistema periodico
 Capitolo 9 Il sistema periodico 1. La classificazione degli elementi 2. Il sistema periodico di Mendeleev 3. La moderna tavola periodica 4. I simboli di Lewis 5. Le proprietà periodiche 6. Metalli, non
Capitolo 9 Il sistema periodico 1. La classificazione degli elementi 2. Il sistema periodico di Mendeleev 3. La moderna tavola periodica 4. I simboli di Lewis 5. Le proprietà periodiche 6. Metalli, non
La formula chimica di una sostanza nota la sua composizione %
 La formula chimica di una sostanza nota la sua composizione % Si consideri la sostanza costituita dagli elementi A, B e C e sia nota la sua composizione %, che si ottiene sperimentalmente 1. Si divide
La formula chimica di una sostanza nota la sua composizione % Si consideri la sostanza costituita dagli elementi A, B e C e sia nota la sua composizione %, che si ottiene sperimentalmente 1. Si divide
Dispensa di Scienze integrate Docente : Prof.ssa Elena Angotti I.P.S.A.A. Polo di Cutro Corso Serale Classe I A Anno scolastico I Modulo
 Dispensa di Scienze integrate Docente : Prof.ssa Elena Angotti I.P.S.A.A. Polo di Cutro Corso Serale Classe I A Anno scolastico 2013-2014 I Modulo La composizione della materia Possiamo definire materia
Dispensa di Scienze integrate Docente : Prof.ssa Elena Angotti I.P.S.A.A. Polo di Cutro Corso Serale Classe I A Anno scolastico 2013-2014 I Modulo La composizione della materia Possiamo definire materia
Le particelle dell atomo
 La carica elettrica I fenomeni elettrici sono noti fin dall antichità: gli antichi Greci usavano la parola elektron per spiegare il fenomeno dell elettrizzazione dell ambra. I Greci sapevano che strofinando
La carica elettrica I fenomeni elettrici sono noti fin dall antichità: gli antichi Greci usavano la parola elektron per spiegare il fenomeno dell elettrizzazione dell ambra. I Greci sapevano che strofinando
Sono gli atomi indivisibili?
 Sono gli atomi indivisibili? L atomo è la particella più piccola di un elemento che possiede tutte le caratteristiche chimiche dell elemento stesso. Sono noti 112 elementi o specie atomiche diverse (90
Sono gli atomi indivisibili? L atomo è la particella più piccola di un elemento che possiede tutte le caratteristiche chimiche dell elemento stesso. Sono noti 112 elementi o specie atomiche diverse (90
La Vita è una Reazione Chimica
 La Vita è una Reazione Chimica Acqua Oro Zucchero La vita è una reazione chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola
La Vita è una Reazione Chimica Acqua Oro Zucchero La vita è una reazione chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola
ELEMENTI di CHIMICA NUCLEARE. La FISSIONE NUCLEARE
 ELEMENTI di CHIMICA NUCLEARE La FISSIONE NUCLEARE Lo scienziato Otto Hahn nel 938 scoprì che l'uranio 35 9U è fissile. La fissione è una rottura dei nuclei pesanti e può avvenire quando un neutrone lento
ELEMENTI di CHIMICA NUCLEARE La FISSIONE NUCLEARE Lo scienziato Otto Hahn nel 938 scoprì che l'uranio 35 9U è fissile. La fissione è una rottura dei nuclei pesanti e può avvenire quando un neutrone lento
2. La struttura dell atomo
 2. La struttura dell atomo 2.1 Particelle elementari 2.2 I modelli atomici: storia dell atomo 2.3 Numero atomico e numero di massa; 2.4 Isotopi; 2.5 Elementi e tavola periodica 2.1 Particelle elementari
2. La struttura dell atomo 2.1 Particelle elementari 2.2 I modelli atomici: storia dell atomo 2.3 Numero atomico e numero di massa; 2.4 Isotopi; 2.5 Elementi e tavola periodica 2.1 Particelle elementari
Elementi di Chimica. Lezione 03
 Elementi di Chimica Lezione 03 Elementi atomi e molecole Come si è detto tutta la materia esistente in natura è costituita da 92 elementi. Tuttavia ben pochi di questi elementi si trovano in natura sotto
Elementi di Chimica Lezione 03 Elementi atomi e molecole Come si è detto tutta la materia esistente in natura è costituita da 92 elementi. Tuttavia ben pochi di questi elementi si trovano in natura sotto
Le Reazioni Chimiche
 Le Reazioni Chimiche Quando gli atomi si uniscono: La Molecola Gli atomi hanno la capacità di unirsi tra loro formando le MOLECOLE. Le Formule Chimiche Per indicare le molecole si usano le FORMULE CHIMICHE
Le Reazioni Chimiche Quando gli atomi si uniscono: La Molecola Gli atomi hanno la capacità di unirsi tra loro formando le MOLECOLE. Le Formule Chimiche Per indicare le molecole si usano le FORMULE CHIMICHE
Solo all'inizio del XIX secolo J. Dalton propose la teoria atomica moderna
 ATOMI Solo all'inizio del XIX secolo J. Dalton propose la teoria atomica moderna Dalton formulò la sua teoria atomica avvalendosi delle conoscenze chimiche che possedeva: la legge della conservazione della
ATOMI Solo all'inizio del XIX secolo J. Dalton propose la teoria atomica moderna Dalton formulò la sua teoria atomica avvalendosi delle conoscenze chimiche che possedeva: la legge della conservazione della
Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico
 I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
I LEGAMI CHIMICI Legami atomici o forti Legami molecolari o deboli Legame covalente Puro Polare Legame dativo o di coordinazione Legame ionico Legame metallico Legame dipolo-dipolo Legame idrogeno Legame
C.I. CHIMICA-TECNOLOGIA DEI MATERIALI Modulo di Chimica. Lezione del 7 Marzo 2016
 C.I. CHIMICA-TECNOLOGIA DEI MATERIALI Modulo di Chimica Lezione del 7 Marzo 2016 Particelle Elementari Carica Massa SI (C) Atom. SI (kg) Atom. Protone 1.602x10-19 +1 1.673x10-27 1.0073 Neutrone 0 0 1.675x10-27
C.I. CHIMICA-TECNOLOGIA DEI MATERIALI Modulo di Chimica Lezione del 7 Marzo 2016 Particelle Elementari Carica Massa SI (C) Atom. SI (kg) Atom. Protone 1.602x10-19 +1 1.673x10-27 1.0073 Neutrone 0 0 1.675x10-27
Atomi, molecole e ioni
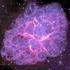 Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Atomi, molecole e ioni anione + - catione Teoria atomica di Dalton 1. Un elemento è composto da particelle minuscole chiamate atomi. 2. In una normale reazione chimica, nessun atomo di nessun elemento
Le reazioni di ossido-riduzione
 Le reazioni di ossido-riduzione Si dicono reazioni di ossidazione e di riduzione (o ossido-riduzione) quelle reazioni che avvengono con cambiamento del numero di elettroni che una specie chimica coinvolge
Le reazioni di ossido-riduzione Si dicono reazioni di ossidazione e di riduzione (o ossido-riduzione) quelle reazioni che avvengono con cambiamento del numero di elettroni che una specie chimica coinvolge
Scienziati in Erba Chimica
 Scienziati in Erba Chimica Acqua Oro Zucchero La Chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola periodica degli elementi
Scienziati in Erba Chimica Acqua Oro Zucchero La Chimica ü ü ü ü ü ü ü ü ü ü Cosa studia la chimica? Classificazione della materia Stati della materia Formule chimiche Atomo Tavola periodica degli elementi
RIASSUNTI DI CHIMICA
 Tecla Spelgatti RIASSUNTI DI CHIMICA per il liceo scientifico 2 - LA TAVOLA PERIODICA Questo testo è distribuito con licenza Common Creative: http://creativecommons.org/licenses/ CC BY-NC-ND Attribuzione
Tecla Spelgatti RIASSUNTI DI CHIMICA per il liceo scientifico 2 - LA TAVOLA PERIODICA Questo testo è distribuito con licenza Common Creative: http://creativecommons.org/licenses/ CC BY-NC-ND Attribuzione
La chimica studia la materia e i cambiamenti ai quali essa va soggetta. La materia è tutto ciò che possiede massa e occupa spazio.
 La chimica studia la materia e i cambiamenti ai quali essa va soggetta. La materia è tutto ciò che possiede massa e occupa spazio. Tutto ciò che potete toccare è materia, e materia sono moltissime cose
La chimica studia la materia e i cambiamenti ai quali essa va soggetta. La materia è tutto ciò che possiede massa e occupa spazio. Tutto ciò che potete toccare è materia, e materia sono moltissime cose
SINTESI C4. La quantità di materia: la mole
 La massa degli atomi Al momento della prima stesura della tavola periodica, Mendeleev non era a oscenza dell esistenza dei protoni, scoperti solo alcuni anni più tardi. Il criterio di classificazione degli
La massa degli atomi Al momento della prima stesura della tavola periodica, Mendeleev non era a oscenza dell esistenza dei protoni, scoperti solo alcuni anni più tardi. Il criterio di classificazione degli
Andrea Nella Michela Mazzucchi Diego Galli Milo Galli
 Andrea Nella Michela Mazzucchi Diego Galli Milo Galli Le rocce formano la parte solida del nostro pianeta. Come vedremo, esse si sono formate attraverso processi diversi, la cui durata può andare da pochi
Andrea Nella Michela Mazzucchi Diego Galli Milo Galli Le rocce formano la parte solida del nostro pianeta. Come vedremo, esse si sono formate attraverso processi diversi, la cui durata può andare da pochi
MASSE ATOMICHE. 1,000 g di idrogeno reagiscono con 7,9367 g di ossigeno massa atomica ossigeno=2 x 7,9367=15,873 g (relativa all'idrogeno)
 MASSE ATOMICHE Sono a volte impropriamente chiamate pesi atomici. All'epoca di Dalton non era possibile pesare i singoli atomi ma solo trovare la massa di un atomo relativa a quella di un altro acqua di
MASSE ATOMICHE Sono a volte impropriamente chiamate pesi atomici. All'epoca di Dalton non era possibile pesare i singoli atomi ma solo trovare la massa di un atomo relativa a quella di un altro acqua di
Elementi: specie chimiche che resistono bene ad ogni tentativo di decomposizione. Composti: specie chimiche definite formate da due o più elementi
 Elementi: specie chimiche che resistono bene ad ogni tentativo di decomposizione Composti: specie chimiche definite formate da due o più elementi Elemento Simbolo nomi con radici latine nomi derivati dalla
Elementi: specie chimiche che resistono bene ad ogni tentativo di decomposizione Composti: specie chimiche definite formate da due o più elementi Elemento Simbolo nomi con radici latine nomi derivati dalla
Capitolo 3. LE TRASFORMAZIONI CHIMICHE DELLA MATERIA La teoria particellare un po' più da vicino
 Capitolo 3 LE TRASFORMAZIONI CHIMICHE DELLA MATERIA La teoria particellare un po' più da vicino N.B I concetti proposti sulle slide, in linea di massima seguono l ordine e i contenuti del libro, ma!!!!
Capitolo 3 LE TRASFORMAZIONI CHIMICHE DELLA MATERIA La teoria particellare un po' più da vicino N.B I concetti proposti sulle slide, in linea di massima seguono l ordine e i contenuti del libro, ma!!!!
 ELETTRONEGATIVITA CAPACITA DI UN ATOMO DI ATTIRARE UNA COPPIA DI ELETTRONI DI LEGAME DETERMINANDO COSI IL TIPO DI LEGAME CHE SI VIENE A FORMARE. DERIVA DA ALTRE DUE GRANDEZZE I. Energia di ionizzazione:
ELETTRONEGATIVITA CAPACITA DI UN ATOMO DI ATTIRARE UNA COPPIA DI ELETTRONI DI LEGAME DETERMINANDO COSI IL TIPO DI LEGAME CHE SI VIENE A FORMARE. DERIVA DA ALTRE DUE GRANDEZZE I. Energia di ionizzazione:
Lezione 2. Leggi ponderali
 Lezione 2 Leggi ponderali I miscugli eterogenei presentano i componenti distinguibili in due o più fasi, in rapporti di massa altamente variabili e che mantengono le caratteristiche originarie. I miscugli
Lezione 2 Leggi ponderali I miscugli eterogenei presentano i componenti distinguibili in due o più fasi, in rapporti di massa altamente variabili e che mantengono le caratteristiche originarie. I miscugli
L2 - Completa la seguente frase: "L'auto sta al telaio come il corpo sta..."
 Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come continua questa serie di numeri? 3-4 - 6-9 - 13-18 -... a) 21 b) 22 c) 23 d) 24 L2 - Completa
Simulazione test di ingresso Ingegneria Industriale Viterbo Quesiti di Logica, Chimica e Fisica Logica L1 - Come continua questa serie di numeri? 3-4 - 6-9 - 13-18 -... a) 21 b) 22 c) 23 d) 24 L2 - Completa
Semimetalli. Sono rappresentati da B, Si, As, Te, At, Ge, Sb e Po. Nell'immagine At è erroneamente non indicato.
 Semimetalli Sono rappresentati da B, Si, As, Te, At, Ge, Sb e Po. Nell'immagine At è erroneamente non indicato. Elementi chimici, quali antimonio, arsenico, bismuto, che presentano proprietà in parte metalliche
Semimetalli Sono rappresentati da B, Si, As, Te, At, Ge, Sb e Po. Nell'immagine At è erroneamente non indicato. Elementi chimici, quali antimonio, arsenico, bismuto, che presentano proprietà in parte metalliche
MOLECOLE. 2 - i legami chimici. Prof. Vittoria Patti
 MOLECOLE 2 - i legami chimici Prof. Vittoria Patti Gli stati di aggregazione della materia STATO SOLIDO molecole ravvicinate, struttura ordinata, volume proprio, forma propria STATO LIQUIDO molecole
MOLECOLE 2 - i legami chimici Prof. Vittoria Patti Gli stati di aggregazione della materia STATO SOLIDO molecole ravvicinate, struttura ordinata, volume proprio, forma propria STATO LIQUIDO molecole
RIASSUNTI DI CHIMICA
 Tecla Spelgatti RIASSUNTI DI CHIMICA per il liceo scientifico 1 - LA STRUTTURA DELLA MATERIA Questo testo è distribuito con licenza Common Creative: http://creativecommons.org/licenses/ CC BY-NC-ND Attribuzione
Tecla Spelgatti RIASSUNTI DI CHIMICA per il liceo scientifico 1 - LA STRUTTURA DELLA MATERIA Questo testo è distribuito con licenza Common Creative: http://creativecommons.org/licenses/ CC BY-NC-ND Attribuzione
TAVOLA PERIODICA Gli elementi sono sostanza pure dalle quali non è possibile ottenere, mediante gli ordinari mezzi chimici, sostanze più semplici.
 TAVOLA PERIODICA Gli elementi sono sostanza pure dalle quali non è possibile ottenere, mediante gli ordinari mezzi chimici, sostanze più semplici. Se per esempio, facciamo l'analisi di un oggetto di rame,
TAVOLA PERIODICA Gli elementi sono sostanza pure dalle quali non è possibile ottenere, mediante gli ordinari mezzi chimici, sostanze più semplici. Se per esempio, facciamo l'analisi di un oggetto di rame,
L atomo. Il neutrone ha una massa 1839 volte superiore a quella dell elettrone. 3. Le particelle fondamentali dell atomo
 L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
L atomo 3. Le particelle fondamentali dell atomo Gli atomi sono formati da tre particelle fondamentali: l elettrone con carica negativa; il protone con carica positiva; il neutrone privo di carica. Il
PROVA 1. Dati i composti con formula KBr e HClO 2 :
 PROVA 1 Dati i composti con formula KBr e HClO 2 : 1) Individuare a quale categoria di composti appartengono (ossidi,anidridi,idrossidi,acidi,sali) 2) Determinare le valenze o i numeri di ossidazione di
PROVA 1 Dati i composti con formula KBr e HClO 2 : 1) Individuare a quale categoria di composti appartengono (ossidi,anidridi,idrossidi,acidi,sali) 2) Determinare le valenze o i numeri di ossidazione di
Chimica. La Chimica è la scienza che cerca di comprendere il comportamento della materia studiando il comportamento di atomi e molecole
 Chimica La Chimica è la scienza che descrive la materia, le sue proprietà e le trasformazioni che essa subisce, insieme alle variazioni energetiche che accompagnano questi processi La Chimica è la scienza
Chimica La Chimica è la scienza che descrive la materia, le sue proprietà e le trasformazioni che essa subisce, insieme alle variazioni energetiche che accompagnano questi processi La Chimica è la scienza
L INFINITAMENTE PICCOLO
 L INFINITAMENTE PICCOLO http://www.youtube.com/watch?v=cumf9nu-nim (VIDEO POTENZE DI DIECI) Cos'è una potenza di dieci? E' un modo per esprimere brevemente numeri molto grandi o molto piccoli. 10 6 si
L INFINITAMENTE PICCOLO http://www.youtube.com/watch?v=cumf9nu-nim (VIDEO POTENZE DI DIECI) Cos'è una potenza di dieci? E' un modo per esprimere brevemente numeri molto grandi o molto piccoli. 10 6 si
1) Calcola la massa molecolare relativa e la massa molare delle seguenti sostanze: NH ( x3) = u.m.a 17.
 1) Calcola la massa molecolare relativa e la massa molare delle seguenti sostanze: NH3 14.0067+(1.00797x3) = 17.03 u.m.a 17.03 gr mol -1 2) Qual è la massa in grammi di 1,00 mol di atomi di fosforo (P)
1) Calcola la massa molecolare relativa e la massa molare delle seguenti sostanze: NH3 14.0067+(1.00797x3) = 17.03 u.m.a 17.03 gr mol -1 2) Qual è la massa in grammi di 1,00 mol di atomi di fosforo (P)
Struttura atomica della materia
 Struttura atomica della materia 1 FASE fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente e fisicamente omogenea delimitata da superfici di separazione ben definite 2 Classificazione della materia
Struttura atomica della materia 1 FASE fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente e fisicamente omogenea delimitata da superfici di separazione ben definite 2 Classificazione della materia
Massa assoluta e relativa e mole
 Massa assoluta e relativa e mole Massa atomica assoluta.. Massa di un atomo di un dato elemento. In questo caso si parla spesso di peso atomico assoluto, che viene espresso in grammi: l'ordine dei valori
Massa assoluta e relativa e mole Massa atomica assoluta.. Massa di un atomo di un dato elemento. In questo caso si parla spesso di peso atomico assoluto, che viene espresso in grammi: l'ordine dei valori
Chimica Generale ed Inorganica
 Chimica Generale ed Inorganica Chimica Generale prof. Dario Duca H 2 O, CO, CO 2 MgO legge di conservazione della massa Lavoisier legge della composizione costante Proust teoria atomica di Dalton i) gli
Chimica Generale ed Inorganica Chimica Generale prof. Dario Duca H 2 O, CO, CO 2 MgO legge di conservazione della massa Lavoisier legge della composizione costante Proust teoria atomica di Dalton i) gli
Le unità fondamentali SI. Corrente elettrica
 ESERITAZIONE 1 1 Le unità fondamentali SI Grandezza fisica Massa Lunghezza Tempo Temperatura orrente elettrica Quantità di sostanza Intensità luminosa Nome dell unità chilogrammo metro secondo Kelvin ampere
ESERITAZIONE 1 1 Le unità fondamentali SI Grandezza fisica Massa Lunghezza Tempo Temperatura orrente elettrica Quantità di sostanza Intensità luminosa Nome dell unità chilogrammo metro secondo Kelvin ampere
Com è fatto l atomo ATOMO. UNA VOLTA si pensava che l atomo fosse indivisibile. OGGI si pensa che l atomo è costituito da tre particelle
 STRUTTURA ATOMO Com è fatto l atomo ATOMO UNA VOLTA si pensava che l atomo fosse indivisibile OGGI si pensa che l atomo è costituito da tre particelle PROTONI particelle con carica elettrica positiva e
STRUTTURA ATOMO Com è fatto l atomo ATOMO UNA VOLTA si pensava che l atomo fosse indivisibile OGGI si pensa che l atomo è costituito da tre particelle PROTONI particelle con carica elettrica positiva e
2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una
 Capitolo 2 Risposte alle Domande ed esercizi inclusi nel Capitolo 2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una regione di spazio
Capitolo 2 Risposte alle Domande ed esercizi inclusi nel Capitolo 2.1 (p. 37) Bohr descrisse un orbitale atomico come una traiettoria circolare seguita dall elettrone. Un orbitale è una regione di spazio
Zolfo (Z = 16) Conf. Elettronica 1s 2 2s 2 2p 6 3s 2 3p 4 Conf. Elettronica esterna 3s 2 3p 4
 TAVOLA PERIODICA DEGLI ELEMENTI Gli elementi sono ordinati nella tavola periodica secondo numero atomico crescente ed in base alle loro proprietà chimico-fisiche che seguono un andamento periodico. Gli
TAVOLA PERIODICA DEGLI ELEMENTI Gli elementi sono ordinati nella tavola periodica secondo numero atomico crescente ed in base alle loro proprietà chimico-fisiche che seguono un andamento periodico. Gli
reazioni Sostanze Reazioni di sintesi Reazioni di decomposizione
 Si consumano nelle reazioni Si formano nelle reagenti Si trasformano con prodotti Sostanze Sostanze semplici Sostanze composte Non ottenibili con Non decomponibili con Reazioni di sintesi Reazioni di decomposizione
Si consumano nelle reazioni Si formano nelle reagenti Si trasformano con prodotti Sostanze Sostanze semplici Sostanze composte Non ottenibili con Non decomponibili con Reazioni di sintesi Reazioni di decomposizione
Configurazione elettronica e collegamento alla tavola periodica
 Configurazione elettronica e collegamento alla tavola periodica Modelli atomici a confronto Un elettrone che si trova in un certo livello possiede l energia associata a quel livello, in particolare al
Configurazione elettronica e collegamento alla tavola periodica Modelli atomici a confronto Un elettrone che si trova in un certo livello possiede l energia associata a quel livello, in particolare al
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 7 Le particelle dell atomo 1. La natura elettrica della materia 2. Le particelle fondamentali
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 7 Le particelle dell atomo 1. La natura elettrica della materia 2. Le particelle fondamentali
Corso di CHIMICA LEZIONE 3
 Corso di CHIMICA LEZIONE 3 1 2 3 4 5 6 7 H Li Na K Fr Be Ma g Ca Ba TAVOLA PERIODICA He I II s 1 s 2 III IV V VI VII VIII p 1 p 2 p 3 p 4 p 5 p 6 blocco s La Ac 6 7 d 1 d 2 d 3 d 4 d 5 d 6 d 7 d 8 d 9
Corso di CHIMICA LEZIONE 3 1 2 3 4 5 6 7 H Li Na K Fr Be Ma g Ca Ba TAVOLA PERIODICA He I II s 1 s 2 III IV V VI VII VIII p 1 p 2 p 3 p 4 p 5 p 6 blocco s La Ac 6 7 d 1 d 2 d 3 d 4 d 5 d 6 d 7 d 8 d 9
SISTEMA INTERNAZIONALE IL SISTEMA INTERNAZIONALE CLASSIFICA LE GRANDEZZE E LE RISPETTIVE UNITA' DI MISURA LE GRANDEZZE VENGONO SUDDIVISE IN:
 SISTEMA INTERNAZIONALE IL SISTEMA INTERNAZIONALE CLASSIFICA LE GRANDEZZE E LE RISPETTIVE UNITA' DI MISURA LE GRANDEZZE VENGONO SUDDIVISE IN: GRANDEZZE FONDAMENTALI GRANDEZZE DERIVATE Grandezza Unità di
SISTEMA INTERNAZIONALE IL SISTEMA INTERNAZIONALE CLASSIFICA LE GRANDEZZE E LE RISPETTIVE UNITA' DI MISURA LE GRANDEZZE VENGONO SUDDIVISE IN: GRANDEZZE FONDAMENTALI GRANDEZZE DERIVATE Grandezza Unità di
Corso di Studi in Scienze Naturali Corso di Chimica Generale e Inorganica Dott.ssa Maria Cristina Paganini Prof. Elio Giamello
 Corso di Studi in Scienze Naturali Corso di Chimica Generale e Inorganica Dott.ssa Maria Cristina Paganini Prof. Elio Giamello Avvertenza: Le immagini seguenti, proiettate durante le lezioni sono tratte
Corso di Studi in Scienze Naturali Corso di Chimica Generale e Inorganica Dott.ssa Maria Cristina Paganini Prof. Elio Giamello Avvertenza: Le immagini seguenti, proiettate durante le lezioni sono tratte
SEZIONE D - LE BIOMOLECOLE di Mauro Festa Larel, Patrizia Panunzio, Elisabetta Rusconi, Giovanni Valsecchi
 SEZIONE D - LE BIOMOLECOLE di Mauro Festa Larel, Patrizia Panunzio, Elisabetta Rusconi, Giovanni Valsecchi SEZIONE D - LE BIOMOLECOLE D.1 - PREMESSA: UN PO DI CHIMICA Tutta la materia è formata da atomi
SEZIONE D - LE BIOMOLECOLE di Mauro Festa Larel, Patrizia Panunzio, Elisabetta Rusconi, Giovanni Valsecchi SEZIONE D - LE BIOMOLECOLE D.1 - PREMESSA: UN PO DI CHIMICA Tutta la materia è formata da atomi
Atomi, Molecole e Ioni. Capitolo 2
 Atomi, Molecole e Ioni Capitolo 2 La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti gli atomi di un dato elemento sono identici
Atomi, Molecole e Ioni Capitolo 2 La Teoria Atomica di Dalton (1808) 1. Gli Elementi sono composti da particelle estremamente piccole, denominate atomi. 2. Tutti gli atomi di un dato elemento sono identici
Struttura atomica della materia
 Struttura atomica della materia 1 FASE fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente e fisicamente omogenea delimitata da superfici di separazione ben definite 2 Classificazione della materia
Struttura atomica della materia 1 FASE fase 3 fase 1 fase 2 FASE: porzione di materia chimicamente e fisicamente omogenea delimitata da superfici di separazione ben definite 2 Classificazione della materia
materia atomi miscugli omogenei e eterogenei sostanze elementari composti
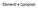 Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
Chimica. La Chimica è la scienza che cerca di comprendere il comportamento della materia studiando il comportamento di atomi e molecole
 Chimica La Chimica è la scienza che descrive la materia, le sue proprietà e le trasformazioni che essa subisce, insieme alle variazioni energetiche che accompagnano questi processi La Chimica è la scienza
Chimica La Chimica è la scienza che descrive la materia, le sue proprietà e le trasformazioni che essa subisce, insieme alle variazioni energetiche che accompagnano questi processi La Chimica è la scienza
Orbitali nei primi tre livelli
 Orbitali nei primi tre livelli La tavola periodica degli elementi Numeri quantici e tavola Configurazioni elettroniche degli atomi Elenco degli orbitali occupati in un atomo nel suo stato fondamentale
Orbitali nei primi tre livelli La tavola periodica degli elementi Numeri quantici e tavola Configurazioni elettroniche degli atomi Elenco degli orbitali occupati in un atomo nel suo stato fondamentale
La chimica della vita. Sylvia S. Mader Immagini e concetti della biologia Zanichelli editore, 2012
 La chimica della vita 1 Tutta la materia è composta da elementi chimici È materia qualsiasi cosa, vivente e non vivente, che occupi dello spazio e che abbia una massa. La materia è composta da elementi
La chimica della vita 1 Tutta la materia è composta da elementi chimici È materia qualsiasi cosa, vivente e non vivente, che occupi dello spazio e che abbia una massa. La materia è composta da elementi
Teoria Atomica di Dalton
 Teoria Atomica di Dalton Il concetto moderno della materia si origina nel 1806 con la teoria atomica di John Dalton: Ogni elementoè composto di atomi. Gli atomi di un dato elemento sono uguali. Gli atomi
Teoria Atomica di Dalton Il concetto moderno della materia si origina nel 1806 con la teoria atomica di John Dalton: Ogni elementoè composto di atomi. Gli atomi di un dato elemento sono uguali. Gli atomi
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro
 Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
Struttura dell atomo e Sistema Periodico degli elementi unità 1, 2 e 3, modulo C del libro Gli atomi di tutti gli elementi sono formati da tre tipi di particelle elementari: elettrone, protone e neutrone.
Come possiamo conoscere il numero di atomi o molecole presenti in una definita quantità di sostanza?
 Come possiamo conoscere il numero di atomi o molecole presenti in una definita quantità di sostanza? Fisicamente è impossibile contare gli atomi contenuti in una data quantita di sostanza. E impossibile
Come possiamo conoscere il numero di atomi o molecole presenti in una definita quantità di sostanza? Fisicamente è impossibile contare gli atomi contenuti in una data quantita di sostanza. E impossibile
struttura atomica della materia La chimica
 Struttura atomica della materia 1 La chimica La chimica è la scienza che si occupa dello studio della composizione e delle proprietà delle varie forme della materia 2 bbvbsxbfxbfx 1 Classificazione della
Struttura atomica della materia 1 La chimica La chimica è la scienza che si occupa dello studio della composizione e delle proprietà delle varie forme della materia 2 bbvbsxbfxbfx 1 Classificazione della
risposte agli esercizi del libro
 risposte agli esercizi del libro 1 SOLUZIONI ESERCIZI FINE CPITOLO 1 B D C 4 C 5 B 6 C 7 D 8 9 D 11 C 1 B 1 B 14 B 15 C 16 C 18 B 19 a) fisica; b) materiale; c) macroscopica; d) fusione; e) hanno-non occupano
risposte agli esercizi del libro 1 SOLUZIONI ESERCIZI FINE CPITOLO 1 B D C 4 C 5 B 6 C 7 D 8 9 D 11 C 1 B 1 B 14 B 15 C 16 C 18 B 19 a) fisica; b) materiale; c) macroscopica; d) fusione; e) hanno-non occupano
alle FaColtà UNiVERSitaRiE
 tst i HiMia PR l asso all Faoltà UNiVRSitaRi 1. indicare quale dei seguenti elementi NoN è di transizione: a Fe zn as u r (Medicina e hirurgia 2005) 2. indicare la configurazione elettronica possibile
tst i HiMia PR l asso all Faoltà UNiVRSitaRi 1. indicare quale dei seguenti elementi NoN è di transizione: a Fe zn as u r (Medicina e hirurgia 2005) 2. indicare la configurazione elettronica possibile
A a B b C c. a : b : c
 Consideriamo un composto di formula generica: A a B b C c La formula di un composto (ionico o molecolare) fornisce in maniera immediata e diretta la sua composizione atomica: Una molecola di formula A
Consideriamo un composto di formula generica: A a B b C c La formula di un composto (ionico o molecolare) fornisce in maniera immediata e diretta la sua composizione atomica: Una molecola di formula A
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Le leggi fondamentali della chimica
 Dall alchimia alla chimica moderna Le leggi fondamentali della chimica Questo è il segreto dell'alchimia: esiste un modo di manipolare la materia e l'energia in modo da produrre ciò che gli scienziati
Dall alchimia alla chimica moderna Le leggi fondamentali della chimica Questo è il segreto dell'alchimia: esiste un modo di manipolare la materia e l'energia in modo da produrre ciò che gli scienziati
Elementi sistemati nella TAVOLA PERIODICA DEGLI ELEMENTI in base al numero atomico crescente O, H, N, C (+ del 96% della materia vivente)
 OVERVIEW Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi
OVERVIEW Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi
Gli elementi presenti in natura sono 120, di cui:
 Gli elementi presenti in natura sono 120, di cui: 92 naturali 18 prodotti artificialmente 4 incerti poiché non ne è stata provata l'esistenza a causa della loro brevissima vita 3 ipotetici 3 scoperti nel
Gli elementi presenti in natura sono 120, di cui: 92 naturali 18 prodotti artificialmente 4 incerti poiché non ne è stata provata l'esistenza a causa della loro brevissima vita 3 ipotetici 3 scoperti nel
I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO
 I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO REGOLA DELL OTTETTO: Tutti gli atomi si legano, cedono, acquistano o condividono elettroni per raggiungere un livello esterno pieno di otto (o due) elettroni.
I LEGAMI CHIMICI E LA REGOLA DELL OTTETTO REGOLA DELL OTTETTO: Tutti gli atomi si legano, cedono, acquistano o condividono elettroni per raggiungere un livello esterno pieno di otto (o due) elettroni.
1) Bilanciare la seguente reazione redox con il metodo ionico-elettronico Ag (s) + H + (aq) + NO 3
 A ) Soluzioni Esercizi I esonero del 29/11/2005 1) Bilanciare la seguente reazione redox con il metodo ionicoelettronico Ag (s) + + (aq) + N 3 (aq) Ag + (aq) + N 2 (g) + 2 (l) Calcolare quanti grammi di
A ) Soluzioni Esercizi I esonero del 29/11/2005 1) Bilanciare la seguente reazione redox con il metodo ionicoelettronico Ag (s) + + (aq) + N 3 (aq) Ag + (aq) + N 2 (g) + 2 (l) Calcolare quanti grammi di
Le Reazioni Chimiche
 I Legami chimici Quando gli atomi cedono, acquistano o mettono in comune degli elettroni formano un legame chimico. I Legami chimici Gli atomi cercano sempre di completare il loro guscio esterno cedendo,
I Legami chimici Quando gli atomi cedono, acquistano o mettono in comune degli elettroni formano un legame chimico. I Legami chimici Gli atomi cercano sempre di completare il loro guscio esterno cedendo,
La quantità chimica LA MOLE
 La quantità chimica LA MOLE 1 QUANTO PESA UN ATOMO? Se lo misurassimo in grammi, l atomo di H, il più piccolo, avrebbe una massa di 1,6 x10-24 g. Per convenzione, si assegna un valore arbitrario (12) alla
La quantità chimica LA MOLE 1 QUANTO PESA UN ATOMO? Se lo misurassimo in grammi, l atomo di H, il più piccolo, avrebbe una massa di 1,6 x10-24 g. Per convenzione, si assegna un valore arbitrario (12) alla
CONFIGURAZIONE ELETTRONICA. In generale la configurazione elettronica indica come sono posizionati gli elettroni intorno al nucleo di un atomo.
 CONFIGURAZIONE ELETTRONICA In generale la configurazione elettronica indica come sono posizionati gli elettroni intorno al nucleo di un atomo. ORBITA : Zona intorno al nucleo di diversa energia dove ruotano
CONFIGURAZIONE ELETTRONICA In generale la configurazione elettronica indica come sono posizionati gli elettroni intorno al nucleo di un atomo. ORBITA : Zona intorno al nucleo di diversa energia dove ruotano
