5. FLUIDI TERMODINAMICI
|
|
|
- Gianpaolo Stefani
- 8 anni fa
- Visualizzazioni
Transcript
1 5. FLUIDI TERMODINAMICI 5.1 Introduzione Un sistema termodinamico è in genere rappresentato da una quantità di una determinata materia della quale siano definibili le proprietà termodinamiche. Se tali proprietà sono uniformi nello spazio la quantità di materia in questione può essere definita fluido termodinamico. Un fluido termodinamico può essere costituito da una o più sostanze presenti in uno o più stati di aggregazione della materia. Un fluido termodinamico costituito da un unica sostanza caratterizzata da una composizione chimica uniforme in tutta la sua massa e invariabile nel tempo si dice sostanza pura. Un fluido termodinamico costituito da più sostanze pure perfettamente miscibili tra loro è chiamato miscela. Come si è detto un fluido termodinamico si può presentare in uno o più stati di aggregazione della materia che vengono denominati fasi. Definiremo fase di una sostanza pura una sua regione omogenea dal punto di vista fisico. In conseguenza della variazione dello stato termodinamico, ogni sostanza può sempre passare da una fase all altra. Questo passaggio prende il nome di transizione di fase o anche cambiamento di stato di aggregazione: quest ultima denominazione è alla base dell inesatta denominazione di cambiamento di stato con la quale talvolta il fenomeno è chiamato. Un cambiamento di stato è invece l effetto di una trasformazione termodinamica che può o no dar luogo anche a un cambiamento di fase. Quando il fluido termodinamico è una miscela, ogni sostanza che la compone può comparire in una o più fasi: la miscela resta allora un fluido termodinamico solo se la composizione chimica resta uniforme e invariabile in tutta la sua massa quale che sia la fase considerata. 5.2 Regola delle fasi o di GIBBS Le proprietà caratteristiche di un fluido termodinamico che si presenta in una o più fasi sono descritte dalla cosiddetta equazione di stato, questa è una funzione matematica che lega tra loro le sue grandezze di stato togliendo ad alcune di esse la loro indipendenza. Quando tale funzione è troppo complessa essa viene rappresentata graficamente e, questa rappresentazione, dà luogo a un diagramma di stato. L equazione di stato di un generico sistema si può scrivere nella forma: f ( p,v,t,...) = 0 (5.1) espressione che mostra simbolicamente come, per il sistema considerato, tutte le grandezze di stato sono legate attraverso la funzione f che è detta equazione di stato. L equazione può coinvolgere un numero qualsiasi di grandezze di stato tuttavia il valore di alcune di esse non è indipendente: il numero delle grandezze di stato che possono assumere valori indipendenti è determinato dalle caratteristiche del sistema ovvero dal numero C delle sue componenti chimiche e dal numero F delle fasi in cui esse sono presenti. 67
2 Si dice varianza V di un sistema in equilibrio termodinamico il numero dei gradi di libertà del sistema ovvero il numero delle grandezze di stato intensive che possono assumere valori indipendenti senza che cambi il numero della fasi presenti. E evidente che la frase...che possono assumere valori indipendenti corrisponde a dire...che possono essere imposti liberamente ovvero i cui valori possano essere variati senza che cambi il numero delle fasi presenti. La varianza di un sistema chimicamente e fisicamente eterogeneo, formato da un numero C di componenti chimicamente distinti, in un certo numero F di fasi fisicamente distinte, può venir valutata attraverso la regola delle fasi di Gibbs che determina il numero V di grandezze di stato intensive indipendenti che definiscono univocamente lo stato fisico di un sistema in equilibrio termodinamico. La regola delle fasi di Gibbs si esprime nella relazione: V = C F + 2 (5.2) ovvero lo stato del sistema è individuato quando si conosce un numero di coordinate intensive pari a quello dei componenti meno quello delle fasi più due. Applicando tale regola si osserva che: Per un sistema termodinamico costituito da due componenti presenti in una sola fase si ottiene: V = = 3. Per esempio, sono sistemi di questo tipo: l aria atmosferica rappresentata come una miscela tra aria secca e vapor d acqua; una massa di acqua e alcool in fase liquida; un volume di idrogeno e ossigeno entrambi in fase gassosa, Per un sistema termodinamico costituito da un solo componente presente in una sola fase (un sistema chimicamente e fisicamente omogeneo: C=1, F=1) si ottiene: V = = 2; sono necessarie cioè solo due coordinate intensive per definirne lo stato. Ciò significa che se si assumono tre coordinate caratterizzanti il sistema, come p, v e T, esiste, come si è visto a proposito dei diagrammi di processo nel cap. 3, una equazione di stato del tipo f(p,v,t)=0 la cui forma dipende dalle proprietà della sostanza considerata. Il sistema quindi è a 2 variabili indipendenti ed ogni sua coordinata intensiva può essere espressa in funzione delle altre due. Per esempio, sono sistemi di questo tipo: una massa d acqua liquida, un certo volume di gas, una massa di metallo. Per un sistema termodinamico costituito da un solo componente presente in due fasi distinte si ottiene: V = = 1. Per esempio, sono sistemi di questo tipo: una massa di acqua e ghiaccio; un certo volume di gas parzialmente condensato; una massa di metallo parzialmente fusa. E interessante notare che per un sistema termodinamico costituito da un solo componente presente in tutte tre le fasi (solida, liquida, gassosa) si ottiene: V = = 0. Ciò significa che il sistema non ha in questo caso alcun grado di libertà, non appena viene variato il valore di una sua grandezza di stato sparisce una delle tre fasi presenti. questo stato si definisce punto triplo della sostanza. La regola delle fasi fu ottenuta nel 1875 da Josiah Willard Gibbs, docente di Fisica e Matematica alla Yale University. La relazione fu il risultato di una teoria generale dell equilibrio dei sistemi eterogenei, sviluppata da Gibbs tra il 1875 ed il
3 5.3 Cambiamenti di fase Gli stati di aggregazione o fasi in cui la materia si presenta sono tre: solido, liquido, aeriforme. All interno di ognuna di queste tre fasi sono possibili, come si vedrà, delle distinzioni che possono dar luogo a differenti denominazioni: valga per tutte l esempio della fase aeriforme all interno della quale una sostanza si suole denominare più vapore o gas a seconda che la fase aeriforme sia o no in stati termodinamici prossimi a quelli nei quali può avvenire il cambiamento di fase. I passaggi tra le diverse fasi prendono i nomi seguenti: Passaggio da solido a liquido fusione Passaggio da liquido a solido solidificazione Passaggio da solido a aeriforme sublimazione Passaggio da aeriforme a solido condensazione (brinamento) Passaggio da aeriforme e a liquido liquefazione o condensazione Passaggio da liquido a aeriforme evaporazione Nella pratica, tuttavia, entrambi i passaggi di fase del vapore (da vapore a solido e anche da vapore a liquido) si indicano con il nome di condensazione. fusione SOLIDO solidificazione LIQUIDO sublimazione liquefazione o condensazione condensazione evaporazione AERIFORME Figura 5.1 Nomenclatura dei passaggi di fase Sia dato un sistema costituito da due fasi della medesima sostanza compresenti in equilibrio: la condizione di equilibrio viene detta condizione di saturazione ed entrambe le fasi vengono dette sature. Per esempio, un sistema in cui siano compresenti liquido e vapore indica che esso è in condizioni di saturazione cioè è costituito da liquido saturo e vapore saturo. In tale situazione, un sistema bifase, monocomponente ha, come sopra ricordato, variabilità pari a 1: ciò equivale ad ammettere che è possibile la variazione di una sola grandezza termodinamica intensiva se si vuole mantenere il sistema in tali condizioni (senza che sparisca una delle fasi presenti). 69
4 Nella realtà, tuttavia, i sistemi non sono sempre in equilibrio. Si consideri ad esempio un sistema isolato costituito da una porzione di spazio di volume V nel quale, dopo che è stato fatto il vuoto venga introdotta una massa m di sostanza in fase liquida il cui volume specifico è v. Se V > m v immediatamente ha inizio il fenomeno di evaporazione e lo spazio V-m v, inizialmente vuoto, si riempie di vapore. Il fenomeno perdura, facendo passare dalla fase liquida a quella di vapore una quantità sempre maggiore della massa m, fino a raggiungere la condizione di saturazione: la fase liquida della sostanza si presenta a questo punto in condizioni di liquido saturo, quella aeriforme in condizioni di vapore saturo e il sistema, finalmente in equilibrio, permane in condizioni immutate nel tempo. In questa situazione si può assumere che il numero di molecole che ad ogni istante passano dalla fase liquida a quella aeriforme è pari al numero di molecole che compiono il passaggio inverso. Se si misura la pressione all interno della fase aeriforme si trova un determinato valore che rappresenta la pressione di saturazione del vapore per lo stato termodinamico al quale si trova il sistema: questo stesso valore è anche detto tensione di vapore del liquido. La pressione di saturazione è quindi calcolabile come: Un'espressione utilizzata per il calcolo può assumere la forma: con A, B costanti che dipendono unicamente dal fluido. p sat = f (T) (5.3) ln (p sat ) = A - B/ T (5.4) È questa la differenza sostanziale del comportamento dei vapori saturi rispetto a quello dei gas, per i quali, come si vedrà, la p non è funzione solo della temperatura ma anche del volume secondo l'equazione di stato. Se, mantenendo costanti tutte le altre grandezze di stato, si aumenta il volume V le condizioni di equilibrio si raggiungono sempre alla medesima pressione di saturazione ma aumenta la massa m v della sostanza che cambia di fase. Può accadere che il volume V del sistema sia così grande che il liquido continui a evaporare senza mai raggiungere la pressione di saturazione del vapore: in tal caso tutto il liquido passerà in fase aeriforme e le condizioni raggiunte alla fine del transitorio saranno di vapore non saturo o di gas a seconda di quanto grande è il volume V. Si noti che, mantenendo V costante ma cambiando la temperatura del sistema, la pressione di saturazione (o tensione di vapore del liquido) varia secondo una funzione crescente della temperatura in genere di tipo esponenziale; e varia anche in questo caso la massa m v della sostanza che cambia di fase. Si indica con il nome titolo del vapore x il rapporto m v /m dove m è la massa della sostanza. Si può scrivere anche: x v = (5.5) m m + v m l dove m l è la massa della sostanza in fase liquida. 70
5 Il passaggio da una fase all altra non avviene in modo gratuito ma richiede dell energia in quote diverse per ogni sostanza. L energia necessaria a provocare il passaggio di fase dell unità di massa di una determinata sostanza, in condizioni iniziali e finali di saturazione, prende il nome, secondo il passaggio considerato, di: calore di fusione (solidificazione), calore di sublimazione (condensazione) o calore di evaporazione (condensazione) di quella sostanza e la sua unità di misura è [J/kg]. Il calore di evaporazione r (o di vaporizzazione) può essere calcolato dalla relazione seguente Equazione di Clapeyron: dp r = T ( v v v l ) (5.6) dt Il calore di evaporazione è una funzione della sola temperatura, si annulla in corrispondenza della temperatura critica. 5.4 Diagrammi di Stato Se si considerano tutti gli stati di aggregazione in cui può presentarsi una sostanza pura, rappresentate su un sistema di coordinate spaziali le grandezze p,v,t il legame funzionale esistente tra di esse è rappresentabile graficamente come una superficie continua formata dall insieme delle singole superfici che descrivono ognuna gli stati della sostanza nelle singole fasi o in condizione bifasica. Se si considera un diagramma p-v-t, è possibile descrivervi il comportamento di una sostanza distinguendo (vedi figura 5.2) le zone in cui coesiste un equilibrio bifase dalle zone in cui la sostanza considerata si trova in equilibrio in un dato stato di aggregazione molecolare. Figura 5.2 Diagramma p-v-t per una sostanza pura. 71
6 Tracciando le linee isobare (uguale pressione) o le linee isoterme (uguale temperatura) è possibile seguire i cambiamenti di fase. Le curve p-v-t si presentano come in figura 5.3: è da notare il comportamento caratteristico dell'acqua (ma anche di antimonio, bismuto e gallio) che presentano una diversa inclinazione delle superfici di separazione solido - liquido. Tali sostanze infatti, durante il processo di solidificazione aumentano il volume specifico. Nel diagramma p-v-t è possibile evidenziare il punto triplo: ovvero la condizione per la quale coesistono in equilibrio le tre fasi. Per ciascuna sostanza al punto triplo corrispondono valori delle grandezze p, v, T rigorosamente definiti. Per l acqua, per esempio, p = 611 Pa, v = 0,001 m 3 /kg, T = 273,16 K (0,01 C). Figura 5.3 Diagramma p-v-t per l acqua Proiettando le diverse superfici nel piano p-t, è possibile ottenere il diagramma di equilibrio. In una tale rappresentazione le aree a due fasi si riducono a linee: i cambiamenti di fase avvengono infatti a pressione e temperatura costanti (figura 5.4). Possono essere interessanti anche i diagrammi T-v e p-v: nel primo, proiettando una linea isobara, è possibile seguire i passaggi di fase (vedi in figura 5.5) e rilevare le eventuali anomalie nel comportamento. Il secondo è utilizzabile soprattutto per seguire le trasformazioni liquido-vapore: in esso si può infatti evidenziare con chiarezza la curva che delimita l'equilibrio bifase liquido-vapore. Tale curva (detta curva limite o campana di Andrews) culmina nel punto critico, caratteristico di ciascuna sostanza. Il punto critico è caratterizzato dal fatto che tutte le proprietà dei due stati di aggregazione diventano identiche. Esso costituisce il limite oltre il quale non si riesce a distinguere, percorrendo una trasformazione isoterma, lo stato di aggregazione liquido da quello aeriforme: oltre tale isoterma (detta critica) si parla 72
7 genericamente di fluido. Se il sistema effettua una trasformazione isoterma (a temperatura inferiore a quella critica: vedi figura) che parte da uno stato di equilibrio in fase liquida L e che termina in uno stato di equilibrio in fase aeriforme G, il punto di partenza corrisponde ad uno stato di liquido sottoraffreddato, ovvero di liquido ad una temperatura inferiore rispetto a quella propria del corrispondente stato di saturazione (di liquido saturo), posto sulla curva limite, ad uguale pressione p L ; mentre lo stato di arrivo è detto di vapore surriscaldato, ovvero di vapore ad una temperatura superiore rispetto a quella del corrispondente stato di saturazione (di vapore saturo secco), posto sulla curva limite, ad uguale pressione p G. Figura 5.4 Diagramma di equilibrio p-t per una sostanza pura (a), per l acqua (b) Figura 5.5 Diagrammi T-v e p-v per una sostanza pura 73
8 Tabella 5.1. Valori caratteristici (punto critico, punto triplo) per alcune sostanze. Sostanza p T [bar] T T [K] T EN [K] p C [bar] T C [K] He 4,22 2,29 5,19 H 2 0,068 13,81 20,39 12,97 33,23 N 2 0,128 6,15 77,35 33,94 126,20 O 2 0, ,82 90,19 50,80 154,77 H 2 O 0, ,16 373,15 220,55 647,13 CO 2 5,17 216,48 73,77 31,04 NH 3 0,06 315,37 239,8 112,97 132, Equazioni di stato Sulla base del postulato noto come regola delle fasi, per un fluido puro comprimibile monofase, qualsiasi grandezza intensiva può essere descritta come funzione di solo altre due grandezze intensive. Le relazioni che coinvolgono la pressione p, la temperatura T ed il volume specifico v assumono grande importanza, sono note come equazioni di stato e possono essere date nella forma implicita: f (p, v, T) = 0 (5.1) Lo scopo più ovvio di una tale relazione è l utilizzo che se ne può fare per la determinazione del comportamento p-v-t di una sostanza in un determinato intervallo di valori. Nel prossimo capitolo si approfondirà questo argomento considerando una classe di fluidi termodinamici molto interessanti: i gas ideali. BIBLIOGRAFIA R.C. Reid, J.M. Prausnitz, B.E. Poling. The properties of gases & liquids. Mc Graw Hill int. Ed. - Fourth Ed K. Wark. Advanced thermodynamics for engineers. Mc Graw Hill int. Ed A. Cavallini, L. Mattarolo. Termodinamica Applicata. CLEUP - Padova
GLI STATI DI AGGREGAZIONE DELLA MATERIA. Lo stato gassoso
 GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato gassoso Classificazione della materia MATERIA Composizione Struttura Proprietà Trasformazioni 3 STATI DI AGGREGAZIONE SOLIDO (volume e forma propri) LIQUIDO
Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti.
 Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti. Solvente (componente presente in maggior quantità) SOLUZIONE Soluti
Una soluzione è un sistema omogeneo (cioè costituito da una sola fase, che può essere liquida, solida o gassosa) a due o più componenti. Solvente (componente presente in maggior quantità) SOLUZIONE Soluti
Complementi di Termologia. I parte
 Prof. Michele Giugliano (Dicembre 2) Complementi di Termologia. I parte N.. - Calorimetria. Il calore è una forma di energia, quindi la sua unità di misura, nel sistema SI, è il joule (J), tuttavia si
Prof. Michele Giugliano (Dicembre 2) Complementi di Termologia. I parte N.. - Calorimetria. Il calore è una forma di energia, quindi la sua unità di misura, nel sistema SI, è il joule (J), tuttavia si
Termodinamica: legge zero e temperatura
 Termodinamica: legge zero e temperatura Affrontiamo ora lo studio della termodinamica che prende in esame l analisi dell energia termica dei sistemi e di come tale energia possa essere scambiata, assorbita
Termodinamica: legge zero e temperatura Affrontiamo ora lo studio della termodinamica che prende in esame l analisi dell energia termica dei sistemi e di come tale energia possa essere scambiata, assorbita
La materia. La materia è ogni cosa che occupa uno spazio (e possiamo percepire con i nostri sensi).
 La materia La materia è ogni cosa che occupa uno spazio (e possiamo percepire con i nostri sensi). Essa è costituita da sostanze, ciascuna delle quali è formata da un determinato tipo di particelle piccolissime,
La materia La materia è ogni cosa che occupa uno spazio (e possiamo percepire con i nostri sensi). Essa è costituita da sostanze, ciascuna delle quali è formata da un determinato tipo di particelle piccolissime,
Stati di aggregazione della materia unità 2, modulo A del libro
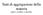 Stati di aggregazione della materia unità 2, modulo A del libro Gli stati di aggregazione della materia sono tre: solido, liquido e gassoso, e sono caratterizzati dalle seguenti grandezze: Quantità --->
Stati di aggregazione della materia unità 2, modulo A del libro Gli stati di aggregazione della materia sono tre: solido, liquido e gassoso, e sono caratterizzati dalle seguenti grandezze: Quantità --->
Gas perfetti e sue variabili
 Gas perfetti e sue variabili Un gas è detto perfetto quando: 1. è lontano dal punto di condensazione, e quindi è molto rarefatto 2. su di esso non agiscono forze esterne 3. gli urti tra le molecole del
Gas perfetti e sue variabili Un gas è detto perfetto quando: 1. è lontano dal punto di condensazione, e quindi è molto rarefatto 2. su di esso non agiscono forze esterne 3. gli urti tra le molecole del
Ripasso sulla temperatura, i gas perfetti e il calore
 Ripasso sulla temperatura, i gas perfetti e il calore Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia La temperatura Fenomeni non interpretabili con le leggi della meccanica Dilatazione
Ripasso sulla temperatura, i gas perfetti e il calore Prof. Daniele Ippolito Liceo Scientifico Amedeo di Savoia di Pistoia La temperatura Fenomeni non interpretabili con le leggi della meccanica Dilatazione
Università degli studi di MILANO Facoltà di AGRARIA. El. di Chimica e Chimica Fisica Mod. 2 CHIMICA FISICA. Lezione 2 LO STATO GASSOSO
 Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 2 CHIMICA FISICA Lezione 2 Anno Accademico 2010-2011 Docente: Dimitrios Fessas LO STATO GASSOSO Prof. Dimitrios
Università degli studi di MILANO Facoltà di AGRARIA El. di Chimica e Chimica Fisica Mod. 2 CHIMICA FISICA Lezione 2 Anno Accademico 2010-2011 Docente: Dimitrios Fessas LO STATO GASSOSO Prof. Dimitrios
Gas, liquidi, solidi. Tutti i gas, tranne l'elio, solidificano a basse temperature (alcuni richiedono anche alte pressioni).
 Gas, liquidi, solidi Tutti i gas raffreddati liquefano Tutti i gas, tranne l'elio, solidificano a basse temperature (alcuni richiedono anche alte pressioni). Sostanza T L ( C) T E ( C) He - -269 H 2-263
Gas, liquidi, solidi Tutti i gas raffreddati liquefano Tutti i gas, tranne l'elio, solidificano a basse temperature (alcuni richiedono anche alte pressioni). Sostanza T L ( C) T E ( C) He - -269 H 2-263
FISICA-TECNICA Miscela di gas e vapori. Igrometria
 FISICA-TECNICA Miscela di gas e vapori. Igrometria Katia Gallucci Spesso è necessario variare il contenuto di vapore presente in una corrente gassosa. Lo studio di come si possono realizzare queste variazioni
FISICA-TECNICA Miscela di gas e vapori. Igrometria Katia Gallucci Spesso è necessario variare il contenuto di vapore presente in una corrente gassosa. Lo studio di come si possono realizzare queste variazioni
CALORE. Compie lavoro. Il calore è energia. Temperatura e calore. L energia è la capacità di un corpo di compiere un lavoro
 Cos è il calore? Per rispondere si osservino le seguenti immagini Temperatura e calore Il calore del termosifone fa girare una girandola Il calore del termosifone fa scoppiare un palloncino Il calore del
Cos è il calore? Per rispondere si osservino le seguenti immagini Temperatura e calore Il calore del termosifone fa girare una girandola Il calore del termosifone fa scoppiare un palloncino Il calore del
Termologia. Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti
 Termologia Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti Trasmissione del calore Legge di Wien Legge di Stefan-Boltzmann Gas
Termologia Introduzione Scale Termometriche Espansione termica Capacità termica e calori specifici Cambiamenti di fase e calori latenti Trasmissione del calore Legge di Wien Legge di Stefan-Boltzmann Gas
LABORATORIO DI CHIMICA GENERALE E INORGANICA
 UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
UNIVERSITA DEGLI STUDI DI MILANO Facoltà di Scienze Matematiche, Fisiche e Naturali Corso di Laurea Triennale in Chimica CORSO DI: LABORATORIO DI CHIMICA GENERALE E INORGANICA Docente: Dr. Alessandro Caselli
9. TRASFORMAZIONI TERMODINAMICHE E CICLI REALI
 9. TRASFORMAZIONI TERMODINAMICHE E CICLI REALI 9. Introduzione I processi termodinamici che vengono realizzati nella pratica devono consentire la realizzazione di uno scambio di energia termica o di energia
9. TRASFORMAZIONI TERMODINAMICHE E CICLI REALI 9. Introduzione I processi termodinamici che vengono realizzati nella pratica devono consentire la realizzazione di uno scambio di energia termica o di energia
Capitolo 2 Le trasformazioni fisiche della materia
 Capitolo 2 Le trasformazioni fisiche della materia 1.Gli stati fisici della materia 2.I sistemi omogenei e i sistemi eterogenei 3.Le sostanze pure e i miscugli 4.I passaggi di stato 5. la teoria particellare
Capitolo 2 Le trasformazioni fisiche della materia 1.Gli stati fisici della materia 2.I sistemi omogenei e i sistemi eterogenei 3.Le sostanze pure e i miscugli 4.I passaggi di stato 5. la teoria particellare
L E L E G G I D E I G A S P A R T E I
 L E L E G G I D E I G A S P A R T E I Variabili di stato Equazioni di stato Legge di Boyle Pressione, temperatura, scale termometriche Leggi di Charles/Gay-Lussac Dispense di Chimica Fisica per Biotecnologie
L E L E G G I D E I G A S P A R T E I Variabili di stato Equazioni di stato Legge di Boyle Pressione, temperatura, scale termometriche Leggi di Charles/Gay-Lussac Dispense di Chimica Fisica per Biotecnologie
p atm 1. V B ; 2. T B ; 3. W A B 4. il calore specifico a volume costante c V
 1 Esercizio (tratto dal Problema 13.4 del Mazzoldi 2) Un gas ideale compie un espansione adiabatica contro la pressione atmosferica, dallo stato A di coordinate, T A, p A (tutte note, con p A > ) allo
1 Esercizio (tratto dal Problema 13.4 del Mazzoldi 2) Un gas ideale compie un espansione adiabatica contro la pressione atmosferica, dallo stato A di coordinate, T A, p A (tutte note, con p A > ) allo
Termodinamica. Sistema termodinamico. Piano di Clapeyron. Sistema termodinamico. Esempio. Cosa è la termodinamica? TERMODINAMICA
 Termodinamica TERMODINAMICA Cosa è la termodinamica? La termodinamica studia la conversione del calore in lavoro meccanico Prof Crosetto Silvio 2 Prof Crosetto Silvio Il motore dell automobile trasforma
Termodinamica TERMODINAMICA Cosa è la termodinamica? La termodinamica studia la conversione del calore in lavoro meccanico Prof Crosetto Silvio 2 Prof Crosetto Silvio Il motore dell automobile trasforma
CALCOLO DELL'ENERGIA INTERNA
 CALCOLO DELL'ENERGIA INTERNA Enrico Valenti Matricola 145442 29 novembre ore 10,30-12,30 ( trasformazione a temperatura costante ) U 0 = 0 J energia ( J ) p 0 = 1 bar pressione ( Pa ) T 0 = 273 K temperatura
CALCOLO DELL'ENERGIA INTERNA Enrico Valenti Matricola 145442 29 novembre ore 10,30-12,30 ( trasformazione a temperatura costante ) U 0 = 0 J energia ( J ) p 0 = 1 bar pressione ( Pa ) T 0 = 273 K temperatura
Funzioni funzione dominio codominio legge argomento variabile indipendente variabile dipendente
 Funzioni In matematica, una funzione f da X in Y consiste in: 1. un insieme X detto dominio di f 2. un insieme Y detto codominio di f 3. una legge che ad ogni elemento x in X associa uno ed un solo elemento
Funzioni In matematica, una funzione f da X in Y consiste in: 1. un insieme X detto dominio di f 2. un insieme Y detto codominio di f 3. una legge che ad ogni elemento x in X associa uno ed un solo elemento
LA TERMOLOGIA. studia le variazioni di dimensione di un corpo a causa di una
 LA TERMOLOGIA La termologia è la parte della fisica che si occupa dello studio del calore e dei fenomeni legati alle variazioni di temperatura subite dai corpi. Essa si può distinguere in: Termometria
LA TERMOLOGIA La termologia è la parte della fisica che si occupa dello studio del calore e dei fenomeni legati alle variazioni di temperatura subite dai corpi. Essa si può distinguere in: Termometria
1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He. 2) L'acqua è:
 1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He 2) L'acqua è: a. una sostanza elementare b. un composto chimico c. una miscela omogenea d. una soluzione 3) Quale dei seguenti elementi
1)Quale tra i seguenti elementi è un gas nobile? a. Si b. Mo c. Ge d. He 2) L'acqua è: a. una sostanza elementare b. un composto chimico c. una miscela omogenea d. una soluzione 3) Quale dei seguenti elementi
I DIAGRAMMA DI MOLLIER E TABELLE DEL VAPOR D'ACQUA
 I DIAGRAMMA DI MOLLIER E TABELLE DEL VAPOR D'ACQUA DIAGRAMMA DI MOLLIER DEL VAPORE D'ACQUA RAPPRESENTA I VALORI DELLE VARIABILI TERMODINAMICHE DEL VAPOR D'ACQUA IN UN PIANO h (ASSE Y) / s (ASSE X) h =
I DIAGRAMMA DI MOLLIER E TABELLE DEL VAPOR D'ACQUA DIAGRAMMA DI MOLLIER DEL VAPORE D'ACQUA RAPPRESENTA I VALORI DELLE VARIABILI TERMODINAMICHE DEL VAPOR D'ACQUA IN UN PIANO h (ASSE Y) / s (ASSE X) h =
2. Leggi finanziarie di capitalizzazione
 2. Leggi finanziarie di capitalizzazione Si chiama legge finanziaria di capitalizzazione una funzione atta a definire il montante M(t accumulato al tempo generico t da un capitale C: M(t = F(C, t C t M
2. Leggi finanziarie di capitalizzazione Si chiama legge finanziaria di capitalizzazione una funzione atta a definire il montante M(t accumulato al tempo generico t da un capitale C: M(t = F(C, t C t M
COMPONENTI TERMODINAMICI APERTI
 CAPITOLO NONO COMPONENTI TERMODINAMICI APERTI Esempi applicativi Vengono di seguito esaminati alcuni componenti di macchine termiche che possono essere considerati come sistemi aperti A) Macchina termica
CAPITOLO NONO COMPONENTI TERMODINAMICI APERTI Esempi applicativi Vengono di seguito esaminati alcuni componenti di macchine termiche che possono essere considerati come sistemi aperti A) Macchina termica
V= R*I. LEGGE DI OHM Dopo aver illustrato le principali grandezze elettriche è necessario analizzare i legami che vi sono tra di loro.
 LEGGE DI OHM Dopo aver illustrato le principali grandezze elettriche è necessario analizzare i legami che vi sono tra di loro. PREMESSA: Anche intuitivamente dovrebbe a questo punto essere ormai chiaro
LEGGE DI OHM Dopo aver illustrato le principali grandezze elettriche è necessario analizzare i legami che vi sono tra di loro. PREMESSA: Anche intuitivamente dovrebbe a questo punto essere ormai chiaro
SISTEMA BINARIO DI DUE LIQUIDI VOLATILI TOTALMENTE MISCIBILI che seguono Raoult
 SISTEM INRIO DI DUE IQUIDI OTII MENTE MISCIII che seguono Raoult Consideriamo due liquidi e totalmente miscibili di composizione χ e χ presenti in un contenitore ad una certa temperatura T=T 1. o strato
SISTEM INRIO DI DUE IQUIDI OTII MENTE MISCIII che seguono Raoult Consideriamo due liquidi e totalmente miscibili di composizione χ e χ presenti in un contenitore ad una certa temperatura T=T 1. o strato
Corrispondenze e funzioni
 Corrispondenze e funzioni L attività fondamentale della mente umana consiste nello stabilire corrispondenze e relazioni tra oggetti; è anche per questo motivo che il concetto di corrispondenza è uno dei
Corrispondenze e funzioni L attività fondamentale della mente umana consiste nello stabilire corrispondenze e relazioni tra oggetti; è anche per questo motivo che il concetto di corrispondenza è uno dei
Temperatura. V(t) = Vo (1+at) Strumento di misura: termometro
 I FENOMENI TERMICI Temperatura Calore Trasformazioni termodinamiche Gas perfetti Temperatura assoluta Gas reali Principi della Termodinamica Trasmissione del calore Termoregolazione del corpo umano Temperatura
I FENOMENI TERMICI Temperatura Calore Trasformazioni termodinamiche Gas perfetti Temperatura assoluta Gas reali Principi della Termodinamica Trasmissione del calore Termoregolazione del corpo umano Temperatura
3. Le Trasformazioni Termodinamiche
 3. Le Trasformazioni Termodinamiche Lo stato termodinamico di un gas (perfetto) è determinato dalle sue variabili di stato: ressione, olume, Temperatura, n moli ffinché esse siano determinate è necessario
3. Le Trasformazioni Termodinamiche Lo stato termodinamico di un gas (perfetto) è determinato dalle sue variabili di stato: ressione, olume, Temperatura, n moli ffinché esse siano determinate è necessario
13 La temperatura - 8. Il gas perfetto
 La mole e l equazione del gas perfetto Tutto ciò che vediamo intorno a noi è composto di piccolissimi grani, che chiamiamo «molecole». Per esempio, il ghiaccio, l acqua liquida e il vapore acqueo sono
La mole e l equazione del gas perfetto Tutto ciò che vediamo intorno a noi è composto di piccolissimi grani, che chiamiamo «molecole». Per esempio, il ghiaccio, l acqua liquida e il vapore acqueo sono
È una grandezza fisica FONDAMENTALE, SCALARE UNITÀ DI MISURA NEL S.I. : K (KELVIN)
 È una grandezza fisica FONDAMENTALE, SCALARE UNITÀ DI MISURA NEL S.I. : K (KELVIN) È STRETTAMENTE LEGATA ALLA VELOCITÀ DI VIBRAZIONE DELLE MOLECOLE IN UN CORPO: SE LA TEMPERATURA DI UN CORPO AUMENTA LE
È una grandezza fisica FONDAMENTALE, SCALARE UNITÀ DI MISURA NEL S.I. : K (KELVIN) È STRETTAMENTE LEGATA ALLA VELOCITÀ DI VIBRAZIONE DELLE MOLECOLE IN UN CORPO: SE LA TEMPERATURA DI UN CORPO AUMENTA LE
LEZIONE 1. Materia: Proprietà e Misura
 LEZIONE 1 Materia: Proprietà e Misura MISCELE, COMPOSTI, ELEMENTI SOSTANZE PURE E MISCUGLI La materia può essere suddivisa in sostanze pure e miscugli. Un sistema è puro solo se è formato da una singola
LEZIONE 1 Materia: Proprietà e Misura MISCELE, COMPOSTI, ELEMENTI SOSTANZE PURE E MISCUGLI La materia può essere suddivisa in sostanze pure e miscugli. Un sistema è puro solo se è formato da una singola
Università degli Studi di Milano Corso di Laurea in Chimica Industriale. Laboratorio di Processi e Impianti Industriali Chimici I
 Milano, Marzo 2014 Università degli Studi di Milano Corso di Laurea in Chimica Industriale Laboratorio di Processi e Impianti Industriali Chimici I Determinazione dell equilibrio Liquido-Vapore (condizioni
Milano, Marzo 2014 Università degli Studi di Milano Corso di Laurea in Chimica Industriale Laboratorio di Processi e Impianti Industriali Chimici I Determinazione dell equilibrio Liquido-Vapore (condizioni
LO STATO GASSOSO. Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi
 LO STATO GASSOSO Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi STATO GASSOSO Un sistema gassoso è costituito da molecole
LO STATO GASSOSO Proprietà fisiche dei gas Leggi dei gas Legge dei gas ideali Teoria cinetico-molecolare dei gas Solubilità dei gas nei liquidi STATO GASSOSO Un sistema gassoso è costituito da molecole
Relazioni statistiche: regressione e correlazione
 Relazioni statistiche: regressione e correlazione È detto studio della connessione lo studio si occupa della ricerca di relazioni fra due variabili statistiche o fra una mutabile e una variabile statistica
Relazioni statistiche: regressione e correlazione È detto studio della connessione lo studio si occupa della ricerca di relazioni fra due variabili statistiche o fra una mutabile e una variabile statistica
GAS. I gas si assomigliano tutti
 I gas si assomigliano tutti Aeriforme liquido solido GAS Descrizione macroscopica e microscopica degli stati di aggregazione della materia Fornendo energia al sistema, le forze di attrazione tra le particelle
I gas si assomigliano tutti Aeriforme liquido solido GAS Descrizione macroscopica e microscopica degli stati di aggregazione della materia Fornendo energia al sistema, le forze di attrazione tra le particelle
CHIMICA. Una teoria è scientifica solo se è falsificabile (cioè se è possibile sperimentalmente smentire le sue previsioni)
 CHIMICA SCIENZA SPERIMENTALE: cioè si basa sul metodo sperimentale (Galileo è il precursore). Osservazione dei fenomeni (raccolta e interpretazioni dati) Formulazione ipotesi Verifica sperimentale (eventualmente
CHIMICA SCIENZA SPERIMENTALE: cioè si basa sul metodo sperimentale (Galileo è il precursore). Osservazione dei fenomeni (raccolta e interpretazioni dati) Formulazione ipotesi Verifica sperimentale (eventualmente
'RPDQGHFRQFHWWXDOL Alcuni interrogativi su fenomeni fisici e chimici
 ,OPDWHULDOHGLGDWWLFRFKHVHJXHqVWDWRVFHOWRWUDGRWWRHDGDWWDWRGDO*UXSSRGLFKLPLFD GHOO,7,60DMRUDQDGL*UXJOLDVFR7RULQR0DUFR)DODVFD$QJHOR&LPHQLV3DROD&RVFLD /RUHGDQD$QJHOHUL$QWRQHOOD0DUWLQL'DULR*D]]ROD*UD]LD5L]]R*LXVL'L'LR
,OPDWHULDOHGLGDWWLFRFKHVHJXHqVWDWRVFHOWRWUDGRWWRHDGDWWDWRGDO*UXSSRGLFKLPLFD GHOO,7,60DMRUDQDGL*UXJOLDVFR7RULQR0DUFR)DODVFD$QJHOR&LPHQLV3DROD&RVFLD /RUHGDQD$QJHOHUL$QWRQHOOD0DUWLQL'DULR*D]]ROD*UD]LD5L]]R*LXVL'L'LR
Pressione. Esempio. Definizione di pressione. Legge di Stevino. Pressione nei fluidi EQUILIBRIO E CONSERVAZIONE DELL ENERGIA NEI FLUIDI
 Pressione EQUILIBRIO E CONSERVAZIONE DELL ENERGIA NEI FLUIDI Cos è la pressione? La pressione è una grandezza che lega tra di loro l intensità della forza e l aerea della superficie su cui viene esercitata
Pressione EQUILIBRIO E CONSERVAZIONE DELL ENERGIA NEI FLUIDI Cos è la pressione? La pressione è una grandezza che lega tra di loro l intensità della forza e l aerea della superficie su cui viene esercitata
1. Distribuzioni campionarie
 Università degli Studi di Basilicata Facoltà di Economia Corso di Laurea in Economia Aziendale - a.a. 2012/2013 lezioni di statistica del 3 e 6 giugno 2013 - di Massimo Cristallo - 1. Distribuzioni campionarie
Università degli Studi di Basilicata Facoltà di Economia Corso di Laurea in Economia Aziendale - a.a. 2012/2013 lezioni di statistica del 3 e 6 giugno 2013 - di Massimo Cristallo - 1. Distribuzioni campionarie
Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola.
 Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola. La formula empirica e una formula in cui il rappporto tra gli atomi e il piu semplice possibil Acqua Ammoniaca
Una formula molecolare è una formula chimica che dà l'esatto numero degli atomi di una molecola. La formula empirica e una formula in cui il rappporto tra gli atomi e il piu semplice possibil Acqua Ammoniaca
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Acqua azzurra, acqua chiara. Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao
 Acqua azzurra, acqua chiara Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao Proprietà fisiche Ecosistemi acquatici Origine della vita Ciclo dell acqua Acqua Scoperte Sensazioni Leggi La
Acqua azzurra, acqua chiara Istituto Comprensivo della Galilla Scuola Media Dessì - Ballao Proprietà fisiche Ecosistemi acquatici Origine della vita Ciclo dell acqua Acqua Scoperte Sensazioni Leggi La
Basi di matematica per il corso di micro
 Basi di matematica per il corso di micro Microeconomia (anno accademico 2006-2007) Lezione del 21 Marzo 2007 Marianna Belloc 1 Le funzioni 1.1 Definizione Una funzione è una regola che descrive una relazione
Basi di matematica per il corso di micro Microeconomia (anno accademico 2006-2007) Lezione del 21 Marzo 2007 Marianna Belloc 1 Le funzioni 1.1 Definizione Una funzione è una regola che descrive una relazione
LA CORRENTE ELETTRICA CONTINUA
 LA CORRENTE ELETTRICA CONTINUA (Fenomeno, indipendente dal tempo, che si osserva nei corpi conduttori quando le cariche elettriche fluiscono in essi.) Un conduttore metallico è in equilibrio elettrostatico
LA CORRENTE ELETTRICA CONTINUA (Fenomeno, indipendente dal tempo, che si osserva nei corpi conduttori quando le cariche elettriche fluiscono in essi.) Un conduttore metallico è in equilibrio elettrostatico
Energia e Lavoro. In pratica, si determina la dipendenza dallo spazio invece che dal tempo
 Energia e Lavoro Finora abbiamo descritto il moto dei corpi (puntiformi) usando le leggi di Newton, tramite le forze; abbiamo scritto l equazione del moto, determinato spostamento e velocità in funzione
Energia e Lavoro Finora abbiamo descritto il moto dei corpi (puntiformi) usando le leggi di Newton, tramite le forze; abbiamo scritto l equazione del moto, determinato spostamento e velocità in funzione
PINCH TECHNOLOGY. Il target può essere: minima area degli scambiatori minimo consumo di energia minimo costo annuo totale
 PINCH TECHNOLOGY Obiettivo => ottimizzare i flussi energetici nel sistema i.e. trovare la migliore disposizione degli scambiatori di calore (energia) necessari per ottenere le temperature finali richieste.
PINCH TECHNOLOGY Obiettivo => ottimizzare i flussi energetici nel sistema i.e. trovare la migliore disposizione degli scambiatori di calore (energia) necessari per ottenere le temperature finali richieste.
LEGGI DEI GAS / CALORI SPECIFICI. Introduzione 1
 LEGGI DEI GAS / CALORI SPECIFICI Introduzione 1 1 - TRASFORMAZIONE ISOBARA (p = costante) LA PRESSIONE RIMANE COSTANTE DURANTE TUTTA LA TRASFORMAZIONE V/T = costante (m, p costanti) Q = m c p (Tf - Ti)
LEGGI DEI GAS / CALORI SPECIFICI Introduzione 1 1 - TRASFORMAZIONE ISOBARA (p = costante) LA PRESSIONE RIMANE COSTANTE DURANTE TUTTA LA TRASFORMAZIONE V/T = costante (m, p costanti) Q = m c p (Tf - Ti)
Temperatura e Calore
 Temperatura e Calore 1 Temperatura e Calore Stati di Aggregazione Temperatura Scale Termometriche Dilatazione Termica Il Calore L Equilibrio Termico La Propagazione del Calore I Passaggi di Stato 2 Gli
Temperatura e Calore 1 Temperatura e Calore Stati di Aggregazione Temperatura Scale Termometriche Dilatazione Termica Il Calore L Equilibrio Termico La Propagazione del Calore I Passaggi di Stato 2 Gli
Proprieta meccaniche dei fluidi
 Proprieta meccaniche dei fluidi 1. Definizione di fluido: liquido o gas 2. La pressione in un fluido 3. Equilibrio nei fluidi: legge di Stevino 4. Il Principio di Pascal 5. Il barometro di Torricelli 6.
Proprieta meccaniche dei fluidi 1. Definizione di fluido: liquido o gas 2. La pressione in un fluido 3. Equilibrio nei fluidi: legge di Stevino 4. Il Principio di Pascal 5. Il barometro di Torricelli 6.
QUESITI DI FISICA RISOLTI A LEZIONE TERMODINAMICA
 QUESITI DI FISICA RISOLTI A LEZIONE TERMODINAMICA Un recipiente contiene gas perfetto a 27 o C, che si espande raggiungendo il doppio del suo volume iniziale a pressione costante. La temperatura finale
QUESITI DI FISICA RISOLTI A LEZIONE TERMODINAMICA Un recipiente contiene gas perfetto a 27 o C, che si espande raggiungendo il doppio del suo volume iniziale a pressione costante. La temperatura finale
Esercitazione X - Legge dei gas perfetti e trasformazioni
 Esercitazione X - Legge dei gas perfetti e trasformazioni termodinamiche Formulario Il primo principio della termodinamica afferma che la variazione dell energia interna di un sistema U è uguale alla somma
Esercitazione X - Legge dei gas perfetti e trasformazioni termodinamiche Formulario Il primo principio della termodinamica afferma che la variazione dell energia interna di un sistema U è uguale alla somma
Acidi e basi. HCl H + + Cl - (acido cloridrico) NaOH Na + + OH - (idrossido di sodio; soda caustica)
 Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Temperatura e Calore
 Temperatura e Calore La materia è un sistema fisico a molti corpi Gran numero di molecole (N A =6,02 10 23 ) interagenti tra loro Descrizione mediante grandezze macroscopiche (valori medi su un gran numero
Temperatura e Calore La materia è un sistema fisico a molti corpi Gran numero di molecole (N A =6,02 10 23 ) interagenti tra loro Descrizione mediante grandezze macroscopiche (valori medi su un gran numero
23 CAPITOLO 2: RELAZIONI TRA LE DIVERSE FASI DI UN CAMPIONE DI TERRENO
 v 23 CAPITOLO 2: RELAZIONI TRA LE DIERSE FASI DI UN CAMPIONE DI TERRENO CAPITOLO 2: RELAZIONI TRA LE DIERSE FASI DI UN CAMPIONE DI TERRENO Un campione di terreno viene considerato come un sistema multifase,
v 23 CAPITOLO 2: RELAZIONI TRA LE DIERSE FASI DI UN CAMPIONE DI TERRENO CAPITOLO 2: RELAZIONI TRA LE DIERSE FASI DI UN CAMPIONE DI TERRENO Un campione di terreno viene considerato come un sistema multifase,
Classificazione della materia: Sostanze pure e miscugli
 Classificazione della materia: Sostanze pure e miscugli la composizione e quindi le proprietà intensive sono le stesse in ogni parte del sistema La composizione e le proprietà intensive variano da una
Classificazione della materia: Sostanze pure e miscugli la composizione e quindi le proprietà intensive sono le stesse in ogni parte del sistema La composizione e le proprietà intensive variano da una
Ripetizioni Cagliari di Manuele Atzeni - 3497702002 - info@ripetizionicagliari.it
 Calorimetria: soluzioni Problema di: Calorimetria - Q0001 Problema di: Calorimetria - Q0002 Scheda 8 Ripetizioni Cagliari di Manuele Atzeni - 3497702002 - info@ripetizionicagliari.it Testo [Q0001] Quanta
Calorimetria: soluzioni Problema di: Calorimetria - Q0001 Problema di: Calorimetria - Q0002 Scheda 8 Ripetizioni Cagliari di Manuele Atzeni - 3497702002 - info@ripetizionicagliari.it Testo [Q0001] Quanta
IMPIANTI DI CLIMATIZZAZIONE: TERMODINAMICA DEI CICLI FRIGORIFERI AD ARIA ED ACQUA. Ing. Attilio Pianese (commissione Energia e Impianti)
 IMPIANTI DI CLIMATIZZAZIONE: TERMODINAMICA DEI CICLI FRIGORIFERI AD ARIA ED ACQUA Ing. Attilio Pianese (commissione Energia e Impianti) SCOPO DEGLI IMPIANTI DI CONDIZIONAMENTO Gli impianti di condizionamento
IMPIANTI DI CLIMATIZZAZIONE: TERMODINAMICA DEI CICLI FRIGORIFERI AD ARIA ED ACQUA Ing. Attilio Pianese (commissione Energia e Impianti) SCOPO DEGLI IMPIANTI DI CONDIZIONAMENTO Gli impianti di condizionamento
EQUAZIONE DI STATO e LEGGI DEI GAS esercizi risolti Classi quarte L.S.
 EQUAZIONE DI STATO e LEGGI DEI GAS esercizi risolti Classi quarte L.S. In questa dispensa verrà riportato lo svolgimento di alcuni esercizi inerenti l'equazione di stato dei gas perfetti e le principali
EQUAZIONE DI STATO e LEGGI DEI GAS esercizi risolti Classi quarte L.S. In questa dispensa verrà riportato lo svolgimento di alcuni esercizi inerenti l'equazione di stato dei gas perfetti e le principali
352&(662',&20%867,21(
 352&(662',&20%867,21( Il calore utilizzato come fonte energetica convertibile in lavoro nella maggior parte dei casi, è prodotto dalla combustione di sostanze (es. carbone, metano, gasolio) chiamate combustibili.
352&(662',&20%867,21( Il calore utilizzato come fonte energetica convertibile in lavoro nella maggior parte dei casi, è prodotto dalla combustione di sostanze (es. carbone, metano, gasolio) chiamate combustibili.
Complementi di Analisi per Informatica *** Capitolo 2. Numeri Complessi. e Circuiti Elettrici. a Corrente Alternata. Sergio Benenti 7 settembre 2013
 Complementi di Analisi per nformatica *** Capitolo 2 Numeri Complessi e Circuiti Elettrici a Corrente Alternata Sergio Benenti 7 settembre 2013? ndice 2 Circuiti elettrici a corrente alternata 1 21 Circuito
Complementi di Analisi per nformatica *** Capitolo 2 Numeri Complessi e Circuiti Elettrici a Corrente Alternata Sergio Benenti 7 settembre 2013? ndice 2 Circuiti elettrici a corrente alternata 1 21 Circuito
LE FUNZIONI A DUE VARIABILI
 Capitolo I LE FUNZIONI A DUE VARIABILI In questo primo capitolo introduciamo alcune definizioni di base delle funzioni reali a due variabili reali. Nel seguito R denoterà l insieme dei numeri reali mentre
Capitolo I LE FUNZIONI A DUE VARIABILI In questo primo capitolo introduciamo alcune definizioni di base delle funzioni reali a due variabili reali. Nel seguito R denoterà l insieme dei numeri reali mentre
Transitori del primo ordine
 Università di Ferrara Corso di Elettrotecnica Transitori del primo ordine Si consideri il circuito in figura, composto da un generatore ideale di tensione, una resistenza ed una capacità. I tre bipoli
Università di Ferrara Corso di Elettrotecnica Transitori del primo ordine Si consideri il circuito in figura, composto da un generatore ideale di tensione, una resistenza ed una capacità. I tre bipoli
PSICROMETRIA DELL ARIA UMIDA
 PSICROMETRIA DELL ARIA UMIDA 1. PROPRIETÀ TERMODINAMICHE DEI GAS PERFETTI Un modello di comportamento interessante per la termodinamica è quello cosiddetto d i gas perfetto. Il gas perfetto è naturalmente
PSICROMETRIA DELL ARIA UMIDA 1. PROPRIETÀ TERMODINAMICHE DEI GAS PERFETTI Un modello di comportamento interessante per la termodinamica è quello cosiddetto d i gas perfetto. Il gas perfetto è naturalmente
Indice. 1 Introduzione alle Equazioni Differenziali 1 1.1 Esempio introduttivo... 1 1.2 Nomenclatura e Teoremi di Esistenza ed Unicità...
 Indice 1 Introduzione alle Equazioni Differenziali 1 1.1 Esempio introduttivo............................. 1 1.2 Nomenclatura e Teoremi di Esistenza ed Unicità.............. 5 i Capitolo 1 Introduzione
Indice 1 Introduzione alle Equazioni Differenziali 1 1.1 Esempio introduttivo............................. 1 1.2 Nomenclatura e Teoremi di Esistenza ed Unicità.............. 5 i Capitolo 1 Introduzione
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA
 LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
I.T.C.G.T T. Acerbo - Pescara LABORATORIO DI FISICA A. S. 2009/10
 I.T.C.G.T T. Acerbo - Pescara LABORATORIO DI FISICA A. S. 2009/10 Cognome: D Ovidio Nome: Stefania Classe: 2 B Geometri Data: 04/12/2009 Gruppo: F. Illiceto; V. Ivanochko; M.C. Scopino; M.Terenzi N. pagine:
I.T.C.G.T T. Acerbo - Pescara LABORATORIO DI FISICA A. S. 2009/10 Cognome: D Ovidio Nome: Stefania Classe: 2 B Geometri Data: 04/12/2009 Gruppo: F. Illiceto; V. Ivanochko; M.C. Scopino; M.Terenzi N. pagine:
POMPA DI CALORE CICLO FRIGORIFERO A COMPRESSIONE DI VAPORE
 POMPA DI CALORE CONDENSATORE = + L T = + L C ORGANO DI ESPANSIONE LIQUIDO COMPRESSORE T COND. E D T 1 VAPORE T EVAP. A B T 2 Schema a blocchi di una macchina frigorifera EVAPORATORE Dal punto di vista
POMPA DI CALORE CONDENSATORE = + L T = + L C ORGANO DI ESPANSIONE LIQUIDO COMPRESSORE T COND. E D T 1 VAPORE T EVAP. A B T 2 Schema a blocchi di una macchina frigorifera EVAPORATORE Dal punto di vista
Esercizi di Fisica Generale
 Esercizi di Fisica Generale 2. Temodinamica prof. Domenico Galli, dott. Daniele Gregori, prof. Umberto Marconi dott. Alessandro Tronconi 27 marzo 2012 I compiti scritti di esame del prof. D. Galli propongono
Esercizi di Fisica Generale 2. Temodinamica prof. Domenico Galli, dott. Daniele Gregori, prof. Umberto Marconi dott. Alessandro Tronconi 27 marzo 2012 I compiti scritti di esame del prof. D. Galli propongono
1. PRIME PROPRIETÀ 2
 RELAZIONI 1. Prime proprietà Il significato comune del concetto di relazione è facilmente intuibile: due elementi sono in relazione se c è un legame tra loro descritto da una certa proprietà; ad esempio,
RELAZIONI 1. Prime proprietà Il significato comune del concetto di relazione è facilmente intuibile: due elementi sono in relazione se c è un legame tra loro descritto da una certa proprietà; ad esempio,
APPUNTI DEL CORSO DI SISTEMI IMPIANTISTICI E SICUREZZA INTRODUZIONE AGLI IMPIANTI ELETTRICI: FONDAMENTI DI ELETTROTECNICA
 APPUNTI DEL CORSO DI SISTEMI IMPIANTISTICI E SICUREZZA INTRODUZIONE AGLI IMPIANTI ELETTRICI: FONDAMENTI DI ELETTROTECNICA Concetti e grandezze fondamentali CAMPO ELETTRICO: è un campo vettoriale di forze,
APPUNTI DEL CORSO DI SISTEMI IMPIANTISTICI E SICUREZZA INTRODUZIONE AGLI IMPIANTI ELETTRICI: FONDAMENTI DI ELETTROTECNICA Concetti e grandezze fondamentali CAMPO ELETTRICO: è un campo vettoriale di forze,
Si classifica come una grandezza intensiva
 CAP 13: MISURE DI TEMPERATURA La temperatura È osservata attraverso gli effetti che provoca nelle sostanze e negli oggetti Si classifica come una grandezza intensiva Può essere considerata una stima del
CAP 13: MISURE DI TEMPERATURA La temperatura È osservata attraverso gli effetti che provoca nelle sostanze e negli oggetti Si classifica come una grandezza intensiva Può essere considerata una stima del
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione
 REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
Funzioni inverse Simmetrie rispetto alla bisettrice dei quadranti dispari. Consideriamo la trasformazione descritta dalle equazioni : = y
 Funzioni inverse Simmetrie rispetto alla bisettrice dei quadranti dispari. Consideriamo la trasformazione descritta dalle equazioni : ' = y y' = Consideriamo il punto P(,5) se eseguiamo tra trasformazione
Funzioni inverse Simmetrie rispetto alla bisettrice dei quadranti dispari. Consideriamo la trasformazione descritta dalle equazioni : ' = y y' = Consideriamo il punto P(,5) se eseguiamo tra trasformazione
Spettrofotometria. Le onde luminose consistono in campi magnetici e campi elettrici oscillanti, fra loro perpendicolari.
 Spettrofotometria. Con questo termine si intende l utilizzo della luce nella misura delle concentrazioni chimiche. Per affrontare questo argomento dovremo conoscere: Natura e proprietà della luce. Cosa
Spettrofotometria. Con questo termine si intende l utilizzo della luce nella misura delle concentrazioni chimiche. Per affrontare questo argomento dovremo conoscere: Natura e proprietà della luce. Cosa
LA CORRENTE ELETTRICA
 L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
L CORRENTE ELETTRIC H P h Prima che si raggiunga l equilibrio c è un intervallo di tempo dove il livello del fluido non è uguale. Il verso del movimento del fluido va dal vaso a livello maggiore () verso
CORRENTE E TENSIONE ELETTRICA LA CORRENTE ELETTRICA
 CORRENTE E TENSIONE ELETTRICA La conoscenza delle grandezze elettriche fondamentali (corrente e tensione) è indispensabile per definire lo stato di un circuito elettrico. LA CORRENTE ELETTRICA DEFINIZIONE:
CORRENTE E TENSIONE ELETTRICA La conoscenza delle grandezze elettriche fondamentali (corrente e tensione) è indispensabile per definire lo stato di un circuito elettrico. LA CORRENTE ELETTRICA DEFINIZIONE:
FONDAMENTI CHIMICO FISICI DEI PROCESSI IL SECONDO E IL TERZO PRINCIPIO DELLA TERMODINAMICA
 FONDAMENTI CHIMICO FISICI DEI PROCESSI IL SECONDO E IL TERZO PRINCIPIO DELLA TERMODINAMICA LE MACCHINE TERMICHE Sono sistemi termodinamici che trasformano il calore in lavoro. Operano ciclicamente, cioè
FONDAMENTI CHIMICO FISICI DEI PROCESSI IL SECONDO E IL TERZO PRINCIPIO DELLA TERMODINAMICA LE MACCHINE TERMICHE Sono sistemi termodinamici che trasformano il calore in lavoro. Operano ciclicamente, cioè
2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà. I liquidi e loro proprietà
 2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà 1 I liquidi e loro proprietà 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito. I gas occupano i loro contenitori uniformemente
2014 2015 CCS - Biologia CCS - Fisica I gas e loro proprietà 1 I liquidi e loro proprietà 2 Proprietà Generali dei Gas I gas possono essere espansi all infinito. I gas occupano i loro contenitori uniformemente
Consideriamo due polinomi
 Capitolo 3 Il luogo delle radici Consideriamo due polinomi N(z) = (z z 1 )(z z 2 )... (z z m ) D(z) = (z p 1 )(z p 2 )... (z p n ) della variabile complessa z con m < n. Nelle problematiche connesse al
Capitolo 3 Il luogo delle radici Consideriamo due polinomi N(z) = (z z 1 )(z z 2 )... (z z m ) D(z) = (z p 1 )(z p 2 )... (z p n ) della variabile complessa z con m < n. Nelle problematiche connesse al
Fresco con il sol e 60% de risparmio energetico. SOLARCOOL TECNOLOGIA Spiegazione termodinamica
 Fresco con il sol e 60% de risparmio energetico SOLARCOOL TECNOLOGIA Spiegazione termodinamica L efficienza del sistema Solar Cool è possibile grazie ad un effetto fisico del flusso di massa, che è un
Fresco con il sol e 60% de risparmio energetico SOLARCOOL TECNOLOGIA Spiegazione termodinamica L efficienza del sistema Solar Cool è possibile grazie ad un effetto fisico del flusso di massa, che è un
Dimensione di uno Spazio vettoriale
 Capitolo 4 Dimensione di uno Spazio vettoriale 4.1 Introduzione Dedichiamo questo capitolo ad un concetto fondamentale in algebra lineare: la dimensione di uno spazio vettoriale. Daremo una definizione
Capitolo 4 Dimensione di uno Spazio vettoriale 4.1 Introduzione Dedichiamo questo capitolo ad un concetto fondamentale in algebra lineare: la dimensione di uno spazio vettoriale. Daremo una definizione
Esercitazione IX - Calorimetria
 Esercitazione IX - Calorimetria Esercizio 1 Un blocco di rame di massa m Cu = 5g si trova a una temperatura iniziale T i = 25 C. Al blocco viene fornito un calore Q = 120J. Determinare la temperatura finale
Esercitazione IX - Calorimetria Esercizio 1 Un blocco di rame di massa m Cu = 5g si trova a una temperatura iniziale T i = 25 C. Al blocco viene fornito un calore Q = 120J. Determinare la temperatura finale
FUNZIONE. Si scrive: A B f: A B x y=f(x) (si legge: f funzione da A in B) x f y= f(x)
 1 FUNZIONE Dati gli insiemi A e B, si definisce funzione da A in B una relazione o legge o corrispondenza che ad ogni elemento di A associa uno ed un solo elemento di B. Si scrive: A B f: A B f() (si legge:
1 FUNZIONE Dati gli insiemi A e B, si definisce funzione da A in B una relazione o legge o corrispondenza che ad ogni elemento di A associa uno ed un solo elemento di B. Si scrive: A B f: A B f() (si legge:
Come visto precedentemente l equazione integro differenziale rappresentativa dell equilibrio elettrico di un circuito RLC è la seguente: 1 = (1)
 Transitori Analisi nel dominio del tempo Ricordiamo che si definisce transitorio il periodo di tempo che intercorre nel passaggio, di un sistema, da uno stato energetico ad un altro, non è comunque sempre
Transitori Analisi nel dominio del tempo Ricordiamo che si definisce transitorio il periodo di tempo che intercorre nel passaggio, di un sistema, da uno stato energetico ad un altro, non è comunque sempre
Rette e curve, piani e superfici
 Rette e curve piani e superfici ) dicembre 2 Scopo di questo articolo è solo quello di proporre uno schema riepilogativo che metta in luce le caratteristiche essenziali delle equazioni di rette e curve
Rette e curve piani e superfici ) dicembre 2 Scopo di questo articolo è solo quello di proporre uno schema riepilogativo che metta in luce le caratteristiche essenziali delle equazioni di rette e curve
APPUNTI DI MATEMATICA ALGEBRA \ INSIEMISTICA \ TEORIA DEGLI INSIEMI (1)
 ALGEBRA \ INSIEMISTICA \ TEORIA DEGLI INSIEMI (1) Un insieme è una collezione di oggetti. Il concetto di insieme è un concetto primitivo. Deve esistere un criterio chiaro, preciso, non ambiguo, inequivocabile,
ALGEBRA \ INSIEMISTICA \ TEORIA DEGLI INSIEMI (1) Un insieme è una collezione di oggetti. Il concetto di insieme è un concetto primitivo. Deve esistere un criterio chiaro, preciso, non ambiguo, inequivocabile,
LA MACCHINA FRIGORIFERA E LA POMPA DI
 asdf LA MACCHINA FRIGORIFERA E LA POMPA DI CALORE 12 March 2012 Il ciclo di Carnot... "al contrario" Nell'articolo dedicato alla macchina termica, avevamo visto nel finale la macchina di Carnot e il ciclo
asdf LA MACCHINA FRIGORIFERA E LA POMPA DI CALORE 12 March 2012 Il ciclo di Carnot... "al contrario" Nell'articolo dedicato alla macchina termica, avevamo visto nel finale la macchina di Carnot e il ciclo
Anno 3. Funzioni: dominio, codominio e campo di esistenza
 Anno 3 Funzioni: dominio, codominio e campo di esistenza 1 Introduzione In questa lezione parleremo delle funzioni. Ne daremo una definizione e impareremo a studiarne il dominio in relazione alle diverse
Anno 3 Funzioni: dominio, codominio e campo di esistenza 1 Introduzione In questa lezione parleremo delle funzioni. Ne daremo una definizione e impareremo a studiarne il dominio in relazione alle diverse
LA MATERIA Suggerimenti didattici e schede
 LA MATERIA Suggerimenti didattici e schede Iniziamo il percorso chiedendo a un bambino di consegnarci alcune cose: una gomma, una penna, un capello. Domandiamo a un altro di consegnarci una gioia, una
LA MATERIA Suggerimenti didattici e schede Iniziamo il percorso chiedendo a un bambino di consegnarci alcune cose: una gomma, una penna, un capello. Domandiamo a un altro di consegnarci una gioia, una
e-dva - eni-depth Velocity Analysis
 Lo scopo dell Analisi di Velocità di Migrazione (MVA) è quello di ottenere un modello della velocità nel sottosuolo che abbia dei tempi di riflessione compatibili con quelli osservati nei dati. Ciò significa
Lo scopo dell Analisi di Velocità di Migrazione (MVA) è quello di ottenere un modello della velocità nel sottosuolo che abbia dei tempi di riflessione compatibili con quelli osservati nei dati. Ciò significa
Moto circolare uniforme
 Moto circolare uniforme 01 - Moto circolare uniforme. Il moto di un corpo che avviene su una traiettoria circolare (una circonferenza) con velocità (in modulo, intensità) costante si dice moto circolare
Moto circolare uniforme 01 - Moto circolare uniforme. Il moto di un corpo che avviene su una traiettoria circolare (una circonferenza) con velocità (in modulo, intensità) costante si dice moto circolare
La distribuzione Normale. La distribuzione Normale
 La Distribuzione Normale o Gaussiana è la distribuzione più importante ed utilizzata in tutta la statistica La curva delle frequenze della distribuzione Normale ha una forma caratteristica, simile ad una
La Distribuzione Normale o Gaussiana è la distribuzione più importante ed utilizzata in tutta la statistica La curva delle frequenze della distribuzione Normale ha una forma caratteristica, simile ad una
Matematica generale CTF
 Successioni numeriche 19 agosto 2015 Definizione di successione Monotonìa e limitatezza Forme indeterminate Successioni infinitesime Comportamento asintotico Criterio del rapporto per le successioni Definizione
Successioni numeriche 19 agosto 2015 Definizione di successione Monotonìa e limitatezza Forme indeterminate Successioni infinitesime Comportamento asintotico Criterio del rapporto per le successioni Definizione
Esponenziali elogaritmi
 Esponenziali elogaritmi Potenze ad esponente reale Ricordiamo che per un qualsiasi numero razionale m n prendere n>0) si pone a m n = n a m (in cui si può sempre a patto che a sia un numero reale positivo.
Esponenziali elogaritmi Potenze ad esponente reale Ricordiamo che per un qualsiasi numero razionale m n prendere n>0) si pone a m n = n a m (in cui si può sempre a patto che a sia un numero reale positivo.
Visione d insieme DOMANDE E RISPOSTE SULL UNITÀ
 Visione d insieme DOMANDE E RISPOSTE SULL UNITÀ Che cos è la corrente elettrica? Nei conduttori metallici la corrente è un flusso di elettroni. L intensità della corrente è il rapporto tra la quantità
Visione d insieme DOMANDE E RISPOSTE SULL UNITÀ Che cos è la corrente elettrica? Nei conduttori metallici la corrente è un flusso di elettroni. L intensità della corrente è il rapporto tra la quantità
L H 2 O nelle cellule vegetali e
 L H 2 O nelle cellule vegetali e il suo trasporto nella pianta H 2 O 0.96 Å H O 105 H 2s 2 2p 4 tendenza all ibridizzazione sp 3 H δ+ O δ- δ+ 1.75 Å H legame idrogeno O δ- H H δ+ δ+ energia del legame
L H 2 O nelle cellule vegetali e il suo trasporto nella pianta H 2 O 0.96 Å H O 105 H 2s 2 2p 4 tendenza all ibridizzazione sp 3 H δ+ O δ- δ+ 1.75 Å H legame idrogeno O δ- H H δ+ δ+ energia del legame
Il trasporto di materia. Principi di Ingegneria Chimica Ambientale
 Il trasporto di materia Principi di Ingegneria Chimica Ambientale 1 Considerazioni preliminari Il nostro studio sarà limitato a: miscele binarie miscele diluite (ossia in cui la frazione molare di uno
Il trasporto di materia Principi di Ingegneria Chimica Ambientale 1 Considerazioni preliminari Il nostro studio sarà limitato a: miscele binarie miscele diluite (ossia in cui la frazione molare di uno
