I benefici dei contraccettivi ormonali combinati (COC) continuano a
|
|
|
- Gilberta Nicoletti
- 7 anni fa
- Visualizzazioni
Transcript
1 22 Novembre 2013 EMA/709120/2013 I benefici dei contraccettivi ormonali combinati (COC) continuano a superarne i rischi Informazioni sui medicinali da aggiornare per aiutare le donne a prendere decisioni informate circa la loro scelta di contraccezione L Agenzia Europea dei Medicinali ha ora completato la sua rivalutazione dei contraccettivi ormonali combinati (COC), in particolare del rischio di tromboembolia venosa (TEV o coaguli di sangue nelle vene) associato al loro uso. Il Committee for Medicinal Products for Human Use (CHMP) dell'agenzia Europea dei medicinali ha concluso che i benefici dei COC nel prevenire gravidanze indesiderate continuano a superare i loro rischi, e che il ben noto rischio di TEV associato all uso di tutti i COC è basso. La rivalutazione ha rafforzato l'importanza di garantire che siano previste informazioni chiare ed aggiornate per le donne che fanno uso di questi medicinali e per i professionisti sanitari che forniscono consulenza ed assistenza clinica. Le informazioni sui COC saranno aggiornate per aiutare le donne a prendere decisioni informate insieme al loro medico circa la loro scelta di contraccezione. E importante che le donne siano rese consapevoli del rischio di TEV e dei suoi segni e sintomi, e che i medici, nel prescrivere un contraccettivo, prendano in considerazione i fattori di rischio individuali di ciascuna donna. I medici dovrebbero anche considerare come il rischio di TEV associato ad un particolare COC si confronti con gli altri COC (vedere tabella di seguito). La rivalutazione ha anche esaminato il rischio di tromboembolia arteriosa (TEA, coaguli di sangue nelle arterie, che possono potenzialmente causare un ictus o un attacco cardiaco). Questo rischio è molto basso e non vi è alcuna prova di una differenza nel livello di rischio tra medicinali a seconda del tipo di progestinico. Il parere del CHMP, in accordo con la precedente raccomandazione del Pharmacovigilance Risk Assessment Committee (PRAC), sarà ora inviata alla Commissione Europea per l'adozione di una decisione giuridicamente vincolante per aggiornare le informazioni sui medicinali di tutti i COC in tutta l'ue. 7 Westferry Circus Canary Wharf London E14 4HB United Kingdom Telephone +44 (0) Facsimile +44 (0) info@ema.europa.eu Website An agency of the European Union European Medicines Agency, Reproduction is authorised provided the source is acknowledged.
2 Informazioni per le pazienti Questa ampia rivalutazione europea ha considerato i benefici ed i rischi associati all uso dei contraccettivi ormonali combinati (COC), in particolare il rischio di formazione di coaguli di sangue associato a questi farmaci. Ha confermato che i benefici dei COC superano il rischio di formazione di coaguli di sangue, rischio che è stato ben noto per molti anni ed è molto basso. Se avete assunto un COC senza alcun problema, non vi è alcun motivo di interromperne l'assunzione sulla base di questa rivalutazione. E importante, però, che siate consapevoli del rischio di formazione di coaguli di sangue associato all uso di questi farmaci, anche se è molto basso. Il rischio di formazione coaguli di sangue nelle vene varia tra i COC, a seconda del tipo di progestinico (un ormone) che contengono e può variare da 5 a 12 casi di coaguli di sangue per donne che li utilizzano per un anno (vedere tabella di seguito). Ciò a fronte di 2 casi di coaguli di sangue nelle vene ogni anno per donne che non utilizzano COC. Si dovrebbe anche essere consapevoli dei fattori che aumentano il vostro rischio di formazione di coaguli ed essere a conoscenza di come questi possono cambiare nel tempo. I fattori di rischio includono l'essere molto in sovrappeso, l'aumento dell'età, l avere un membro della famiglia che ha avuto un coagulo di sangue in età relativamente giovane (ad esempio sotto i 50 anni), l avere emicrania o l essere immobilizzati per un lungo periodo (ad esempio a causa di una malattia o infortunio). Il vostro rischio di formazione di un coagulo di sangue è anche più alto nel primo anno di utilizzo di un COC. Si dovrebbe discutere con il proprio medico curante qual è per voi il tipo più contraccezione. appropriato di Quando si assume un COC, dovreste essere attente ai segni e sintomi di coaguli di sangue, che possono includere dolore o gonfiore alle gambe, improvvisa ed inspiegabile mancanza di respiro, respirazione rapida o tosse, dolore toracico, debolezza o intorpidimento del viso, del braccio o della gamba. Se manifestate uno di questi segni e sintomi dovete consultare immediatamente un medico. Se avete domande o dubbi, parlatene con il vostro medico, farmacista o infermiere. Informazioni per gli operatori sanitari L ampia rivalutazione europea dei contraccettivi ormonali combinati (COC) ha confermato che il rischio noto di tromboembolia venosa (TEV) associato all uso di tutti i COC a basse dosi (etinilestradiolo <50 mcg) è piccolo. Esistono differenze tra i COC nel loro rischio di TEV a seconda del tipo di progestinico che contengono. I dati attualmente disponibili indicano che i COC contenenti i progestinici levonorgestrel, noretisterone o norgestimate hanno il più basso rischio di TEV (vedere tabella sotto). Quando si prescrive un COC, dovrebbe essere prestata un attenta considerazione ai fattori di rischio individuali in atto nella donna, in particolare quelli per TEV, e la differenza nel rischio di TEV tra i medicinali. I COC sono controindicati se una donna ha uno o più fattori di rischio gravi che la espongano ad alto rischio di formazione coaguli di sangue. EMA/709120/2013 Page 2/5
3 Non vi è alcuna evidenza di differenze tra COC a basso dosaggio nel loro rischio di tromboembolia arteriosa (TEA). Poiché i fattori di rischio individuali di una donna cambieranno nel corso del tempo, vi è la necessità di rivalutare periodicamente l'idoneità del suo contraccettivo. E anche importante aumentare la consapevolezza su segni e sintomi di TEV e prescrive un COC. TEA quando si Il personale sanitario dovrebbe sempre prendere in considerazione la possibilità di una tromboembolia associata all uso di COC con una donna che mostra i sintomi sopra descritti. EMA/709120/2013 Page 3/5
4 Rischio di sviluppare un coagulo di sangue ( TEV) in un anno Donne che non assumono una compressa/cerotto/anello ormonale combinato e che non sono incinte levonorgestrel, noretisterone o norgestimate etonogestrel o norelgestromina drospirenone, gestodene o desogestrel clormadinone, dienogest o nomegestrolo Circa 2 su donne Circa 5 7 su donne Circa 6 12 su donne Circa 9 12 su donne Non ancora noto 1 Ulteriori studi sono in corso o in programma per raccogliere dati sufficienti per stimare il rischio associato a questi medicinali. 1 Informazioni aggiuntive sui medicinali I COC contengono due tipi di ormoni, un estrogeno e un progestinico. La rivalutazione ha incluso tutti i contraccettivi contenenti estrogeni a basso dosaggio ed i seguenti progestinici: clormadinone, desogestrel, dienogest, drospirenone, etonogestrel, gestodene, nomegestrolo, norelgestromina e norgestimato. Questi sono a volte denominati come contraccettivi di 'terza generazione' o di 'quarta generazione' e sono disponibili come compresse, cerotti e anelli vaginali. Durante la rivalutazione, il rischio di TEV associato all uso con questi medicinali è stato confrontato con quello dei COC contenenti levonorgestrel e noretisterone (anche noti come contraccettivi di 'seconda generazione'). La classificazione come 'seconda, terza o quarta generazione' non è comunque basata su dati scientifici e non è standardizzata, e può variare tra istituzioni e pubblicazioni. Con l'eccezione di Zoely (nomegestrolo acetato/estradiolo), Ioa (nomegestrolo acetato/ estradiolo) ed Evra (norelgestromina/etinilestradiolo), che sono stati autorizzati a livello centrale attraverso l'ema, tutti gli altri contraccettivi combinati nell'unione Europea sono stati autorizzati tramite procedure nazionali. Informazioni aggiuntive sulla procedura La rivalutazione dei contraccettivi ormonali combinati è stata iniziata nel mese di Febbraio 2013 su richiesta della Francia secondo l articolo 31 della Direttiva 2001/83/CE. La fase iniziale di questa rivalutazione è stata effettuata dal Pharmacovigilance Risk Assessment Committee (PRAC), il Comitato responsabile della valutazione di problematiche di sicurezza EMA/709120/2013 Page 4/5
5 inerenti i medicinali ad uso umano, che ha emesso una serie di raccomandazioni. Le raccomandazioni del PRAC sono state trasmesse al Committee for Medicinal Products for Human Use (CHMP), responsabile di tutte le questioni concernenti i medicinali per uso umano, che ha adottato il parere definitivo dell'agenzia. Il parere del CHMP sarà ora trasmesso alla Commissione Europea, che emetterà una decisione definitiva a tempo debito. EMA/709120/2013 Page 5/5
Conclusioni scientifiche e motivi delle conclusioni
 Allegato II Conclusioni scientifiche e motivi della variazione dei termini delle autorizzazioni all immissione in commercio e spiegazione dettagliata delle differenze rispetto alla raccomandazione del
Allegato II Conclusioni scientifiche e motivi della variazione dei termini delle autorizzazioni all immissione in commercio e spiegazione dettagliata delle differenze rispetto alla raccomandazione del
DOMANDE E RISPOSTE SUI CONTRACCETTIVI ORMONALI COMBINATI: INFORMAZIONI AGGIORNATE PER LE DONNE
 DOMANDE E RISPOSTE SUI CONTRACCETTIVI ORMONALI COMBINATI: INFORMAZIONI AGGIORNATE PER LE DONNE Perché sono ora disponibili nuove informazioni? Un ampia recente revisione europea ha valutato i benefici
DOMANDE E RISPOSTE SUI CONTRACCETTIVI ORMONALI COMBINATI: INFORMAZIONI AGGIORNATE PER LE DONNE Perché sono ora disponibili nuove informazioni? Un ampia recente revisione europea ha valutato i benefici
CONTRACCETTIVI ORMONALI E RISCHIO DI COAGULI NEL SANGUE
 CONTRACCETTIVI ORMONALI E RISCHIO DI COAGULI NEL SANGUE Tutti questi farmaci sono contraccettivi ormonali combinati (COC): contengono un estrogeno (quasi sempre etinilestradiolo) e un progestinico In base
CONTRACCETTIVI ORMONALI E RISCHIO DI COAGULI NEL SANGUE Tutti questi farmaci sono contraccettivi ormonali combinati (COC): contengono un estrogeno (quasi sempre etinilestradiolo) e un progestinico In base
Il CMDh approva la restrizione dell uso di bromocriptina per bloccare la produzione di latte materno
 21 Agosto 2014 EMA/441377/2014 Il CMDh approva la restrizione dell uso di bromocriptina per bloccare la produzione di latte materno Il farmaco non deve essere usato abitualmente per prevenire o bloccare
21 Agosto 2014 EMA/441377/2014 Il CMDh approva la restrizione dell uso di bromocriptina per bloccare la produzione di latte materno Il farmaco non deve essere usato abitualmente per prevenire o bloccare
L EMA conferma le raccomandazioni per ridurre al minimo il rischio di PML, un infezione cerebrale, associato all uso di Tysabri
 25/04/2016 EMA/266665/2016 L EMA conferma le raccomandazioni per ridurre al minimo il rischio di PML, un infezione cerebrale, associato all uso di Tysabri Per i pazienti a più alto rischio è necessario
25/04/2016 EMA/266665/2016 L EMA conferma le raccomandazioni per ridurre al minimo il rischio di PML, un infezione cerebrale, associato all uso di Tysabri Per i pazienti a più alto rischio è necessario
26 luglio 2013 EMA/443003/ Westferry Circus Canary Wharf London E14 4HB United Kingdom
 26 luglio 2013 EMA/443003/2013 L Agenzia Europea dei Medicinali raccomanda modifiche nell uso dei medicinali a base di metoclopramide Le modifiche hanno l obiettivo principale di ridurre il rischio di
26 luglio 2013 EMA/443003/2013 L Agenzia Europea dei Medicinali raccomanda modifiche nell uso dei medicinali a base di metoclopramide Le modifiche hanno l obiettivo principale di ridurre il rischio di
I medici non devono più prescrivere medicinali contenenti calcitonina in forma di spray nasale per il trattamento dell'osteoporosi.
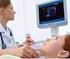 20 Luglio 2012 EMA/CHMP/483874/2012 L Agenzia Europea del Medicinali raccomanda la limitazione dell uso a lungo termine di medicinali a base di calcitonina Ritiro della formulazione intranasale per il
20 Luglio 2012 EMA/CHMP/483874/2012 L Agenzia Europea del Medicinali raccomanda la limitazione dell uso a lungo termine di medicinali a base di calcitonina Ritiro della formulazione intranasale per il
AIFA Agenzia Italiana del Farmaco Benfluorex
 AIFA - Benfluorex 18/12/2009 (Livello 2) AIFA Agenzia Italiana del Farmaco Benfluorex Comunicato EMEA Domande e Risposte (FAQ) file:///c /documenti/ben950.htm [18/12/2009 15.50.04] 18 December 2009 EMA/CHM/815033/2009
AIFA - Benfluorex 18/12/2009 (Livello 2) AIFA Agenzia Italiana del Farmaco Benfluorex Comunicato EMEA Domande e Risposte (FAQ) file:///c /documenti/ben950.htm [18/12/2009 15.50.04] 18 December 2009 EMA/CHM/815033/2009
Questa pagina contiene le risposte alle domande frequenti ricevute dall Agenzia europea per i medicinali.
 4 novembre 2011 EMA/527628/2011 Direzione Questa pagina contiene le risposte alle domande frequenti ricevute dall Agenzia europea per i medicinali. Se le risposte alle vostre domande non si trovano in
4 novembre 2011 EMA/527628/2011 Direzione Questa pagina contiene le risposte alle domande frequenti ricevute dall Agenzia europea per i medicinali. Se le risposte alle vostre domande non si trovano in
REPORT EUROPEO SULLA FARMACOVIGILANZA OTTOBRE 2012
 REPORT EUROPEO SULLA FARMACOVIGILANZA OTTOBRE 2012 COMITATO DI VALUTAZIONE DEI RISCHI PER LA FARMACOVIGILANZA (PHARMACOVIGILANCE RISK ASSESSMENT COMMITTEE: PRAC) Ordine del giorno della riunione tenutasi
REPORT EUROPEO SULLA FARMACOVIGILANZA OTTOBRE 2012 COMITATO DI VALUTAZIONE DEI RISCHI PER LA FARMACOVIGILANZA (PHARMACOVIGILANCE RISK ASSESSMENT COMMITTEE: PRAC) Ordine del giorno della riunione tenutasi
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA ITALIANA DEL FARMACO (AIFA) Gennaio 2014 Contraccettivi ormonali combinati: per essere consapevoli della differenza di rischio di tromboembolia tra
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA ITALIANA DEL FARMACO (AIFA) Gennaio 2014 Contraccettivi ormonali combinati: per essere consapevoli della differenza di rischio di tromboembolia tra
Guida per l utilizzo dei rapporti online fornisce
 Protezione della salute dei pazienti La presente guida per l utilizzo dei rapporti online fornisce informazioni sui campi di dati, sul formato, sulla corretta interpretazione e sulle funzionalità delle
Protezione della salute dei pazienti La presente guida per l utilizzo dei rapporti online fornisce informazioni sui campi di dati, sul formato, sulla corretta interpretazione e sulle funzionalità delle
La Commissione Europea prenderà la decisione finale legale
 25 Aprile 2014 EMA/240581/2014 CMDh sostiene la nuova raccomandazione per minimizzare il rischio di alterata capacità nella guida e ridotta prontezza mentale nel mattino successivo all assunzione di zolpidem
25 Aprile 2014 EMA/240581/2014 CMDh sostiene la nuova raccomandazione per minimizzare il rischio di alterata capacità nella guida e ridotta prontezza mentale nel mattino successivo all assunzione di zolpidem
EMA conferma le raccomandazioni per minimizzare il rischio di PML, un infezione del cervello, in seguito a utilizzo di Tysabri
 26 febbraio 2016 EMA/137488/2016 EMA conferma le raccomandazioni per minimizzare il rischio di PML, un infezione del cervello, in seguito a utilizzo di Tysabri Più frequenti scansioni di Risonanza Magnetica
26 febbraio 2016 EMA/137488/2016 EMA conferma le raccomandazioni per minimizzare il rischio di PML, un infezione del cervello, in seguito a utilizzo di Tysabri Più frequenti scansioni di Risonanza Magnetica
CONTRACCETTIVI ORMONALI E RISCHIO DI COAGULI NEL SANGUE
 CONTRACCETTIVI ORMONALI E RISCHIO DI COAGULI NEL SANGUE Tutti questi farmaci sono contraccettivi ormonali combinati (COC): contengono un estrogeno (quasi sempre etinilestradiolo) e un progestinico In base
CONTRACCETTIVI ORMONALI E RISCHIO DI COAGULI NEL SANGUE Tutti questi farmaci sono contraccettivi ormonali combinati (COC): contengono un estrogeno (quasi sempre etinilestradiolo) e un progestinico In base
DISPOSITIVI MEDICI RIUTILIZZABILI, IN ARRIVO REGOLAMENTO UE
 19-10-2013 DISPOSITIVI MEDICI RIUTILIZZABILI, IN ARRIVO REGOLAMENTO UE (ANSA) - ROMA, 18 OTT - Cateteri, protesi e peacemaker riutilizzabili, ma dietro accurata procedura. Sembra questo il futuro di molti
19-10-2013 DISPOSITIVI MEDICI RIUTILIZZABILI, IN ARRIVO REGOLAMENTO UE (ANSA) - ROMA, 18 OTT - Cateteri, protesi e peacemaker riutilizzabili, ma dietro accurata procedura. Sembra questo il futuro di molti
25 ottobre 2013 EMA/644345/ Westferry Circus Canary Wharf London E14 4HB United Kingdom
 25 ottobre 2013 EMA/644345/2013 L Agenzia Europea dei Medicinali conferma le modifiche nell uso dei medicinali a base di metoclopramide Le modifiche hanno l obiettivo principale di ridurre il rischio di
25 ottobre 2013 EMA/644345/2013 L Agenzia Europea dei Medicinali conferma le modifiche nell uso dei medicinali a base di metoclopramide Le modifiche hanno l obiettivo principale di ridurre il rischio di
RoActemra. tocilizumab. Che cos è RoActemra? Per che cosa si usa RoActemra? Riassunto destinato al pubblico
 EMA/18167/2014 EMEA/H/C/000955 Riassunto destinato al pubblico tocilizumab Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
EMA/18167/2014 EMEA/H/C/000955 Riassunto destinato al pubblico tocilizumab Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
Humira. adalimumab. Che cos è Humira? Per che cosa si usa Humira? Riassunto destinato al pubblico
 EMA/65420/2013 EMEA/H/C/000481 Riassunto destinato al pubblico adalimumab Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
EMA/65420/2013 EMEA/H/C/000481 Riassunto destinato al pubblico adalimumab Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
Nel caso del mieoloma multiplo, un tumore che colpisce un tipo di globuli bianchi detti cellule plasmatiche, Revlimid è usato:
 EMA/112959/2016 EMA/H/C/000717 Riassunto destinato al pubblico lenalidomide Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
EMA/112959/2016 EMA/H/C/000717 Riassunto destinato al pubblico lenalidomide Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
Raccomandazioni più stringenti sul rischio di gravi reazioni da ipersensibilità con Rienso (ferumoxitolo)*
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) 31gennaio 2014 Raccomandazioni più stringenti sul rischio di gravi reazioni da
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) 31gennaio 2014 Raccomandazioni più stringenti sul rischio di gravi reazioni da
Pradaxa è un medicinale contenente il principio attivo dabigatran etexilato. È disponibile in capsule (75, 110 e 150 mg).
 EMA/47517/2015 EMEA/H/C/000829 Riassunto destinato al pubblico dabigatran etexilato Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato
EMA/47517/2015 EMEA/H/C/000829 Riassunto destinato al pubblico dabigatran etexilato Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato
Humira. adalimumab. Che cos è Humira? Per che cosa si usa Humira? Riassunto destinato al pubblico
 EMA/722238/2012 EMEA/H/C/000481 Riassunto destinato al pubblico adalimumab Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
EMA/722238/2012 EMEA/H/C/000481 Riassunto destinato al pubblico adalimumab Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
Nuovo testo delle informazioni sul prodotto Estratti dalle raccomandazioni del PRAC in merito a segnali
 15 September 2016 EMA/PRAC/603534/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nuovo testo delle informazioni sul prodotto Estratti dalle raccomandazioni del PRAC in merito a segnali Adottato
15 September 2016 EMA/PRAC/603534/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nuovo testo delle informazioni sul prodotto Estratti dalle raccomandazioni del PRAC in merito a segnali Adottato
Il CMDh conferma le raccomandazioni sulla restrizione d uso dei medicinali a base di domperidone
 28 Aprile 2014 EMA/236452/2014 Il CMDh conferma le raccomandazioni sulla restrizione d uso dei medicinali a base di domperidone La Commissione Europea assumerà una decisione definitiva Il Gruppo di Coordinamento
28 Aprile 2014 EMA/236452/2014 Il CMDh conferma le raccomandazioni sulla restrizione d uso dei medicinali a base di domperidone La Commissione Europea assumerà una decisione definitiva Il Gruppo di Coordinamento
Il CMDh approva le raccomandazioni per restringere l uso dei medicinali contenenti diacereina
 21 March 2014 EMA/162540/2014 Il CMDh approva le raccomandazioni per restringere l uso dei medicinali contenenti diacereina Le restrizioni hanno lo scopo di limitare il rischio di diarrea grave e effetti
21 March 2014 EMA/162540/2014 Il CMDh approva le raccomandazioni per restringere l uso dei medicinali contenenti diacereina Le restrizioni hanno lo scopo di limitare il rischio di diarrea grave e effetti
vaccino pneumococcico polisaccaridico coniugato (13-valente, adsorbito)
 EMA/90006/2015 EMEA/H/C/001104 Riassunto destinato al pubblico vaccino pneumococcico polisaccaridico coniugato (13-valente, adsorbito) Questo è il riassunto della relazione pubblica europea di valutazione
EMA/90006/2015 EMEA/H/C/001104 Riassunto destinato al pubblico vaccino pneumococcico polisaccaridico coniugato (13-valente, adsorbito) Questo è il riassunto della relazione pubblica europea di valutazione
Nuovo testo delle informazioni sul prodotto Estratti dalle raccomandazioni del PRAC in merito a segnali
 25 February 2016 EMA/PRAC/137786/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nuovo testo delle informazioni sul prodotto Estratti dalle raccomandazioni del PRAC in merito a Adottato nella riunione
25 February 2016 EMA/PRAC/137786/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nuovo testo delle informazioni sul prodotto Estratti dalle raccomandazioni del PRAC in merito a Adottato nella riunione
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
Limitazioni d uso dei medicinali contenenti domperidone
 1 settembre 2014 EMA/465179/2014 Il 23 aprile 2014 il gruppo di coordinamento per le procedure di mutuo riconoscimento e decentrate - medicinali per uso umano (CMDh) ha approvato le raccomandazioni relative
1 settembre 2014 EMA/465179/2014 Il 23 aprile 2014 il gruppo di coordinamento per le procedure di mutuo riconoscimento e decentrate - medicinali per uso umano (CMDh) ha approvato le raccomandazioni relative
MabThera. rituximab. Che cos è MabThera? Per che cosa si usa MabThera? Riassunto destinato al pubblico
 EMA/614203/2010 EMEA/H/C/000165 Riassunto destinato al pubblico rituximab Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
EMA/614203/2010 EMEA/H/C/000165 Riassunto destinato al pubblico rituximab Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
Avastin è utilizzato con altri medicinali antitumorali per il trattamento dei seguenti tipi di cancro negli adulti:
 EMA/487904/2016 EMEA/H/C/000582 Riassunto destinato al pubblico bevacizumab Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
EMA/487904/2016 EMEA/H/C/000582 Riassunto destinato al pubblico bevacizumab Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
ESTMAR 150 MCG/20 MCG COMPRESSE ESTMAR 150 MCG/30 MCG COMPRESSE. Variazioni degli stampati relativamente agli aspetti della sicurezza
 FARMACOVIGILANZA ESTMAR 150 MCG/20 MCG COMPRESSE ESTMAR 150 MCG/30 MCG COMPRESSE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione
FARMACOVIGILANZA ESTMAR 150 MCG/20 MCG COMPRESSE ESTMAR 150 MCG/30 MCG COMPRESSE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione
MYWY 0,02 MG/3 MG COMPRESSE RIVESTITE CON FILM. Variazioni degli stampati relativamente agli aspetti della sicurezza
 FARMACOVIGILANZA MYWY 0,02 MG/3 MG COMPRESSE RIVESTITE CON FILM Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione V&A/P/77468
FARMACOVIGILANZA MYWY 0,02 MG/3 MG COMPRESSE RIVESTITE CON FILM Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono conseguenti alla Determinazione V&A/P/77468
Raccomandazioni d uso sui medicinali contenenti ibuprofene ad alte dosi
 22 Maggio 2015 EMA/325007/2015 Comunicato Stampa EMA Raccomandazioni d uso sui medicinali contenenti ibuprofene ad alte dosi La revisione conferma un lieve rischio cardiovascolare con dosaggi giornalieri
22 Maggio 2015 EMA/325007/2015 Comunicato Stampa EMA Raccomandazioni d uso sui medicinali contenenti ibuprofene ad alte dosi La revisione conferma un lieve rischio cardiovascolare con dosaggi giornalieri
Allegato III. Modifiche ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo
 Allegato III Modifiche ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Queste modifiche ai paragrafi pertinenti del Riassunto delle Caratteristiche
Allegato III Modifiche ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Queste modifiche ai paragrafi pertinenti del Riassunto delle Caratteristiche
GAZZETTA UFFICIALE DELLA REPUBBLICA ITALIANA Serie generale n. 115
 AGENZIA ITALIANA DEL FARMACO DETERMINAZIONE 9 Maggio 2007 Modifica degli stampati dei medicinali contenenti farmaci antinfiammatori non steroidei (FANS) non selettivi per uso sistemico - ATC M01A. omissis
AGENZIA ITALIANA DEL FARMACO DETERMINAZIONE 9 Maggio 2007 Modifica degli stampati dei medicinali contenenti farmaci antinfiammatori non steroidei (FANS) non selettivi per uso sistemico - ATC M01A. omissis
AIFA - Agenzia Italiana del Farmaco
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
Allegato II. Conclusioni scientifiche e motivi per il rifiuto presentati dall Agenzia europea per i medicinali
 Allegato II Conclusioni scientifiche e motivi per il rifiuto presentati dall Agenzia europea per i medicinali 5 Conclusioni scientifiche Riassunto generale della valutazione scientifica di etinilestradiolo-drospirenone
Allegato II Conclusioni scientifiche e motivi per il rifiuto presentati dall Agenzia europea per i medicinali 5 Conclusioni scientifiche Riassunto generale della valutazione scientifica di etinilestradiolo-drospirenone
Avastin è utilizzato con altri medicinali antitumorali per il trattamento dei seguenti tipi di tumore negli adulti:
 EMA/175824/2015 EMEA/H/C/000582 Riassunto destinato al pubblico bevacizumab Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
EMA/175824/2015 EMEA/H/C/000582 Riassunto destinato al pubblico bevacizumab Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
L Agenzia Europea dei Medicinali raccomanda di limitare l'uso di medicinali contenenti cilostazolo
 22 March 2013 EMA/98571/2013 L Agenzia Europea dei Medicinali raccomanda di limitare l'uso di medicinali contenenti cilostazolo Il Comitato Europeo per i Medicinali per uso Umano (CHMP) dell Agenzia, ha
22 March 2013 EMA/98571/2013 L Agenzia Europea dei Medicinali raccomanda di limitare l'uso di medicinali contenenti cilostazolo Il Comitato Europeo per i Medicinali per uso Umano (CHMP) dell Agenzia, ha
AIFA Agenzia Italiana del Farmaco Nuove Informazioni di Sicurezza Riguardanti le Eparine
 AIFA - Eparine 05/06/2008 (Livello 2) AIFA Agenzia Italiana del Farmaco Nuove Informazioni di Sicurezza Riguardanti le Eparine Comunicato Stampa EMEA Domande e Risposte sull'eparina file:///c /documenti/eppa100.htm
AIFA - Eparine 05/06/2008 (Livello 2) AIFA Agenzia Italiana del Farmaco Nuove Informazioni di Sicurezza Riguardanti le Eparine Comunicato Stampa EMEA Domande e Risposte sull'eparina file:///c /documenti/eppa100.htm
Revolade. eltrombopag. Che cos è Revolade? Per che cosa si usa Revolade? Riassunto destinato al pubblico
 EMA/33466/2016 EMEA/H/C/001110 Riassunto destinato al pubblico eltrombopag Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
EMA/33466/2016 EMEA/H/C/001110 Riassunto destinato al pubblico eltrombopag Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
Foglio illustrativo: informazioni per il paziente DUEVA compresse desogestrel + etinilestradiolo
 Foglio illustrativo: informazioni per il paziente DUEVA compresse desogestrel + etinilestradiolo Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni
Foglio illustrativo: informazioni per il paziente DUEVA compresse desogestrel + etinilestradiolo Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni
Salute della Donna Prevenzione delle complicanze trombotiche associate all uso di estro-progestinici in età riproduttiva
 CENTRO NAZIONALE DI EPIDEMIOLOGIA, SORVEGLIANZA E PROMOZIONE DELLA SALUTE VIALE REGINA ELENA, 299-00161 ROMA TEL. 0649904160- FAX 0649904170 Salute della Donna Prevenzione delle complicanze trombotiche
CENTRO NAZIONALE DI EPIDEMIOLOGIA, SORVEGLIANZA E PROMOZIONE DELLA SALUTE VIALE REGINA ELENA, 299-00161 ROMA TEL. 0649904160- FAX 0649904170 Salute della Donna Prevenzione delle complicanze trombotiche
Valproato t. Opuscolo Informativo per le Pazienti. Contiene informazioni importanti in merito ai rischio del valproato in gravidanza
 Valproato t Opuscolo Informativo per le Pazienti Se sei una ragazza o una donna che assume un medicinale contenente valproato, questo opuscolo è per te Contiene informazioni importanti in merito ai rischio
Valproato t Opuscolo Informativo per le Pazienti Se sei una ragazza o una donna che assume un medicinale contenente valproato, questo opuscolo è per te Contiene informazioni importanti in merito ai rischio
Protelos/Osseor (ranelato di stronzio): nuove informazioni di sicurezza dall EMEA
 PROTELOS : ATTENZIONE! L'azienda farmaceutica francese Servier è nell occhio del ciclone mediatico nel suo paese e in tutta Europa per un dossier dell'emea, in cui viene accusata di aver "nascosto alle
PROTELOS : ATTENZIONE! L'azienda farmaceutica francese Servier è nell occhio del ciclone mediatico nel suo paese e in tutta Europa per un dossier dell'emea, in cui viene accusata di aver "nascosto alle
RISK MANAGEMENT DEL PAZIENTE A RISCHIO TROMBOEMBOLICO
 PREVENZIONE DEL TROMBOEMBOLISMO VENOSO E UTILIZZO DELLA RELATIVA SCHEDA DI VALUTAZIONE: INTEGRAZIONE OSPEDALE-TERRITORIO RISK MANAGEMENT DEL PAZIENTE A RISCHIO TROMBOEMBOLICO ACIREALE 7 DICEMBRE 2013 GENERALITA
PREVENZIONE DEL TROMBOEMBOLISMO VENOSO E UTILIZZO DELLA RELATIVA SCHEDA DI VALUTAZIONE: INTEGRAZIONE OSPEDALE-TERRITORIO RISK MANAGEMENT DEL PAZIENTE A RISCHIO TROMBOEMBOLICO ACIREALE 7 DICEMBRE 2013 GENERALITA
Allegato III. Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo
 Allegato III Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo Nota: Il Riassunto delle caratteristiche del prodotto, l'etichettatura e il foglio
Allegato III Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo Nota: Il Riassunto delle caratteristiche del prodotto, l'etichettatura e il foglio
Progestinici orali (POPs) Progestinici iniettabili Progestinici impiantabili Progestinici intrauterini Progestinici transvaginali
 Contraccezione con solo progestinico Francesco Maria Primiero SAPIENZA UNIVERSITA DI ROMA Il progestinico è l elemento insostituibile della contraccezione ormonale Possibili vie di somministrazione Progestinici
Contraccezione con solo progestinico Francesco Maria Primiero SAPIENZA UNIVERSITA DI ROMA Il progestinico è l elemento insostituibile della contraccezione ormonale Possibili vie di somministrazione Progestinici
Criteri di eligibilita dei contraccettivi ormonali : linee guida a confronto. Daniela Spettoli
 Criteri di eligibilita dei contraccettivi ormonali : linee guida a confronto Daniela Spettoli Cosa sono i criteri di eligibilità risks medical conditions Criteri di eligibilità: quanto stringenti? choose
Criteri di eligibilita dei contraccettivi ormonali : linee guida a confronto Daniela Spettoli Cosa sono i criteri di eligibilità risks medical conditions Criteri di eligibilità: quanto stringenti? choose
Allegato II. Conclusioni scientifiche e motivi della variazione dei termini delle autorizzazioni all immissione in commercio
 Allegato II Conclusioni scientifiche e motivi della variazione dei termini delle autorizzazioni all immissione in commercio 20 Conclusioni scientifiche Riassunto generale della valutazione scientifica
Allegato II Conclusioni scientifiche e motivi della variazione dei termini delle autorizzazioni all immissione in commercio 20 Conclusioni scientifiche Riassunto generale della valutazione scientifica
Eylea. aflibercept. Che cos'è Eylea? Per che cosa si usa Eylea? Riassunto destinato al pubblico
 EMA/677928/2015 EMEA/H/C/002392 Riassunto destinato al pubblico aflibercept Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
EMA/677928/2015 EMEA/H/C/002392 Riassunto destinato al pubblico aflibercept Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
Foglio illustrativo: informazioni per l utilizzatore Yasmin 0,03 mg / 3 mg compresse rivestite con film Etinilestradiolo / Drospirenone
 Foglio illustrativo: informazioni per l utilizzatore Yasmin 0,03 mg / 3 mg compresse rivestite con film Etinilestradiolo / Drospirenone Legga attentamente questo foglio prima di prendere questo medicinale
Foglio illustrativo: informazioni per l utilizzatore Yasmin 0,03 mg / 3 mg compresse rivestite con film Etinilestradiolo / Drospirenone Legga attentamente questo foglio prima di prendere questo medicinale
PROBLEMATICHE GINECOLOGICHE NELLE PAZIENTI AFFETTE DA LAM STEFANO BIANCHI DIPARTIMENTO MATERNO-INFANTILE OSPEDALE SAN GIUSEPPE UNIVERSITA DI MILANO
 PROBLEMATICHE GINECOLOGICHE NELLE PAZIENTI AFFETTE DA LAM STEFANO BIANCHI DIPARTIMENTO MATERNO-INFANTILE OSPEDALE SAN GIUSEPPE UNIVERSITA DI MILANO PROBLEMATICHE GINECOLOGICHE NELLE PAZIENTI AFFETTE DA
PROBLEMATICHE GINECOLOGICHE NELLE PAZIENTI AFFETTE DA LAM STEFANO BIANCHI DIPARTIMENTO MATERNO-INFANTILE OSPEDALE SAN GIUSEPPE UNIVERSITA DI MILANO PROBLEMATICHE GINECOLOGICHE NELLE PAZIENTI AFFETTE DA
LISTA DI CONTROLLO PER I PRESCRITTORI - CONTRACCETTIVI ORMONALI COMBINATI
 LISTA DI CONTROLLO PER I PRESCRITTORI - CONTRACCETTIVI ORMONALI COMBINATI La preghiamo di utilizzare questa lista di controllo insieme al Riassunto delle Caratteristiche del Prodotto durante ogni consulto
LISTA DI CONTROLLO PER I PRESCRITTORI - CONTRACCETTIVI ORMONALI COMBINATI La preghiamo di utilizzare questa lista di controllo insieme al Riassunto delle Caratteristiche del Prodotto durante ogni consulto
DOTT.CARLO MAPELLI CENTRO MENOPAUSA OSPEDALE NIGUARDA RIUNIONE DI AGGIORNAMENTO LUGLIO 2011
 DOTT.CARLO MAPELLI CENTRO MENOPAUSA OSPEDALE NIGUARDA RIUNIONE DI AGGIORNAMENTO LUGLIO 2011 L endometriosi è una patologia ginecologica che interessa il 6-10% delle donne. E considerata una malattia cronica
DOTT.CARLO MAPELLI CENTRO MENOPAUSA OSPEDALE NIGUARDA RIUNIONE DI AGGIORNAMENTO LUGLIO 2011 L endometriosi è una patologia ginecologica che interessa il 6-10% delle donne. E considerata una malattia cronica
Caso clinico 3.1 1º step
 Caso clinico 3.1 1º step La signora Anna Maria di 53 anni vi riporta l esito degli accertamenti che le avevate prescritto in vista di una eventuale HRT. Sposata con due figli ha una anamnesi familiare
Caso clinico 3.1 1º step La signora Anna Maria di 53 anni vi riporta l esito degli accertamenti che le avevate prescritto in vista di una eventuale HRT. Sposata con due figli ha una anamnesi familiare
SCOMPENSO CARDIACO: QUESTIONARIO SUL GRADO DI CONOSCENZA DELLA MALATTIA
 SCOMPENSO CARDIACO: QUESTIONARIO SUL GRADO DI CONOSCENZA DELLA MALATTIA Gentile Sig.ra /Signore, le seguenti domande hanno lo scopo di verificare che cosa conosce della Sua malattia, della sua gestione
SCOMPENSO CARDIACO: QUESTIONARIO SUL GRADO DI CONOSCENZA DELLA MALATTIA Gentile Sig.ra /Signore, le seguenti domande hanno lo scopo di verificare che cosa conosce della Sua malattia, della sua gestione
Allegato III. Emendamenti alle sezioni pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio illustrativo
 Allegato III Emendamenti alle sezioni pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio illustrativo Nota: Il Riassunto delle Caratteristiche del Prodotto, l etichettatura e il foglio
Allegato III Emendamenti alle sezioni pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio illustrativo Nota: Il Riassunto delle Caratteristiche del Prodotto, l etichettatura e il foglio
La contraccezione d emergenza. a cura di Silvana Borsari
 La contraccezione d emergenza a cura di Silvana Borsari International Consortium for Emergency Contraception Cos è la Contraccezione d Emergenza (CE) Si tratta di una serie di metodi contraccettivi che
La contraccezione d emergenza a cura di Silvana Borsari International Consortium for Emergency Contraception Cos è la Contraccezione d Emergenza (CE) Si tratta di una serie di metodi contraccettivi che
Società Italiana di Medicina Generale. Incontro di Formazione Specifica. in Medicina Generale inerente problemi di sfera ostetrico-ginecologica
 Società Italiana di Medicina Generale Incontro di Formazione Specifica in Medicina Generale inerente problemi di sfera ostetrico-ginecologica Prima sessione compendio di casi clinici carta e penna Scaletta
Società Italiana di Medicina Generale Incontro di Formazione Specifica in Medicina Generale inerente problemi di sfera ostetrico-ginecologica Prima sessione compendio di casi clinici carta e penna Scaletta
 AGENZIA ITALIANA DEL FARMACO DETERMINA 5 febbraio 2016 Definizione del regime di fornitura e dei prescrittori per i medicinali a base di testosterone. (Determina n. 199/2016). (16A01493) (GU n.45 del 24-2-2016)
AGENZIA ITALIANA DEL FARMACO DETERMINA 5 febbraio 2016 Definizione del regime di fornitura e dei prescrittori per i medicinali a base di testosterone. (Determina n. 199/2016). (16A01493) (GU n.45 del 24-2-2016)
INFORMAZIONI IMPORTANTI SULLA CONTRACCEZIONE D EMERGENZA
 INFORMAZIONI IMPORTANTI SULLA CONTRACCEZIONE D EMERGENZA CHE COS È LA CONTRACCEZIONE D EMERGENZA? Questo opuscolo contiene informazioni importanti sulla contraccezione d emergenza. Le consigliamo, inoltre,
INFORMAZIONI IMPORTANTI SULLA CONTRACCEZIONE D EMERGENZA CHE COS È LA CONTRACCEZIONE D EMERGENZA? Questo opuscolo contiene informazioni importanti sulla contraccezione d emergenza. Le consigliamo, inoltre,
Allegato II. Conclusioni scientifiche e motivi del parere positivo presentati dall Agenzia europea per i medicinali
 Allegato II Conclusioni scientifiche e motivi del parere positivo presentati dall Agenzia europea per i medicinali 4 Conclusioni scientifiche Riassunto generale della valutazione scientifica di Seasonique
Allegato II Conclusioni scientifiche e motivi del parere positivo presentati dall Agenzia europea per i medicinali 4 Conclusioni scientifiche Riassunto generale della valutazione scientifica di Seasonique
COUMADIN 5 mg compresse warfarin sodico
 COUMADIN 5 mg compresse warfarin sodico Prima di prendere la medicina legga attentamente questo foglietto. Si ricordi che il medico ha prescritto questa medicina solo a lei: non la dia mai a nessun altro.
COUMADIN 5 mg compresse warfarin sodico Prima di prendere la medicina legga attentamente questo foglietto. Si ricordi che il medico ha prescritto questa medicina solo a lei: non la dia mai a nessun altro.
Raccomandazioni PRAC sui segnali per l aggiornamento delle informazioni sul prodotto
 22 gennaio 2015 EMA/PRAC/63310/2015 Comitato per la valutazione dei rischi nell ambito della farmacovigilanza Raccomandazioni PRAC sui segnali per l aggiornamento delle informazioni sul prodotto Adottate
22 gennaio 2015 EMA/PRAC/63310/2015 Comitato per la valutazione dei rischi nell ambito della farmacovigilanza Raccomandazioni PRAC sui segnali per l aggiornamento delle informazioni sul prodotto Adottate
ALLEGATO III MODIFICHE DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO E DEL FOGLIO ILLUSTRATIVO
 ALLEGATO III MODIFICHE DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO E DEL FOGLIO ILLUSTRATIVO 41 MODIFICHE DA INCLUDERE NEI PARAGRAFI PERTINENTI DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO DELLE
ALLEGATO III MODIFICHE DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO E DEL FOGLIO ILLUSTRATIVO 41 MODIFICHE DA INCLUDERE NEI PARAGRAFI PERTINENTI DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO DELLE
Nota Informativa Importante. Guida alla Terapia per i Paziente. Guida alla Contraccezione. Modulo d'informazione e Consenso Informato
 AIFA - Isotretinoina 16/03/2009 (Livello 2) AIFA Agenzia Italiana del Farmaco Isotretinoina Nota Informativa Importante Nuove Modalita' di Prescrizione per i Medicinali Contenenti Isotretinoina ad Uso
AIFA - Isotretinoina 16/03/2009 (Livello 2) AIFA Agenzia Italiana del Farmaco Isotretinoina Nota Informativa Importante Nuove Modalita' di Prescrizione per i Medicinali Contenenti Isotretinoina ad Uso
LA TERAPIA MEDICA DELL ENDOMETRIOSI
 LA TERAPIA MEDICA DELL ENDOMETRIOSI A cura del Dott. Massimiliano Monti Medico Chirurgo, Specialista in Ostetricia e Ginecologia Consultorio AIED, La Spezia Premessa L'endometriosi è una malattia in costante
LA TERAPIA MEDICA DELL ENDOMETRIOSI A cura del Dott. Massimiliano Monti Medico Chirurgo, Specialista in Ostetricia e Ginecologia Consultorio AIED, La Spezia Premessa L'endometriosi è una malattia in costante
Sessualità nella donna
 encathopedia Sessualità nella donna con lesione midollare Contraccezione Sessualità Fertilità Con il contributo della dottoressa Lorita Cito Fertilità Una lesione al midollo spinale non compromette la
encathopedia Sessualità nella donna con lesione midollare Contraccezione Sessualità Fertilità Con il contributo della dottoressa Lorita Cito Fertilità Una lesione al midollo spinale non compromette la
Foglio illustrativo: Informazioni per l utilizzatore
 Foglio illustrativo: Informazioni per l utilizzatore KIPLING 75 microgrammi/30 microgrammi compresse rivestite gestodene/etinilestradiolo MEDICINALE EQUIVALENTE Cose importanti da sapere sui contraccettivi
Foglio illustrativo: Informazioni per l utilizzatore KIPLING 75 microgrammi/30 microgrammi compresse rivestite gestodene/etinilestradiolo MEDICINALE EQUIVALENTE Cose importanti da sapere sui contraccettivi
Foglio illustrativo: informazioni per l utilizzatore
 Foglio illustrativo: informazioni per l utilizzatore Enciela 60 microgrammi/24 ore + 13 microgrammi/24 ore cerotto transdermico gestodene/ etinilestradiolo Medicinale sottoposto a monitoraggio addizionale.
Foglio illustrativo: informazioni per l utilizzatore Enciela 60 microgrammi/24 ore + 13 microgrammi/24 ore cerotto transdermico gestodene/ etinilestradiolo Medicinale sottoposto a monitoraggio addizionale.
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE. Yasmin 0,03 mg / 3 mg compresse rivestite con film Etinilestradiolo / Drospirenone
 FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE Yasmin 0,03 mg / 3 mg compresse rivestite con film Etinilestradiolo / Drospirenone Legga attentamente questo foglio illustrativo prima di prendere questo
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE Yasmin 0,03 mg / 3 mg compresse rivestite con film Etinilestradiolo / Drospirenone Legga attentamente questo foglio illustrativo prima di prendere questo
Per una Medicina Condivisa. Dott.ssa Elena Fachinat 2 aprile 2011
 Per una Medicina Condivisa Dott.ssa Elena Fachinat 2 aprile 2011 Per una Medicina Condivisa SULL EFFICACIA DI UNA TERAPIA SULLA SICUREZZA DI UNA TERAPIA SULL INUTILITA DI UNA TERAPIA CON LA DONNA IN GRAVIDANZA
Per una Medicina Condivisa Dott.ssa Elena Fachinat 2 aprile 2011 Per una Medicina Condivisa SULL EFFICACIA DI UNA TERAPIA SULLA SICUREZZA DI UNA TERAPIA SULL INUTILITA DI UNA TERAPIA CON LA DONNA IN GRAVIDANZA
Foglio illustrativo: informazioni per l utilizzatore. ARIANNA 60 microgrammi/15 microgrammi, compresse rivestite con film Gestodene/Etinilestradiolo
 Foglio illustrativo: informazioni per l utilizzatore ARIANNA 60 microgrammi/15 microgrammi, compresse rivestite con film Gestodene/Etinilestradiolo Legga attentamente questo foglio prima di prendere questo
Foglio illustrativo: informazioni per l utilizzatore ARIANNA 60 microgrammi/15 microgrammi, compresse rivestite con film Gestodene/Etinilestradiolo Legga attentamente questo foglio prima di prendere questo
Quali sono le novità nella terapia ormonale sostitutiva nell insufficienza delle ghiandole surrenaliche?
 ANDREA GIUSTINA Direttore Cattedra Endocrinologia Università degli Studi di Brescia Quali sono le novità nella terapia ormonale sostitutiva nell insufficienza delle ghiandole surrenaliche? Come da determinazione
ANDREA GIUSTINA Direttore Cattedra Endocrinologia Università degli Studi di Brescia Quali sono le novità nella terapia ormonale sostitutiva nell insufficienza delle ghiandole surrenaliche? Come da determinazione
AIFA - Agenzia Italiana del Farmaco
 Giugno 2013 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Limitazioni all uso di TROBALT (retigabina) il trattamento può comportare
Giugno 2013 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Limitazioni all uso di TROBALT (retigabina) il trattamento può comportare
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO. Medicinale non più autorizzato
 ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori
ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 Medicinale sottoposto a monitoraggio addizionale. Ciò permetterà la rapida identificazione di nuove informazioni sulla sicurezza. Agli operatori
Allegato III. Modifiche attinenti i paragrafi del riassunto delle caratteristiche del prodotto e del foglio illustrativo
 Allegato III Modifiche attinenti i paragrafi del riassunto delle caratteristiche del prodotto e del foglio illustrativo 39 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 40 Paragrafo 4.1. Indicazioni terapeutiche
Allegato III Modifiche attinenti i paragrafi del riassunto delle caratteristiche del prodotto e del foglio illustrativo 39 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 40 Paragrafo 4.1. Indicazioni terapeutiche
COMITATO ETICO Modulo informativo-consenso informato tipo riguardante i rischi della donna in gravidanza arruolata in una sperimentazione clinica
 COMITATO ETICO In data 05-05-2014 il Comitato Etico ha approvato la stesura definitiva del Modulo informativo-consenso informato tipo riguardante i rischi della donna in gravidanza arruolata in una sperimentazione
COMITATO ETICO In data 05-05-2014 il Comitato Etico ha approvato la stesura definitiva del Modulo informativo-consenso informato tipo riguardante i rischi della donna in gravidanza arruolata in una sperimentazione
MEET THE EXPERT SCELTA DEL CONTRACCETTIVO ORMONALE E MONITORAGGIO DELLA TERAPIA
 MEET THE EXPERT SCELTA DEL CONTRACCETTIVO ORMONALE E MONITORAGGIO DELLA TERAPIA ROBERTO CASTELLO Medicina Generale/Endocrinologia Azienda Ospedaliera Universitaria di Verona VINCENZO TOSCANO Dipartimento
MEET THE EXPERT SCELTA DEL CONTRACCETTIVO ORMONALE E MONITORAGGIO DELLA TERAPIA ROBERTO CASTELLO Medicina Generale/Endocrinologia Azienda Ospedaliera Universitaria di Verona VINCENZO TOSCANO Dipartimento
Le raccomandazioni della Conferenza di consenso di Torino giugno 2008
 Le raccomandazioni della Conferenza di consenso di Torino giugno 2008 Comitato Promotore: Progetto PartecipaSalute (Istituto Mario Negri, Centro Cochrane Italiano, Agenzia Zadig) e Sistema Nazionale Linee
Le raccomandazioni della Conferenza di consenso di Torino giugno 2008 Comitato Promotore: Progetto PartecipaSalute (Istituto Mario Negri, Centro Cochrane Italiano, Agenzia Zadig) e Sistema Nazionale Linee
Foglio illustrativo: Informazioni per l utilizzatore. KLAIRA compresse rivestite con film Estradiolo valerato / Dienogest
 Foglio illustrativo: Informazioni per l utilizzatore KLAIRA compresse rivestite con film Estradiolo valerato / Dienogest Legga attentamente questo foglio prima di prendere questo medicinale perché contiene
Foglio illustrativo: Informazioni per l utilizzatore KLAIRA compresse rivestite con film Estradiolo valerato / Dienogest Legga attentamente questo foglio prima di prendere questo medicinale perché contiene
L assistenza al post partum Silvia Vaccari
 Presentazione della linea guida Prevenzione e trattamento della emorragia del post partum Sistema nazionale linee guida Roma, 25.09.09 L assistenza al post partum Silvia Vaccari Roma 24 ottobre 2016 Aula
Presentazione della linea guida Prevenzione e trattamento della emorragia del post partum Sistema nazionale linee guida Roma, 25.09.09 L assistenza al post partum Silvia Vaccari Roma 24 ottobre 2016 Aula
Olbia,17 marzo 2012 Paola Bianchi. Vantaggi e rischi della contraccezione nella donna con diabete: presentazione del documento AMD.
 Olbia,17 marzo 2012 Paola Bianchi Vantaggi e rischi della contraccezione nella donna con diabete: presentazione del documento AMD. Caratteristiche del contraccettivo Alta qualità dei servizi informazione
Olbia,17 marzo 2012 Paola Bianchi Vantaggi e rischi della contraccezione nella donna con diabete: presentazione del documento AMD. Caratteristiche del contraccettivo Alta qualità dei servizi informazione
Zoely. MSD Merck Sharp & Dohme AG. Pagina 1. Informazione destinata ai pazienti del Compendio svizzero dei medicamenti. OOMed
 Zoely MSD Merck Sharp & Dohme AG OOMed Che cos è Zoely e quando si usa? Zoely è un medicamento utilizzato per la contraccezione ormonale (la cosiddetta «pillola») per la prevenzione della gravidanza nelle
Zoely MSD Merck Sharp & Dohme AG OOMed Che cos è Zoely e quando si usa? Zoely è un medicamento utilizzato per la contraccezione ormonale (la cosiddetta «pillola») per la prevenzione della gravidanza nelle
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE. Effiprev 2 mg/0,03 mg compresse rivestite con film dienogest ed etinilestradiolo
 FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE Effiprev 2 mg/0,03 mg compresse rivestite con film dienogest ed etinilestradiolo MEDICINALE EQUIVALENTE Cose importanti da sapere sui contraccettivi
FOGLIO ILLUSTRATIVO: INFORMAZIONI PER L UTILIZZATORE Effiprev 2 mg/0,03 mg compresse rivestite con film dienogest ed etinilestradiolo MEDICINALE EQUIVALENTE Cose importanti da sapere sui contraccettivi
gestodene + etinilestradiolo
 gestodene + etinilestradiolo FEDRA 0,075 mg + 0,02 mg compresse rivestite Legga attentamente questo foglio prima di prendere questo medicinale. Conservi questo foglio illustrativo. Potrebbe aver bisogno
gestodene + etinilestradiolo FEDRA 0,075 mg + 0,02 mg compresse rivestite Legga attentamente questo foglio prima di prendere questo medicinale. Conservi questo foglio illustrativo. Potrebbe aver bisogno
Fedra Mori UOC Endocrinologia Ospedale Sant Andrea Roma. Bari, 7-10 novembre 2013
 Fedra Mori UOC Endocrinologia Ospedale Sant Andrea Roma Bari, Cancro della mammella Bari, Il cancro della mammella è una neoplasia ormono-sensibile Nel mondo è la seconda causa di morte dopo il tumore
Fedra Mori UOC Endocrinologia Ospedale Sant Andrea Roma Bari, Cancro della mammella Bari, Il cancro della mammella è una neoplasia ormono-sensibile Nel mondo è la seconda causa di morte dopo il tumore
La contraccezione in adolescenza: nuovi orientamenti nella consulenza contraccettiva.
 La contraccezione in adolescenza: nuovi orientamenti nella consulenza contraccettiva. Drssa Cinzia Melchiorri Spazio Giovani Consultorio Familiare AUSL Imola Il rischio di gravidanza indesiderata nelle
La contraccezione in adolescenza: nuovi orientamenti nella consulenza contraccettiva. Drssa Cinzia Melchiorri Spazio Giovani Consultorio Familiare AUSL Imola Il rischio di gravidanza indesiderata nelle
Foglio illustrativo: informazioni per l utilizzatore. Egogyn 0,150 mg + 0,030 mg compresse rivestite levonorgestrel + etinilestradiolo
 Foglio illustrativo: informazioni per l utilizzatore Egogyn 0,150 mg + 0,030 mg compresse rivestite levonorgestrel + etinilestradiolo Legga attentamente questo foglio prima di usare questo medicinale perché
Foglio illustrativo: informazioni per l utilizzatore Egogyn 0,150 mg + 0,030 mg compresse rivestite levonorgestrel + etinilestradiolo Legga attentamente questo foglio prima di usare questo medicinale perché
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 DENOMINAZIONE DEL MEDICINALE GRACIAL compresse 2 COMPOSIZIONE QUALITATIVA E QUANTITATIVA ciascuna compressa di colore blu contiene 0,025 mg di desogestrel
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1 DENOMINAZIONE DEL MEDICINALE GRACIAL compresse 2 COMPOSIZIONE QUALITATIVA E QUANTITATIVA ciascuna compressa di colore blu contiene 0,025 mg di desogestrel
Acido acetilsalicilico Sandoz 100 mg compresse gastroresistenti Acido acetilsalicilico Medicinale equivalente
 Acido acetilsalicilico Sandoz 100 mg compresse gastroresistenti Acido acetilsalicilico Medicinale equivalente Acido acetilsalicilico Sandoz Page 1 of 4 1. Che cos'è Acido acetilsalicilico Sandoz e a che
Acido acetilsalicilico Sandoz 100 mg compresse gastroresistenti Acido acetilsalicilico Medicinale equivalente Acido acetilsalicilico Sandoz Page 1 of 4 1. Che cos'è Acido acetilsalicilico Sandoz e a che
Foglio illustrativo: informazioni per l utilizzatore. Azalia 75 microgrammi compresse rivestite con film Desogestrel
 Foglio illustrativo: informazioni per l utilizzatore Azalia 75 microgrammi compresse rivestite con film Desogestrel Legga attentamente questo foglio prima di prendere questo medicinale perché contiene
Foglio illustrativo: informazioni per l utilizzatore Azalia 75 microgrammi compresse rivestite con film Desogestrel Legga attentamente questo foglio prima di prendere questo medicinale perché contiene
ELEONORA ZAFFARONI Clinica Ostetrica e Ginecologica di Varese Universita degli Studi dell Insubria
 APPROCCIO RAZIONALE ALLA PRESCRIZIONE DELLA TERAPIA CONTRACCETTIVA ORMONALE ELEONORA ZAFFARONI Clinica Ostetrica e Ginecologica di Varese Universita degli Studi dell Insubria La Contraccezione Ormonale
APPROCCIO RAZIONALE ALLA PRESCRIZIONE DELLA TERAPIA CONTRACCETTIVA ORMONALE ELEONORA ZAFFARONI Clinica Ostetrica e Ginecologica di Varese Universita degli Studi dell Insubria La Contraccezione Ormonale
Allegato III. Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo
 Allegato III Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Gli emendamenti al riassunto delle caratteristiche del prodotto e al foglio
Allegato III Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Gli emendamenti al riassunto delle caratteristiche del prodotto e al foglio
Foglio illustrativo: informazioni per l utilizzatore. SIBILLA 2 mg/0,03 mg compresse rivestite con film
 Foglio illustrativo: informazioni per l utilizzatore SIBILLA 2 mg/0,03 mg compresse rivestite con film Dienogest/Etinilestradiolo Medicinale equivalente Cose importanti da sapere sui contraccettivi ormonali
Foglio illustrativo: informazioni per l utilizzatore SIBILLA 2 mg/0,03 mg compresse rivestite con film Dienogest/Etinilestradiolo Medicinale equivalente Cose importanti da sapere sui contraccettivi ormonali
Il cerotto transdermico*, contraccettivo combinato che si applica una volta alla settimana, è più vantaggioso dei contraccettivi orali combinati?
 Il cerotto transdermico*, contraccettivo combinato che si applica una volta alla settimana, è più vantaggioso dei contraccettivi orali combinati? FA Sonnenberg, CG Hagerty, MJ Price, C Neslusan INTRODUZIONE
Il cerotto transdermico*, contraccettivo combinato che si applica una volta alla settimana, è più vantaggioso dei contraccettivi orali combinati? FA Sonnenberg, CG Hagerty, MJ Price, C Neslusan INTRODUZIONE
Foglio illustrativo: informazioni per l utilizzatore. NOVADIEN 2 mg/0,03 mg compresse rivestite con film
 Foglio illustrativo: informazioni per l utilizzatore NOVADIEN 2 mg/0,03 mg compresse rivestite con film Dienogest/Etinilestradiolo Medicinale equivalente Cose importanti da sapere sui contraccettivi ormonali
Foglio illustrativo: informazioni per l utilizzatore NOVADIEN 2 mg/0,03 mg compresse rivestite con film Dienogest/Etinilestradiolo Medicinale equivalente Cose importanti da sapere sui contraccettivi ormonali
