Le reazioni chimiche biologiche e gli enzimi
|
|
|
- Maria Bello
- 7 anni fa
- Visualizzazioni
Transcript
1 Le reazioni chimiche biologiche e gli enzimi LEZIONE NR. 6 - PSICOBIOLOGIA
2 Le reazioni chimiche consistono in interazioni interatomiche che si svolgono a livello dei loro orbitali, e quindi differenti dalle reazioni nucleari (fusione e fissione) che coinvolgono i cambiamenti a livello del nucleo degli atomi. Nel caso delle molecole biologiche, le reazioni chimiche avvengono in genere fra atomi appartenenti a due molecole differenti, anche se nel caso delle macromolecole è possibile che avvengano reazioni chimiche fra atomi che la compongono. Come tutti i fenomeni fisici del nostro universo, anche le reazioni chimiche biologiche devono obbedire ai principi della termodinamica.
3 1) La quantità totale di energia di un sistema e di un ambiente che lo circonda, rimane sempre costante di conseguenza, qualsiasi siano le trasformazioni che coinvolgono il sistema a l ambiente, non ci sarà mai ne distruzione ne creazione di energia. 2) Tutte le trasformazioni energetiche sono SEMPRE accompagnate dalla dissipazione nell ambiente, sotto forma di calore, di una parte dell energia libera ovvero l energia utilizzabile per compiere un lavoro. Questo fenomeno viene misurato in accordo col concetto di entropia = disordine. Questo implica che un qualsiasi sistema e l ambiente che lo circonda, vedranno sempre l entropia aumentare e l energia libera diminuire. Tuttavia la materia vivente è in grado di controllare i flussi e la direzione di energia libera che vengono scambiati con l ambiente.
4 Assumendo continuamente sostanze in grado di fornire energia: Organismi fotosintetici Organismi chemiosintetici Organismi eterotrofi
5 Trattenendo all interno del corpo il calore che dovrebbe essere dissipato verso l esterno: Piumaggio Pelo Strato adiposo
6 In cosa consistono le reazioni chimiche nello specifico? Immagine 3.1 Basi biologiche Esse sono riarrangiamenti atomici conseguenti ad urti fra le molecole. Infatti un impatto fra due o più molecole, denominati reagenti genera energia cinetica che può anche essere utilizzata come energia chimica atta a rompere i legami delle molecole reagenti ed a formarne di nuovi con diverse conformazioni dando vita a nuove molecole chiamate prodotti.
7 Ovviamente non tutti gli impatti fra molecole danno vita a reazioni chimiche. Affinché ciò avvenga è necessario che i reagenti si urtino fra loro in maniera appropriata. Immagine 3.2 Basi biologiche - Giusto posizionamento relativo - Giusta velocità Se questi parametri sono corretti, forniscono congiuntamente la giusta energia di attivazione
8 Tipologie di reazioni chimiche
9 Caratteristiche delle reazioni chimiche Ogni reazione chimica ha delle precise caratteristiche che bisogna aver presente: Velocità della reazione Energia della reazione Direzione della reazione
10 Velocità Questa viene misurata in quantità di molecole di prodotto che vengono prodotte in ogni unità di tempo. Es. 0,05 moli/minuto oppure moli/secondo. La velocità dipende in massima parte da due parametri: Temperatura in genere l aumento di calore accelera la probabilità che due molecole impattino Concentrazione maggiore è la quantità di molecole in un solvente più è probabile che si incontrino Es. Rettili oppure la febbre
11 Energia Essa è misurabile confrontando il contenuto energetico dei prodotti con il contenuto energetico dei reagenti. Se il contenuto energetico dei prodotti < reagenti, si parla di reazione esoergonica o spontanea. L energia fluisce dai reagenti all ambiente. Se il contenuto energetico dei prodotti > reagenti, si parla di reazione endoergonica o indotta. L energia fluisce dall ambiente ai reagenti. Immagine 3.3 Basi biologiche
12 Esempio concreto: Cambio di livello di masse d acqua. Se dobbiamo portare l acqua da un livello inferiore ad uno superiore. Servirà energia che sarà divisa in due parti: 1. L energia effettivamente necessaria a spostare l acqua (secchi, idropompa) 2. Energia persa sotto forma di calore (calore che si genera nel corpo umano per fatica, o nell idropompa per attrito ingranaggi) Reazione endoergonica
13 Esempio concreto: Cambio di livello di masse d acqua. La caduta dell acqua da un livello superiore ad uno inferiore è un fenomeno spontaneo che genera energia cinetica che a sua volta sarà divisa in due parti: 1. Una parte che potrà essere utilizzata per un lavoro (ruota di un mulino) 2. Energia persa sotto forma di calore (calore che si genera sui massi sul fondo della cascata) Reazione esoergonica
14 La soglia di attivazione Nonostante come detto, alcune reazioni chimiche possano essere spontanee, questo negli organismi biologici avviene molto raramente. Es. le molecole del nostro corpo non si trasformano in CO 2 ed H 2 O nonostante questa trasformazione dal punto di vista esoergonico sia molto favorevole. Immagine 3.4 Basi biologiche Questo avviene perché anche le reazioni esoergoniche hanno bisogno di una iniziale somministrazione di energia, che verrà poi interamente restituita durante la reazione chimica. Es. bruciare un foglio di carta
15 Direzione Ciò che definisce una molecola come reagente o viceversa come prodotto è la direzione entro la quale la reazione chimica avviene. Le molecole collidono e l energia che ne deriva, forma uno stato intermedio chiamato complesso attivato che ha due possibili vie di evoluzione Portare a termine la reazione (condizione energetica più stabile) Regredire alla condizione iniziale (condizione energetica più stabile) Pertanto una reazione chimica è teoricamente sempre reversibile. E la direzione in cui essa procederà dipende da molti fattori, il più importante fra i quali è la concentrazione dei reagenti rispetto a quella dei prodotti.
16 Direzione
17 La reazione chimica nelle cellule organiche La probabilità di inizio e la velocità di una reazione chimica, come detto in precedenza, dipendono dalla temperatura e dalla concentrazione. Tuttavia le cellule non hanno la possibilità di modificare autonomamente e facilmente tali parametri. Per questa ragione, l evoluzione ha dotato gli organismi di catalizzatori che hanno il compito di abbassare la soglia di attivazione di ciascuna reazione, in modo tale che i reagenti che presentano il contenuto energetico adatto a dare il via alla reazione, aumenti. Tali sostanze: 1) Si legano in modo altamente specifico ai reagenti di una data reazione chimica, abbassandone la soglia di attivazione. 2) Non entrano a far parte della reazione e non ne determinano la direzione di svolgimento 3) Non si «consumano» nel corso della reazione, e quindi al termine tornano nuovamente disponibili per ulteriori cicli di reazioni.
18 A parte il caso dei ribozimi (molecole di RNA, coinvolte in alcune fasi di trascrizione e traduzione) i catalizzatori biologici sono sempre delle proteine, denominate enzimi. Gli enzimi sono proteine in grado di riconoscere in modo specifico come reagenti determinate molecole così da poter dare il via a determinate reazioni chimiche. In genere il nome dell enzima dipende dalla reazione chimica che andrà a catalizzare, definita dalla desinenza -asi (es. DNA-polimerasi).
19 La capacità degli enzimi di catalizzare le reazioni chimiche nella materia vivente, dipende in gran parte dal fatto che essendo proteine, sono contraddistinti da una forma tridimensionale data loro dalla struttura terziaria (o quaternaria). Questa struttura consente di avere varie regioni dell enzima che possono interagire in maniera reversibile o stabile con i reagenti (substrato), con fattori che regolano la funzione enzimatica o che ne dirigono la localizzazione intra-cellulare. Immagine 3.8 Basi biologiche In particolare ogni enzima ha una regione chiamata sito attivo che media il riconoscimento stereo-specifico dell enzima, con il substrato. L insieme dell enzima e del substrato, forma il complesso ES
20 Un valido modello di spiegazione dell interazione fra enzima e substrato è stato offerto da Fisher all inizio del XX secolo, ed è stato definito modello chiave serratura. Tale modello spiega come gli enzimi possano avere diversi gradi di specificità nei confronti delle molecole substrato. Alta specificità, accoglie quasi interamente le molecole del substrato. Questo fa in modo che solo e solamente quelle molecole riescano a legarsi all enzima, dando il via alla reazione chimica. Bassa specificità, accoglie solo una porzione dell intera molecola del substrato. Questo fa in modo che molecole diverse fra loro, ma con una parte in comune, che riesce a legarsi all enzima, possano dare il via alla reazione chimica.
21 Il ruolo del complesso enzima-substrato è quello di abbassare la soglia di attivazione della reazione. Questo avviene poiché l enzima mantiene fermi i reagenti in una posizione favorevole, nella quale la maggior parte degli urti fra le loro molecole, riesce a dare il via alla reazione. In conclusione, la presenza di un enzima, consente alla reazione chimica di svolgersi ad elevata velocità minimizzando l energia necessaria per il suo innesco. Immagine 3.9 Basi biologiche
22 Tuttavia, come detto in precedenza l enzima può dare il via alla reazione chimica ma non ne può influenzare la direzione. Ciò vuol dire che la regola esposta in precedenza circa la concentrazione di reagenti e prodotti, rimane valida e che il complesso ES, come risultato potrà avere la formazione dei prodotti, ma anche il ritorno ai singoli reagenti. Per ovviare a tale problema, gli enzimi dopo aver legato a loro i reagenti, vanno incontro ad un cambiamento conformazionale che può portare con più probabilità alla formazione dei prodotti. Immagine 3.10 Basi biologiche
23 La regolazione enzimatica Talvolta il sito attivo, oltre ad ospitare i reagenti, può anche ospitare altre molecole chiamate inibitori enzimatici. Si tratta di molecole molto simili a quelle che creano il normale substrato dell enzima, ma che creano un diverso complesso chiamato E-I. A differenza dei reagenti, gli inibitori non vengono trasformati in prodotti dalla reazione chimica. In alcuni casi gli inibitori sono presenti nella cellula e vengono utilizzate da queste ultime per regolare l attività enzimatica. Più frequentemente queste sostanze vengono introdotte dall esterno dell organismo (farmaci o sostanze velenose). Immagine 3.11 Basi biologiche
24 Acido acetilsalicilico, derivato artificiale di acido salicilico, presente nella corteccia e nelle foglie del salice. È un inibitore degli enzimi ciclo-ossigenasi 1 e 2 che catalizzano le prostaglandine che danno inizio alla risposta infiammatoria. In particolare l aspirina diminuisce la produzione delle prostaglandine a livello dell ipotalamo che è il centro regolatore di tutta la temperatura corporea.
25 Gli inibitori enzimatici inoltre si possono classificare in inibitori competitivi e non competitivi. Sulla base della stabilità del complesso E-I che essi formano. Se il complesso E-I è instabile, dopo breve tempo si romperà liberando nuovamente l enzima che avrà il sito attivo libero di accogliere nuovamente un altra molecola. Se la molecola è un reagente avrà inizio la reazione, se è un inibitore, l enzima sarà bloccato ancora una volta temporaneamente. La probabilità del nuovo legame, dipende come sempre dalla concentrazione dei reagenti o degli inibitori (per tale ragione questi inibitori vengono definiti competitivi). A causa della loro bassa tossicità gli inibitori competitivi sono il principio attivo di molti farmaci utilizzati per l uomo. Se il complesso E-I è stabile. L enzima viene attivato in maniera permanente e l unico rimedio che la cellula ha di attivare nuove reazioni chimiche utili è quella di sintetizzare nuovi enzimi. Immagine 3.12 Basi biologiche A causa della elevata tossicità, gli inibitori non-competitivi, sono frequenti componenti dei veleni rilasciati da animali o piante.
26 Abbiamo visto che gli enzimi possono essere inattivati in maniera reversibile o irreversibile. Ma questi possono anche essere attivati, consentendo così alla cellula di regolarne le funzioni. Ma in cosa consistono di preciso tali regolazioni? In genere sono quasi tutte modificazioni post-traduzione. Ve ne sono di 6 tipologie. E possono agire in maniera singola, contemporanea o sequenziale su ogni enzima. 1) Attivazione mediante taglio proteolitico 2) Attivazione mediante unione con un cofattore 3) Assemblaggio di sub-unità 4) Traslocazione intracellulare 5) Attivazione/Inattivazione mediante cambiamento delle cariche elettriche 6) Regolazione allosterica
27 1) Attivazione mediante taglio proteolitico 2) Attivazione mediante unione con un cofattore 3) Assemblaggio di sub-unità 4) Traslocazione intracellulare 5) Attivazione/Inattivazione mediante cambiamento delle cariche elettriche 6) Regolazione allosterica La cellula genera un pro-enzima inattivo, che diventerà attivo solo a seguito del taglio di una parte della sua catena polipeptidica. Molti enzimi della catalisi proteolitica del tubo digerente funzionano in questo modo.
28 1) Attivazione mediante taglio proteolitico 2) Attivazione mediante unione con un cofattore 3) Assemblaggio di sub-unità 4) Traslocazione intracellulare 5) Attivazione/Inattivazione mediante cambiamento delle cariche elettriche 6) Regolazione allosterica In questo caso l enzima non si attiva solo dopo l unione con i reagenti, ma è necessario che vi si leghi anche un cofattore. Ad esempio nel neurone, l enzima PKA (proteinchinasi A), implicato nei processi di trasduzione del segnale, viene attivato dal legame con il nucleotide camp (AMP ciclico)
29 1) Attivazione mediante taglio proteolitico 2) Attivazione mediante unione con un cofattore 3) Assemblaggio di sub-unità 4) Traslocazione intracellulare 5) Attivazione/Inattivazione mediante cambiamento delle cariche elettriche 6) Regolazione allosterica Singole sub-unità, ognuna delle quali inattiva vengono unite fra loro per formare l enzima completo che diverrà attivo. Un esempio a livello dei neuroni è rappresentato dall enzima adenilato ciclasi che produce il camp partendo dall ATP. Di per sé questo enzima è inattivo, ma quando gli viene assemblata una subunità alpha s, presa dalla proteina G che gli è accanto, allora l enzima si attiva.
30 1) Attivazione mediante taglio proteolitico 2) Attivazione mediante unione con un cofattore 3) Assemblaggio di sub-unità 4) Traslocazione intracellulare 5) Attivazione/Inattivazione mediante cambiamento delle cariche elettriche 6) Regolazione allosterica La molecola enzimatica viene trasportata da un sito intracellulare nel quale non poteva essere attiva, ad un secondo sito intracellulare nella quale può esplicare la propria funzione Es. gli enzimi della fosforilazione ossidativa iniziano a funzionare dopo essere stati trasportati nei mitocondri.
31 1) Attivazione mediante taglio proteolitico 2) Attivazione mediante unione con un cofattore 3) Assemblaggio di sub-unità 4) Traslocazione intracellulare 5) Attivazione/Inattivazione mediante cambiamento delle cariche elettriche 6) Regolazione allosterica Vengono aggiunti o sottratti gruppi funzionali carichi dal punto di vista elettrico, come i gruppi fosfati. Troviamo quindi nuovamente i processi di fosforilazione e defosforilazione che in genere riguardano gli amminoacidi serina, treonina o tirosina. Es. proteinchinasi o fosfatasi.
32 1) Attivazione mediante taglio proteolitico 2) Attivazione mediante unione con un cofattore 3) Assemblaggio di sub-unità 4) Traslocazione intracellulare 5) Attivazione/Inattivazione mediante cambiamento delle cariche elettriche 6) Regolazione allosterica Riguarda una particolare tipologia di enzimi (in genere metabolici) che sulla loro superfice oltre ad avere il sito attivo che accoglie il substrato, hanno anche un secondo sito di legame, chiamato per l appunto sito allosterico che lega gli effettori allosterici che possono essere distinti in: Immagine 3.13 Basi biologiche Inibitori allosterici Attivatori allosterici L azione di queste seconde molecole di ligando, può essere esplicata solo se il sito attivo è libero e viceversa, per via dei cambiamenti conformazionali indotti da entrambi i legami.
33 1) Attivazione mediante taglio proteolitico 2) Attivazione mediante unione con un cofattore 3) Assemblaggio di sub-unità 4) Traslocazione intracellulare 5) Attivazione/Inattivazione mediante cambiamento delle cariche elettriche 6) Regolazione allosterica Enzima chiave Esempio di catena metabolica Regolazione a feed-back Immagine 3.14 Basi biologiche Diventa inibitore allosterico dell enzima chiave
34 Abbiamo visto come gli enzimi vengono regolati. Tuttavia fra l enorme quantità di enzimi che sono presenti nelle cellule del nostro organismo, ve ne sono alcuni che non vengono regolati. Ciò vuol dire che alla cellula basta produrre quel determinato enzima per ottenere in modo automatico i prodotti della reazione chimica che andrà a catalizzare l enzima in questione. In poche parole agisce come un interruttore ON/OFF Tali enzimi vengono definiti come dotati di attività costitutiva Un esempio concreto è rappresentato dai neuroni catecolaminergici. Alcuni fra questi neuroni possono sintetizzare un enzima chiamato dopamina-b-idrossilasi, che catalizza una trasformazione della dopamina in noradrenalina, e vengono quindi detti neuroni noradrenergici. Altri neuroni non codificano questo enzima, e quindi non avviene questa reazione la dopamina rimane dopamina ed i neuroni vengono definiti dopaminergici.
BIOLOGIA GENERALE 19 dicembre 2006
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 19 dicembre 2006 Facoltà di Psicologia Corso di Laurea in Scienze e Tecniche di Psicologia Generale e Sperimentale
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 19 dicembre 2006 Facoltà di Psicologia Corso di Laurea in Scienze e Tecniche di Psicologia Generale e Sperimentale
ENZIMI. Durante la reazione l enzima può essere temporaneamente modificato ma alla fine del processo ritorna nel suo stato originario, un enzima viene
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
CLASSIFICAZIONE O.T.I.L.Is. Lig
 GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
Funzioni dei nucleotidi
 Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
REGOLAZIONE DELL ATTIVITA ENZIMATICA 1) MODULAZIONE ALLOSTERICA NON-COVALENTE (REVERSIBILE)
 REGOLAZIONE DELL ATTIVITA ENZIMATICA - Regolazione a lungo termine: la quantità di enzima può essere controllata regolando la velocità della sua sintesi o degradazione (minuti o ore) - Regolazione a breve
REGOLAZIONE DELL ATTIVITA ENZIMATICA - Regolazione a lungo termine: la quantità di enzima può essere controllata regolando la velocità della sua sintesi o degradazione (minuti o ore) - Regolazione a breve
Esempi di funzioni svolte dalle proteine
 Esempi di funzioni svolte dalle proteine Trasporto di sostanze Esempi di funzioni svolte dalle proteine Trasporto di sostanze Funzioni strutturali Esempi di funzioni svolte dalle proteine Trasporto di
Esempi di funzioni svolte dalle proteine Trasporto di sostanze Esempi di funzioni svolte dalle proteine Trasporto di sostanze Funzioni strutturali Esempi di funzioni svolte dalle proteine Trasporto di
ENZIMI. Un enzima è un catalizzatore (acceleratore) di reazioni biologiche.
 ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
BIOCHIMICA APPLICATA e CLINICA
 BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre
 Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre molecole, anche chimicamente simili al substrato. Saturabilità:
Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre molecole, anche chimicamente simili al substrato. Saturabilità:
Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi)
 ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
Energia per la vita Bibliografia I colori della biologia Giusti- Gatti- Anelli Pearson Ed.
 Energia per la vita Bibliografia I colori della biologia Giusti- Gatti- Anelli Pearson Ed. Ogni alimento che ingeriamo viene scomposto attraverso i processi digestivi nelle sue molecole costituenti come
Energia per la vita Bibliografia I colori della biologia Giusti- Gatti- Anelli Pearson Ed. Ogni alimento che ingeriamo viene scomposto attraverso i processi digestivi nelle sue molecole costituenti come
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
TRASDUZIONE DEL SEGNALE CELLULARE
 TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre
 Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre cellule (contatto cellula-cellula) o con strutture extracellulari
Una risposta cellulare specifica può essere determinata dalla presenza di mediatori chimici (ormoni o altre molecole), dall interazione con altre cellule (contatto cellula-cellula) o con strutture extracellulari
INTRODUZIONE AL METABOLISMO. dal gr. metabolè = trasformazione
 INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
INTRODUZIONE AL METABOLISMO dal gr. metabolè = trasformazione IL Metabolismo Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in una cellula o in un organismo. E costituito da
Regolazione enzimatica Isoenzimi
 Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Le reazioni esoergoniche e quelle endoergoniche del metabolismo cellulare sono legate dalla molecola di ATP.
 1 METABOLISMO CELLULARE Definizione Metabolismo cellulare insieme delle reazioni che producono e necessitano energia nel nostro corpo. Nel metabolismo si distinguono due fasi: Fase catabolica Insieme delle
1 METABOLISMO CELLULARE Definizione Metabolismo cellulare insieme delle reazioni che producono e necessitano energia nel nostro corpo. Nel metabolismo si distinguono due fasi: Fase catabolica Insieme delle
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 15 La termodinamica e la cinetica 1. Le reazioni producono energia 2. Il primo principio della
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 15 La termodinamica e la cinetica 1. Le reazioni producono energia 2. Il primo principio della
INTRODUZIONE ALLA BIOCHIMICA
 INTRODUZIONE ALLA BIOCHIMICA Sistema vivente sistema complesso ed altamente organizzato dotato di una composizione chimica determinata e unica grazie a tale composizione chimica al suo interno si formano
INTRODUZIONE ALLA BIOCHIMICA Sistema vivente sistema complesso ed altamente organizzato dotato di una composizione chimica determinata e unica grazie a tale composizione chimica al suo interno si formano
REGOLAZIONE ENZIMATICA
 REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
Capitolo 5 L energia e il trasporto
 Capitolo 5 L energia e il trasporto La cellula e l energia 5.1 L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità
Capitolo 5 L energia e il trasporto La cellula e l energia 5.1 L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità
La termodinamica studia i flussi/trasformazioni di energia. Bioenergetica: termodinamica applicata ai sistemi biologici
 LA CAPACITÀ DI USARE ENERGIA È CARATTERISTICA DEI SISTEMI VIVENTI Bisogni degli esseri viventi: Energia (luce, molecole organiche) Catalizzatori biologici (enzimi) La termodinamica studia i flussi/trasformazioni
LA CAPACITÀ DI USARE ENERGIA È CARATTERISTICA DEI SISTEMI VIVENTI Bisogni degli esseri viventi: Energia (luce, molecole organiche) Catalizzatori biologici (enzimi) La termodinamica studia i flussi/trasformazioni
Mediatore chimico. Recettore. Trasduzione del segnale. Risposta della cellula
 Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Energia e metabolismi energetici
 Energia e metabolismi energetici L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità di effettuare un lavoro L energia
Energia e metabolismi energetici L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità di effettuare un lavoro L energia
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
Helena Curtis N. Sue Barnes LA FOTOSINTESI INDICE Organismi autotrofi ed eterotrofi Confronto tra fotosintesi e respirazione Reazioni endoergoniche ed esoergoniche Reazioni accoppiate Fase luce-dipendente
Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi.
 ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
L ATP E L ENERGIA LA CHIMICA DELLA VITA GSCATULLO
 L ATP E L ENERGIA LA CHIMICA DELLA VITA GSCATULLO ( L ATP e l energia L energia Energia e reazioni chimiche Una reazione chimica avviene quando gli atomi possiedono energia a sufficiente a combinarsi tra
L ATP E L ENERGIA LA CHIMICA DELLA VITA GSCATULLO ( L ATP e l energia L energia Energia e reazioni chimiche Una reazione chimica avviene quando gli atomi possiedono energia a sufficiente a combinarsi tra
Il trasporto del glucosio
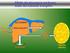 Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
Il trasporto del glucosio Il glucosio non può diffondere direttamente nelle cellule Esso entra nelle cellule mediante due meccanismi di trasporto: a) diffusione facilitata Na + indipendente b) co-trasporto
Termodinamica ENTALPIA...6
 Termodinamica ORGANISMI PRIMO VIVENTI ED ENERGIA...2 PRINCIPIO DELLA TERMODINAMICA...5 ENTALPIA...6 SECONDO PRINCIPIO DELLA TERMODINAMICA... 7 energia libera di Gibbs (G)...9 Variazione di energia libera
Termodinamica ORGANISMI PRIMO VIVENTI ED ENERGIA...2 PRINCIPIO DELLA TERMODINAMICA...5 ENTALPIA...6 SECONDO PRINCIPIO DELLA TERMODINAMICA... 7 energia libera di Gibbs (G)...9 Variazione di energia libera
Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia. a.a
 Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia a.a. 2016-17 Cinetica Chimica studia i fenomeni connessi con la VELOCITA di una REAZIONE Reazioni
Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia a.a. 2016-17 Cinetica Chimica studia i fenomeni connessi con la VELOCITA di una REAZIONE Reazioni
INTRODUZIONE AL METABOLISMO
 INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
INTRODUZIONE AL METABOLISMO METABOLISMO Il metabolismo (dal greco metabolé = trasformazione) è il complesso delle reazioni chimiche coordinate ed integrate che avvengono in una cellula. Il metabolismo
Le trasformazioni chimiche e fisiche della materia. Lezioni d'autore di Giorgio Benedetti
 Le trasformazioni chimiche e fisiche della materia Lezioni d'autore di Giorgio Benedetti INTRODUZIONE (I) VIDEO INTRODUZIONE (II) La comprensione delle proprietà delle sostanze e le trasformazioni che
Le trasformazioni chimiche e fisiche della materia Lezioni d'autore di Giorgio Benedetti INTRODUZIONE (I) VIDEO INTRODUZIONE (II) La comprensione delle proprietà delle sostanze e le trasformazioni che
Le molecole biologiche. Le proteine
 Le molecole biologiche Le proteine Le proteine sono macromolecole che costituiscono la maggior parte delle strutture cellulari ed extra-cellulari Così come nel caso di lipidi e carboidrati, anch esse
Le molecole biologiche Le proteine Le proteine sono macromolecole che costituiscono la maggior parte delle strutture cellulari ed extra-cellulari Così come nel caso di lipidi e carboidrati, anch esse
BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA
 Cap.15 BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA I Legge della Termodinamica: Il contenuto energetico dell
Cap.15 BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA I Legge della Termodinamica: Il contenuto energetico dell
catabolismo anabolismo
 Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in un organismo o in una cellula Il catabolismo è l insieme delle reazioni che portano alla scissione di molecole complesse (ricche
Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in un organismo o in una cellula Il catabolismo è l insieme delle reazioni che portano alla scissione di molecole complesse (ricche
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
Lo scopo della biochimica è la comprensione della vita in termini molecolari.
 Lo scopo della biochimica è la comprensione della vita in termini molecolari. Sebbene la biochimica venga spesso descritta come una scienza della vita e il suo sviluppo venga messo in relazione con la
Lo scopo della biochimica è la comprensione della vita in termini molecolari. Sebbene la biochimica venga spesso descritta come una scienza della vita e il suo sviluppo venga messo in relazione con la
Lezione 1: Atomi e molecole:
 Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
Lezione 1: Atomi e molecole: La materia è costituita da elementi chimici in forma pura o in combinazioni dette composti. La vita richiede circa 25 elementi chimici. La struttura atomica determina il comportamento
MACROMOLECOLE. Polimeri (lipidi a parte)
 MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 20 La velocità di reazione 3 Sommario 1. Che cos è la velocità di reazione 2. L equazione cinetica 3. Gli altri fattori che influiscono
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 20 La velocità di reazione 3 Sommario 1. Che cos è la velocità di reazione 2. L equazione cinetica 3. Gli altri fattori che influiscono
 http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
Unità fondamentale di tutti gli organismi viventi.
 La cellula Unità fondamentale di tutti gli organismi viventi. Cellula procariote Cellula animale Cellula vegetale Le cellule procariote e eucariote Cellula procariote Cellula eucariote Cromosomi Membrana
La cellula Unità fondamentale di tutti gli organismi viventi. Cellula procariote Cellula animale Cellula vegetale Le cellule procariote e eucariote Cellula procariote Cellula eucariote Cromosomi Membrana
LE MOLECOLE BIOLOGICHE
 LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
Capitolo 6 La respirazione cellulare
 Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Capitolo 6 La respirazione cellulare Introduzione alla respirazione cellulare 6.1 La respirazione polmonare rifornisce le nostre cellule di ossigeno ed elimina diossido di carbonio La respirazione polmonare
Energia di attivazione
 Energia di attivazione La maggior parte delle reazioni chimiche avviene con un apporto iniziale di energia per poter prendere l avvio procedere alla giusta velocità. Questo vale per le reazioni esoergoniche
Energia di attivazione La maggior parte delle reazioni chimiche avviene con un apporto iniziale di energia per poter prendere l avvio procedere alla giusta velocità. Questo vale per le reazioni esoergoniche
Il metabolismo cellulare
 Il metabolismo cellulare L obesità è problema sanitario e sociale Tessuto adiposo bianco e bruno È tutta una questione di energia: Se si assumono più molecole energetiche di quelle che ci servono per costruire
Il metabolismo cellulare L obesità è problema sanitario e sociale Tessuto adiposo bianco e bruno È tutta una questione di energia: Se si assumono più molecole energetiche di quelle che ci servono per costruire
Io Non sono un recettore!
 I recettori portano il messaggio extracellulare direttamente nel citoplasma (recettori di membrana) o nel nucleo (recettori nucleari) Io Non sono un recettore! È essenziale per la loro sopravvivenza che
I recettori portano il messaggio extracellulare direttamente nel citoplasma (recettori di membrana) o nel nucleo (recettori nucleari) Io Non sono un recettore! È essenziale per la loro sopravvivenza che
Catalisi. Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A Modulo di Biologia Strutturale
 Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Catalisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie
Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Catalisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie
NADH e NADPH. ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente)
 NADH e NADPH ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente) NADH e NADPH non sono funzionalmente intercambiabili. [NAD + ]/[NADH] ~ 1000 favorisce ossidazione [NADP
NADH e NADPH ATP = 1 moneta (energetica) della cellula NADH, NADPH = 2 moneta (potere riducente) NADH e NADPH non sono funzionalmente intercambiabili. [NAD + ]/[NADH] ~ 1000 favorisce ossidazione [NADP
LE PROTEINE SINTESI PROTEICA. funzione delle proteine nel nostro organismo
 LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
Lo schema più semplice di intervento di un catalizzatore C nella reazione fra due composti A e B è il seguente:
 Un catalizzatore è una sostanza (un elemento o un composto) in grado di modificare la velocità di una reazione chimica senza essere consumato alla fine della reazione stessa, rendendo possibili reazioni
Un catalizzatore è una sostanza (un elemento o un composto) in grado di modificare la velocità di una reazione chimica senza essere consumato alla fine della reazione stessa, rendendo possibili reazioni
METABOLISMO CELLULARE
 METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
METABOLISMO CELLULARE Struttura dell ATP (Adenosintrifosfato) Adenina (base azotata), Ribosio (zucchero) e un gruppo fosforico ATP Il legame covalente tra i gruppi fosforici si spezza facilmente liberando
ISTITUTO D ISTRUZIONE SECONDARIA SUPERIORE GIAN TOMMASO GIORDANI MONTE SANT ANGELO PROGRAMMA SVOLTO DURANTE L ANNO SCOLASTICO 2015/2016
 ISTITUTO D ISTRUZIONE SECONDARIA SUPERIORE GIAN TOMMASO GIORDANI MONTE SANT ANGELO PROGRAMMA SVOLTO DURANTE L ANNO SCOLASTICO 2015/2016 DISCIPLINA D INSEGNAMENTO SCIENZE: BIOLOGIA CHIMICA CLASSE III LICEO
ISTITUTO D ISTRUZIONE SECONDARIA SUPERIORE GIAN TOMMASO GIORDANI MONTE SANT ANGELO PROGRAMMA SVOLTO DURANTE L ANNO SCOLASTICO 2015/2016 DISCIPLINA D INSEGNAMENTO SCIENZE: BIOLOGIA CHIMICA CLASSE III LICEO
Enzimi: catalizzatori biologici
 Enzimi: catalizzatori biologici praticamente tutte le reazioni biochimiche della chimica della vita sono catalizzate da enzimi gli enzimi sono proteine la velocità di reazioni enzimatiche è aumentata di
Enzimi: catalizzatori biologici praticamente tutte le reazioni biochimiche della chimica della vita sono catalizzate da enzimi gli enzimi sono proteine la velocità di reazioni enzimatiche è aumentata di
2 INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA
 INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA 1 INTRODUZIONE 1 L energia chimica Esistono diversi tipi di energia e una tra queste è l energia chimica: un tipo di energia che possiedono tutte le molecole
INCONTRO: LA PRODUZIONE DI ENERGIA NELLA CELLULA 1 INTRODUZIONE 1 L energia chimica Esistono diversi tipi di energia e una tra queste è l energia chimica: un tipo di energia che possiedono tutte le molecole
VELOCITA DI REAZIONE
 VELOCITA DI REAZIONE Analogamente alla velocità di un corpo (velocità = distanza percorsa / tempo impiegato) la velocità di reazione è definita come la variazione di concentrazione dei prodotti o dei reagenti
VELOCITA DI REAZIONE Analogamente alla velocità di un corpo (velocità = distanza percorsa / tempo impiegato) la velocità di reazione è definita come la variazione di concentrazione dei prodotti o dei reagenti
I Lincei per una nuova didattica nella Scuola: una rete nazionale Polo di Brescia
 I Lincei per una nuova didattica nella Scuola: una rete nazionale Polo di Brescia Edizione 2016-2017 Metabolismo: equilibrio e omeostasi dei processi cellulari Lezione: Le principali vie metaboliche, il
I Lincei per una nuova didattica nella Scuola: una rete nazionale Polo di Brescia Edizione 2016-2017 Metabolismo: equilibrio e omeostasi dei processi cellulari Lezione: Le principali vie metaboliche, il
Elementi sistemati nella TAVOLA PERIODICA DEGLI ELEMENTI in base al numero atomico crescente O, H, N, C (+ del 96% della materia vivente)
 OVERVIEW Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi
OVERVIEW Atomo: più piccola porzione di un elemento che mantiene le proprietà chimiche dello stesso Teoria atomica e tavola periodica Legami e interazioni degli atomi Acqua e le sue proprietà Acidi e basi
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Laboratorio Fitness & Wellness
 Laboratorio Fitness & Wellness Anno Accademico 2015/2016 Ewan Thomas, MSc Principi di Bioenergetica e Biomeccanica Metabolismo Catabolismo Processi di degradazione che permettono di liberare energia Anabolismo
Laboratorio Fitness & Wellness Anno Accademico 2015/2016 Ewan Thomas, MSc Principi di Bioenergetica e Biomeccanica Metabolismo Catabolismo Processi di degradazione che permettono di liberare energia Anabolismo
L energia negli esseri viventi: fotosintesi e respirazione viste dal punto di vista chimico
 Dipartimento di Scienze Chimiche e Geologiche L energia negli esseri viventi: fotosintesi e respirazione viste dal punto di vista chimico Gianantonio Battistuzzi La fotosintesi e la respirazione aerobica
Dipartimento di Scienze Chimiche e Geologiche L energia negli esseri viventi: fotosintesi e respirazione viste dal punto di vista chimico Gianantonio Battistuzzi La fotosintesi e la respirazione aerobica
Fonte diretta di Energia è l ATP.
 Una cellula compie tre tipi di lavoro: -Lavoro meccanico: movimenti muscolari.. -Lavoro di trasporto: trasporto contro gradiente -Lavoro chimico: assemblaggio di polimeri da monomeri Fonte diretta di Energia
Una cellula compie tre tipi di lavoro: -Lavoro meccanico: movimenti muscolari.. -Lavoro di trasporto: trasporto contro gradiente -Lavoro chimico: assemblaggio di polimeri da monomeri Fonte diretta di Energia
LA CHIMICA DELLA VITA
 LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
Il metabolismo: concetti di base
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Il metabolismo: concetti di base Caratteristiche generali Strategie Trofiche Il metabolismo:
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Il metabolismo: concetti di base Caratteristiche generali Strategie Trofiche Il metabolismo:
FORMAZIONE DEL LEGAME PEPTIDICO
 AMINOACIDI FORMAZIONE DEL LEGAME PEPTIDICO SEQUENZA AMINOACIDICA DELL INSULINA STRUTTURA SECONDARIA DELLE PROTEINE STRUTTURA TERZIARIA DELLE PROTEINE STRUTTURA QUATERNARIA DELLE PROTEINE Definizione Processi
AMINOACIDI FORMAZIONE DEL LEGAME PEPTIDICO SEQUENZA AMINOACIDICA DELL INSULINA STRUTTURA SECONDARIA DELLE PROTEINE STRUTTURA TERZIARIA DELLE PROTEINE STRUTTURA QUATERNARIA DELLE PROTEINE Definizione Processi
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30)
 TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
fornire energia chimica in vettori attivati ATP e NADH e NADPH e FADH.
 Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
Cibo ed Energia Il glucosio e altre molecole nutritive per esempio i grassi vengono demolite attraverso un ossidazione graduale controllata per fornire energia chimica in una forma utilizzabile dalla cellula,
La chimica della vita
 La chimica della vita Ogni organismo vivente è una macchina sofisticata, risultato di un complesso insieme di reazioni chimiche. La costruzione e il funzionamento di questa macchina si devono all'esistenza
La chimica della vita Ogni organismo vivente è una macchina sofisticata, risultato di un complesso insieme di reazioni chimiche. La costruzione e il funzionamento di questa macchina si devono all'esistenza
DOGMA CENTRALE DELLA BIOLOGIA. Secondo il dogma centrale della biologia, il DNA dirige la. sintesi del RNA che a sua volta guida la sintesi delle
 DOGMA CENTRALE DELLA BIOLOGIA Secondo il dogma centrale della biologia, il DNA dirige la sintesi del RNA che a sua volta guida la sintesi delle proteine. Tuttavia il flusso unidirezionale di informazioni
DOGMA CENTRALE DELLA BIOLOGIA Secondo il dogma centrale della biologia, il DNA dirige la sintesi del RNA che a sua volta guida la sintesi delle proteine. Tuttavia il flusso unidirezionale di informazioni
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Tirosin chinasi senza o con funzione recettoriale
 Tirosin chinasi senza o con funzione recettoriale elica di poliprolina Il dominio chinasico di Src è mantenuto nello stato inattivo mediante due distinte interazioni intramolecolari: il legame del dominio
Tirosin chinasi senza o con funzione recettoriale elica di poliprolina Il dominio chinasico di Src è mantenuto nello stato inattivo mediante due distinte interazioni intramolecolari: il legame del dominio
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Glycogen Synthesis Glicogeno sintesi UTP UDP + 2 P i glycogen (n) + glucose-1-p glycogen (n + 1) Glycogen Phosphorylase P i Glicogeno lisi
 Glycogen Synthesis Glicogeno sintesi UTP UDP + 2 P i glycogen (n) + glucose-1-p glycogen (n + 1) Glycogen Phosphorylase P i Glicogeno lisi Se entrambe le vie fossero attive simultaneamente nella cellula
Glycogen Synthesis Glicogeno sintesi UTP UDP + 2 P i glycogen (n) + glucose-1-p glycogen (n + 1) Glycogen Phosphorylase P i Glicogeno lisi Se entrambe le vie fossero attive simultaneamente nella cellula
Meccanismi effettori dei linfociti T citotossici
 Meccanismi effettori dei linfociti T citotossici Immunità specifica: caratteristiche generali Immunità umorale - Riconoscimento dell antigene mediante anticorpi - Rimozione patogeni e tossine extracellulari
Meccanismi effettori dei linfociti T citotossici Immunità specifica: caratteristiche generali Immunità umorale - Riconoscimento dell antigene mediante anticorpi - Rimozione patogeni e tossine extracellulari
Il metabolismo cellulare
 Il metabolismo cellulare 1 Il metabolismo cellulare CATABOLISMO Processo esoergonico (per produrre energia) Nutriliti NAD FAD NADP e - +H + ANABOLISMO Processo endoergonico Biopolimeri (x es. proteine)
Il metabolismo cellulare 1 Il metabolismo cellulare CATABOLISMO Processo esoergonico (per produrre energia) Nutriliti NAD FAD NADP e - +H + ANABOLISMO Processo endoergonico Biopolimeri (x es. proteine)
Depuratore Biologico anaerobica con produzione di metano (CH4) da decomposizione organica
 Brevetti Depuratore Biologico anaerobica con produzione di metano (CH4) da decomposizione organica Depuratore Biologico anaerobica con produzione di metano (CH4) da decomposizione organica Committente:
Brevetti Depuratore Biologico anaerobica con produzione di metano (CH4) da decomposizione organica Depuratore Biologico anaerobica con produzione di metano (CH4) da decomposizione organica Committente:
Gerard Tortora, Brian Derrickson. Conosciamo
 1 Gerard Tortora, Brian Derrickson Conosciamo il corpo umano Capitolo 1 L organizzazione del corpo umano 1. Che cosa sono l anatomia e la fisiologia 2. I livelli di organizzazione e gli apparati del corpo
1 Gerard Tortora, Brian Derrickson Conosciamo il corpo umano Capitolo 1 L organizzazione del corpo umano 1. Che cosa sono l anatomia e la fisiologia 2. I livelli di organizzazione e gli apparati del corpo
Il livello cellulare di organizzazione: la struttura cellulare. Cattedra di Fisiologia Umana
 Il livello cellulare di organizzazione: la struttura cellulare Cattedra di Fisiologia Umana 1. La diversità delle cellule nel corpo umano Le cellule del corpo hanno molte differenti forme ed una varietà
Il livello cellulare di organizzazione: la struttura cellulare Cattedra di Fisiologia Umana 1. La diversità delle cellule nel corpo umano Le cellule del corpo hanno molte differenti forme ed una varietà
Ruolo del calcio nella cellula
 Ruolo del calcio nella cellula I meccanismi evolutivi hanno attribuito agli ioni fosfato un importanza fondamentale poiché sono necessari per sintetizzare ATP. Per questo motivo la loro concentrazione
Ruolo del calcio nella cellula I meccanismi evolutivi hanno attribuito agli ioni fosfato un importanza fondamentale poiché sono necessari per sintetizzare ATP. Per questo motivo la loro concentrazione
PIANO DI LAVORO ANNUALE
 PIANO DI LAVORO ANNUALE Classe 5D2 A.S. 2015/2016 Disciplina: CHIMICA ORGANICA E BIOCHIMICA Docente: prof.ssa Palma Elena Ore settimanali: 4 (2 laboratorio) Libro di testo: Rippa, Ricciotti La chimica
PIANO DI LAVORO ANNUALE Classe 5D2 A.S. 2015/2016 Disciplina: CHIMICA ORGANICA E BIOCHIMICA Docente: prof.ssa Palma Elena Ore settimanali: 4 (2 laboratorio) Libro di testo: Rippa, Ricciotti La chimica
Nucleotidi 20/12/2013. Nucleotidi (1) Ribosio Vs. Desossirbosio
 I Nucleotidi Hanno Tre Componenti Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Nucleotidi (1) Ribosio Vs. Desossirbosio Un Nucleotide è una molecola costituita da un
I Nucleotidi Hanno Tre Componenti Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Nucleotidi (1) Ribosio Vs. Desossirbosio Un Nucleotide è una molecola costituita da un
costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più
 Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
Il flusso e la regolazione dell informazione genica. Lezione nr. 8 Psicobiologia
 Il flusso e la regolazione dell informazione genica Lezione nr. 8 Psicobiologia L informazione che viene trascritta non riguarda tutto il DNA ma solo delle particolari sequenze definite GENI. Tipologie
Il flusso e la regolazione dell informazione genica Lezione nr. 8 Psicobiologia L informazione che viene trascritta non riguarda tutto il DNA ma solo delle particolari sequenze definite GENI. Tipologie
Lezione n. 11. Reazioni enzimatiche Michaelis-Menten Dipendenza di k da T. Antonino Polimeno 1
 Chimica Fisica Biotecnologie sanitarie Lezione n. 11 Reazioni enzimatiche Michaelis-Menten Dipendenza di k da T Antonino Polimeno 1 senza catalizzatore... con catalizzatore... Antonino Polimeno 2 Catalisi
Chimica Fisica Biotecnologie sanitarie Lezione n. 11 Reazioni enzimatiche Michaelis-Menten Dipendenza di k da T Antonino Polimeno 1 senza catalizzatore... con catalizzatore... Antonino Polimeno 2 Catalisi
Utilizzazione dei dati di monitoraggio biologico
 Utilizzazione dei dati di monitoraggio biologico a livello individuale: valutazione del livello di di esposizione in in funzione dei valori di di riferimento e dei valori limite biologici health based
Utilizzazione dei dati di monitoraggio biologico a livello individuale: valutazione del livello di di esposizione in in funzione dei valori di di riferimento e dei valori limite biologici health based
DESTINI METABOLICI DEL PIRUVATO
 DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
DESTINI METABOLICI DEL PIRUVATO Glicolisi Piruvato Metabolismo aerobico: il piruvato entra nel mitocondrio Acetil-CoA Ciclo di Krebs Catena di trasporto degli elettroni Complesso della Piruvato deidrogenasi
La fotosintesi Bibliografia I colori della biologia Giusti-Gatti-Anelli Ed- Pearson
 La fotosintesi Bibliografia I colori della biologia Giusti-Gatti-Anelli Ed- Pearson ORGANISMI FOTOSINTETICI Osservando piante o alghe al microscopio si possono vedere organuli colorati, all'interno dei
La fotosintesi Bibliografia I colori della biologia Giusti-Gatti-Anelli Ed- Pearson ORGANISMI FOTOSINTETICI Osservando piante o alghe al microscopio si possono vedere organuli colorati, all'interno dei
Introduzione al Metabolismo
 Chimica Biologica A.A. 2010-2011 Introduzione al Metabolismo Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Metabolismo Metabolismo l insieme dei processi attraverso
Chimica Biologica A.A. 2010-2011 Introduzione al Metabolismo Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Metabolismo Metabolismo l insieme dei processi attraverso
BIOSEGNALAZIONE. La ricezione e la trasmissione delle informazioni extracellulari Parte I
 BIOSEGNALAZIONE La ricezione e la trasmissione delle informazioni extracellulari Parte I La coordinazione delle attività metaboliche nei diversi tessuti e organi dei mammiferi avviene mediante il sistema
BIOSEGNALAZIONE La ricezione e la trasmissione delle informazioni extracellulari Parte I La coordinazione delle attività metaboliche nei diversi tessuti e organi dei mammiferi avviene mediante il sistema
Biochimica. Prof. Alessandro Tossi Edificio Q 1 piano lab 106 Dip. Scienze della Vita
 Biochimica Prof. Alessandro Tossi Edificio Q 1 piano lab 106 Dip. Scienze della Vita Biochimica: Definizioni: Chimica dei sistemi viventi Chimica: studio della struttura, interazioni e reazioni delle molecole.
Biochimica Prof. Alessandro Tossi Edificio Q 1 piano lab 106 Dip. Scienze della Vita Biochimica: Definizioni: Chimica dei sistemi viventi Chimica: studio della struttura, interazioni e reazioni delle molecole.
Nucleotidi 26/10/2014. Nucleotidi (1)
 I Nucleotidi Hanno Tre Componenti Base azotata Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Base azotata Qualsiasi composto che manifesta proprietà basiche per via della
I Nucleotidi Hanno Tre Componenti Base azotata Nucleotidi https://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/nucacids.htm Base azotata Qualsiasi composto che manifesta proprietà basiche per via della
INIBIZIONE ENZIMATICA REVERSIBILE Gli inibitori (I) legano l enzima e interferiscono con la loro attività modificando la Vmax, la Km o entrambe.
 INIBIZIONE ENZIMATICA REVERSIBILE Gli inibitori (I) legano l enzima e interferiscono con la loro attività modificando la Vmax, la Km o entrambe. Gli inibitori reversibili si legano all enzima mediante
INIBIZIONE ENZIMATICA REVERSIBILE Gli inibitori (I) legano l enzima e interferiscono con la loro attività modificando la Vmax, la Km o entrambe. Gli inibitori reversibili si legano all enzima mediante
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
L ossidazione completa del glucosio da parte dell O 2. può essere suddivisa in due semi-reazioni
 L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
L ossidazione completa del glucosio da parte dell O 2 C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O può essere suddivisa in due semi-reazioni C 6 H 12 O 6 + 6 O 2 6 CO 2 + 24 H + + 24 e - (si ossidano gli atomi
la cellula al lavoro: cenni di termodinamica, enzimi, struttura della membrana plasmatica e il trasporto di membrana
 la cellula al lavoro: cenni di termodinamica, enzimi, struttura della membrana plasmatica e il trasporto di membrana Forme di energia L energia è la capacità di trasferire calore o compiere un lavoro.
la cellula al lavoro: cenni di termodinamica, enzimi, struttura della membrana plasmatica e il trasporto di membrana Forme di energia L energia è la capacità di trasferire calore o compiere un lavoro.
Velocità di reazione Una trasformazione chimica modifica completamente la natura delle sostanze iniziali ( i reagenti), formando altre specie (i prodo
 Dinamica chimica (cinetica) Studio della velocità di reazione Bibliografia David W. Oxtoby, Norman H. Nachtrieb, Wade A. Freeman Chimica Edises Mario Nardelli Chimica generale Darrell D. Ebbing, Steven
Dinamica chimica (cinetica) Studio della velocità di reazione Bibliografia David W. Oxtoby, Norman H. Nachtrieb, Wade A. Freeman Chimica Edises Mario Nardelli Chimica generale Darrell D. Ebbing, Steven
IPOTESI UN GENE-UN ENZIMA
 IPOTESI UN GENE-UN ENZIMA DNA: contiene tutte le informazioni per definire lo sviluppo e la fisiologia della cellula: ma come svolge questa funzione? Beadle e Tatum (1941): studiando mutanti della comune
IPOTESI UN GENE-UN ENZIMA DNA: contiene tutte le informazioni per definire lo sviluppo e la fisiologia della cellula: ma come svolge questa funzione? Beadle e Tatum (1941): studiando mutanti della comune
Cap.16 GLICOLISI. Glucosio + 2 ADP + 2 Pi + 2 NAD + 2 Piruvato + 2 ATP + 2 H 2 O+ 2 NADH + 2H + 2 ADP + 2 Pi 2 ATP H 2 O 2 NAD + 2 NADH + 2H +
 Cap.16 GLICOLISI Glucosio + 2 ADP + 2 Pi + 2 NAD + 2 Piruvato + 2 ATP + 2 H 2 O+ 2 NADH + 2H + 2 ADP + 2 Pi 2 ATP 2 + 2 H 2 O 2 NAD + 2 NADH + 2H + Via metabolica in 10 tappe (reazioni) La glicolisi può
Cap.16 GLICOLISI Glucosio + 2 ADP + 2 Pi + 2 NAD + 2 Piruvato + 2 ATP + 2 H 2 O+ 2 NADH + 2H + 2 ADP + 2 Pi 2 ATP 2 + 2 H 2 O 2 NAD + 2 NADH + 2H + Via metabolica in 10 tappe (reazioni) La glicolisi può
INIBIZIONE ENZIMATICA REVERSIBILE
 INIBIZIONE ENZIMATICA REVERSIBILE La reazione enzimatica in vitro o in vivo può essere INIBITA REVERSIBILMENTE. Un inibitore (I) legandosi all enzima interferisce con la sua attività modificando la Vmax,
INIBIZIONE ENZIMATICA REVERSIBILE La reazione enzimatica in vitro o in vivo può essere INIBITA REVERSIBILMENTE. Un inibitore (I) legandosi all enzima interferisce con la sua attività modificando la Vmax,
