Equilibrio di Gibbs-Donnan
|
|
|
- Veronica Belli
- 6 anni fa
- Visualizzazioni
Transcript
1 Equilibrio di GibbsDonnan Tra due soluzioni acquose separate da una membrana che sia impermeabile ad uno solo dei soluti si stabilisce un equilibrio (equilibrio di Donnan) garantito da una differenza di potenziale transmembranaria. Una conseguenza dell equilibrio di Donnan è che tra i due compartimenti si stabilisce una differenza di pressione osmotica: la pressione osmotica è maggiore nel compartimento contenente lo ione non diffusibile.
2 Equilibrio di GibbsDonnan Immaginiamo un recipiente diviso da una membrana in due compartimenti (1 e 2) che contengono, rispettivamente, una soluzione di KCl ed una di proteinato di K (KPr) in concentrazioni inizialmente equimolari (10 mm). Immaginiamo, inoltre, che la membrana sia permeabile al K e al Cl, ma non al Pr.
3 Equilibrio di GibbsDonnan Le frecce nere indicano flussi secondo gradiente di concentrazione Le frecce bianche indicano flussi secondo gradiente eletttrico 1) Gli ioni Cl diffondono da 1 a 2 secondo il loro gradiente di concentrazione, ma così facendo creano un gradiente elettrico che li spinge in direzione opposta. 2) Il gradiente elettrico creato dalla diffusione degli ioni Cl richiama ioni K da 1 a 2, ma così facendo gli ioni K creano un gradiente di concentrazione che li spinge in direzione opposta. Quando i flussi unidirezionali contrapposti diventano uguali sia per il K che per il Cl, il flusso netto transmembranario diventa pari a 0 sia per il K che per il Cl
4 Equilibrio di GibbsDonnan Le frecce nere indicano flussi secondo gradiente di concentrazione Le frecce bianche indicano flussi secondo gradiente eletttrico In queste condizioni la differenza di potenziale che si instaura a cavallo della membrana coincide con il potenziale di equilibrio dei due ioni (E K = E Cl ) previsto dall equazione di Nerst. E K E Cl RT [ K] ln z F K [ K] Dal momento che z K = 1 e z Cl = 1, ne consegue che: 1 2 RT [ Cl] xln zclf [ Cl] 1 2 [ [ K] 2 [ Cl] K] 1 [ Cl] 2 quindi [ K][ 1 Cl] 1 [ K] 2[ Cl] 2 Relazione di Donnan 1 I prodotti delle concentrazioni degli ioni permeanti nei due compartimenti sono uguali tra loro.
5 Equilibrio di GibbsDonnan Per il principio dell elettroneutralità delle soluzioni, in ogni soluzione il numero di ioni positivi è uguale al numero di ioni negativi. Pertanto nel compartimento 1 si avrà: [K ] 1 = [Cl ] 1 mentre nel compartimento 2 si verificherà che: [K ] 2 = [Cl ] 2 [Pr ] 2 Quindi, la concentrazione totale degli ioni diffusibili (K e Cl ) è maggiore dal lato dove si trova lo ione non diffusibile (Pr ): [K ] 2 [Cl ] 2 >[K ] 1 [Cl ] 1
6 Equilibrio di GibbsDonnan Cosa comporta l equilibrio di GibbsDonnan? La concentrazione totale degli ioni diffusibili (K e Cl ) è maggiore dal lato dove si trova lo ione non diffusibile (Pr ): [K ] 2 [Cl ] 2 >[K ] 1 [Cl ] 1 Un aumento di pressione osmotica dal lato dello ione non diffusibile
7 Equilibrio di GibbsDonnan All interno di una cellula vi sono molti anioni osmoticamente attivi piuttosto impermeabili, tipo proteinati e nucleotidi. Un equilibrio di GibbsDonnan porterebbe a una disparità di pressione osmotica tra l interno e l esterno della cellula. Lo squilibrio osmotico causerebbe l ingresso d acqua e lo scoppio della cellula
8 Equilibrio di GibbsDonnan Perché una cellula non subisce un rigonfiamento osmotico per effetto Donnan e infine non si rompe? Una spiegazione è che la cellula pompa attivamente Na esternamente, riducendo la pressione osmotica nel citoplasma e incrementando quella del liquido extracellulare
9
10 Potenziale di membrana A cavallo della membrana plasmatica, quindi tra la superficie intra ed extracellulare del doppio strato fosfolipidico, di tutte le cellule esiste una differenza di potenziale detta potenziale di membrana. Esempi di potenziale di membrana
11 Potenziale di membrana A cavallo della membrana plasmatica, quindi tra la superficie intra ed extracellulare del doppio strato fosfolipidico, di tutte le cellule esiste una differenza di potenziale detta potenziale di membrana. La differenza di potenziale esistente tra i due lati della membrana plasmatica può essere misurata sperimentalmente inserendo un elettrodo in una cellula ed un secondo elettrodo nel liquido extracellulare.
12 Potenziale di membrana Per convenzione l'elettrodo extracellulare fa da terra, cioè da riferimento ed è settato a 0 mv. Se l'elettrodo extracellulare è macroscopico, l'elettrodo inserito in cellula è microscopico, tale da adeguarsi alle dimensioni cellulari. E' costituito da una micropipetta riempita da una soluzione elettrolitica in cui è immerso un filo d'argento collegato al voltmetro. La differenza di potenziale a cavallo della membrana plasmatica è generalmente negativa verso il citoplasma e positiva verso l'esterno della cellula. Il suo valore assoluto varia a seconda del tipo cellulare. Nelle cellule nervose è mediamente intorno a 70 mv.
13 Potenziale di membrana Il potenziale di membrana rappresenta una delle caratteristiche più rilevanti della Fisiologia cellulare: in molte cellule il potenziale di membrana è funzionale al trasporto transmembranario di metaboliti o sostanze nutritive, alla regolazione del ph intracellulare e alla regolazione del volume cellulare. Nelle cosiddette cellule eccitabili, neuroni e cellule muscolari, transitorie variazioni del potenziale di membrana rappresentano segnali elettrici la cui insorgenza e propagazione sono alla base del funzionamento del sistenma nervoso e di quello muscolare.
14 Potenziale di membrana La separazione di cariche a cavallo della membrana plasmatica, detta potenziale di membrana, avviene solo a cavallo della membrana mentre il citoplasma e il liquido extracellularesono elettroneutre.
15 Le cellule presentano una d.d.p. stazionaria nel tempo, e posseggono concentrazioni ioniche intracelluari stabilmente diverse da quelle extracellulari
16 Nella maggior parte delle cellule, un certo numero di ioni non è in equilibrio tra il liquido extracellulare e il citoplasma Esempio Muscolo Scheletrico di Rana: Potenziale di Riposo: 90 mv Extra Intra Potenziale Cellulare Cellulare di Equilibrio [Na ] 120 mm 9.2 mm 67 mv [K ] 2.5 mm 140 mm 105 mv [Cl ] 120 mm 34 mm 89 a 96 mv Il Cl è dunque prossimo al suo equilibrio Il Na è lo ione che si trova più lontano da una distribuzione di equilibrio Inoltre, il pot. di membrana non é un potenziale di GibbsDonnan, poiché non si é all'equilibrio, la cellula tende a perdere K e ad acquisire Na.
17 Come si genera il potenziale di membrana? Il potenziale di membrana è essenzialmente un potenziale di diffusione che scaturisce: dalla ineguale distribuzione di ioni sui due versanti della membrana, quindi nei gradienti di concentrazione ionica tra ambiente intracellulare ed extracellulare, generati e mantenuti dalla pompa NaKATPasi dalla diseguale permeabilità agli ioni da parte della membrana plasmatica. (Per permeabilità si intende la capacità di transito degli ioni attraverso canali ionici specifici) Gli ioni maggiormente coinvolti nella genesi del potenziale di membrana sono Na e K. Gli ioni Na sono più concentrati nel liquido extracellulare che dentro la cellula, gli ioni K sono più concentrati in cellula che nel liquido extracellulare. Inoltre, la membrana delle cellule è circa 40 volte più permeabile agli ioni K che agli ioni Na.
18 Come si genera il potenziale di membrana? P K > P Na 1 : 0.02 K 5 mm Na 150 mm Cl 128 mm citoplasma K Na K 150 mm Na 15 mm Cl 8 mm Proteinati Liquido extracellulare 1) Il K, essendo più concentrato all'interno della cellula, ed avendo una elevata permeabilità attraverso la membrana, tende a fuoriuscire dalla cellula. 2) Nel momento in cui gli ioni K si affacciano sul versante extracellulare della membrana caricano positivamente il versante extracellulare, mentre il versante intracellulare della membrana stessa si carica negativamente. 3) Si crea quindi ai due lati della membrana un gradiente elettrico. Tale gradiente elettrico rallenta il movimento degli ioni K, in quanto si oppone alla loro fuoriuscita.
19 P K > P Na 1 : 0.02 K 5 mm Na 150 mm Cl 128 mm Come si genera il potenziale di membrana? K Na K 150 mm Na 15 mm Cl 8 mm Proteinati citoplasma Liquido extracellulare Se il K fosse l'unica specie permeante attraverso la membrana, la forza elettrica derivante dalla separazione di cariche a cavallo della membrana diventerebbe di eguale ampiezza al gradiente di concentrazione chimico che guida gli ioni K a uscire dalla cellula. In tali condizioni il movimento netto di K attraverso la membrana si arresterebbe e si raggiungerebbe il potenziale di equilibrio del K In realtà, il valore del potenziale di equilibrio per il K calcolato si avvicina ma non corrisponde al potenziale di membrana, in quanto è più negativo. Questo dipende dal fatto che la membrana è permeabile, anche se in misura minore, al Na. Pertanto, la differenza di potenziale generata dal movimento del K accelera il movimento del Na facilitando il suo ingresso in cellula, rendendo, così, il potenziale di membrana meno negativo rispetto al potenziale di equilibrio del K.
20 Come si genera il potenziale di membrana? P K > P Na 1 : 0.02 K 5 mm Na 150 mm Cl 128 mm citoplasma K Na K 150 mm Na 15 mm Cl 8 mm Proteinati Liquido extracellulare Pertanto: a) il flusso netto passivo di Na in entrata in cellula è uguale a flusso netto passivo di K in uscita dalla cellula b) non si ha un trasporto netto di cariche da un ambiente all altro e il principio dell elettroneutralità delle soluzioni non è infranto nella massa delle soluzioni in gioco. Lo ione Cl nella maggior parte dei casi è distribuito all equilibrio.
21 Potenziale di membrana Le cellule sono almeno 40 volte più permeabili al K rispetto al Na In quanto una piccola quota di Na riesce ad entrare, la d.d.p. è lievemente più positiva rispetto al pot. di equilibrio del K di 90 mv P K > P Na 1 : 0.02 K Na
22 Come mai il Potenziale di membrana e le concentrazioni ioniche sono COSTANTI nel tempo? La risposta é nell'attività dell Na /K ATPasi di membrana che: 1) espellendo attivamente Na entrato passivamente e ricaptando K, mantiene costanti nel tempo le differenze di concentr. ioniche e di conseguenza indirettamente il pot di membrana K 2K La pompa Na K ATPasi genera dei controflussi attivi che controbilanciano i flusso passivi degli ioni Na e K attraverso i rispettivi canali. Na 3Na 2) essendo elettrogenica (scambia 3 ioni Na con 2 ioni K) può essa stessa generare un potenziale elettrico attivo che si addiziona a quello di diffusione di Na e K. Il contributo al potenziale di membrane derivante dalla elettrogenicità della pompa è di circa il 5%.
23 Potenziale di membrana ed equazione di Goldmann Il potenziale di membrana, essendo un potenziale di diffusione, può essere calcolato mediante l equazione di Goldmann HodgkinKatz. Dal momento che gli ioni maggiormente coinvolti nella genesi del potenziale di membrana sono gli ioni K e Na, l equazione di Goldmann può essere applicata al Na e K : D = RT ln PNa[Na]est PK[K]est zf PNa[Na]int PK[K]int Se dividiamo il numeratore e il denominatore per PK e conglobiamo il termine RT/F, l equazione diventa: D = RT ln PNa/PK[Na]est [K]est zf PNa/PK[Na]int [K]int Se consideriamo che la [Na] est = 145 mm, la [Na] int = 15 mm; la [K] est = 4 mm; la [K] int = 140mM e che la permeabilità del K è circa 40 volte maggiore della permeabilità del Na, allora: D = 58 Log (0,025) (145mM) 4mM = 58Log(0,054) = 73,4mV (0,025)(15mM) 140 mm
24 Potenziale di membrana ed equazione di Goldmann D = 58 Log (0,025) (145mM) 4mM = 58Log(0,054) = 73,4mV (0,025)(15mM) 140 mm Il valore del potenziale di membrana ottenuto è più vicino al potenziale di equilibrio del K (90mV) che a quello del Na (58mV). Se vi fosse un cambiamento di permeabilità relativa al Na e al K, l equazione di Goldmann darebbe origine ad un nuovo valore di potenziale di membrana. E da notare che se la permeabilità a uno dei due ioni è pari a zero, allora l equazione di Godmann si riduce all equazione di Nerst per l altro ione. Se la membrana è permeabile ad un solo ione, il potenziale di membrana è pari al potenziale di equilibrio di quello ione.
25 Potenziale di membrana e forza elettrochimica agente sugli ioni Poiché né il Na né il K si trovano in una situazione di equilibrio, una forza elettrochimica netta agisce su tali ioni. La seguente regola descrive la forza elettrochimica che agisce sugli ioni che permeano attraverso la membrana: La forza elettrochimica netta che agisce su uno ione tende a farlo muovere attraverso la membrana in direzione tale da avvicinare il potenziale di membrana al potenziale di equilibrio di quello stesso ione, cioè tale da portare lo ione più vicino al suo equilibrio. Quindi, quando un certo numero di ioni si distribuisce ai lati di una membrana, e tutti sono lontani dal loro equilibrio elettrochimico, ognuno tenderà a spostare il potenziale di membrana verso il suo potenziale di equilibrio (di Nernst) Più permeabile è la membrana ad un particolare ione, maggiore è la forza con cui quello ione tende a portare il potenziale di membrana verso il proprio potenziale d equilibrio
26 Potenziale di membrana e correnti ioniche Nella genesi del potenziale di membrana l afflusso di sodio è esattamente controbilanciato dall efflusso di potassio. Dal punto di vista elettrico vuol dire che: ik ik ina = 0 K Na K. e per quelle cellule con una sensibile permeabilità al cloro: ina Na ik ina icl = 0
27 Potenziale di membrana e correnti ioniche Per la legge di Ohm: i = E/R ed essendo R = 1/g i = E. g g = conduttanza dello ione che si esprime in S/cm 2 (ms o µs o ps/cm 2 ). E direttamente correlata con la permeabilità E = differenza di potenziale La forza elettromotrice che fa muovere uno ione attraverso la membrana è pari alla differenza tra il potenziale di membrana (E m ) e il suo potenziale di equilibrio (E ione ): E m E ione (di Nernst) Pertanto, la corrente di ogni singolo ione attraverso la membrana matematicamente dalla seguente relazione: può essere descritta i = g (V m E ione ) cioè i K = g k (E m E k ) e i Na = g Na (E m E Na ) e i Cl = g Cl (E m E Cl )
28 Potenziale di membrana e conduttanze ioniche Considerando Na, K e Cl, la differenza di potenziale a cavallo della membrana sarà data dalla EQUAZIONE DELLA CONDUTTANZA DI MEMBRANA: E m = g K g g Na g Cl E K E Na E Dove: g = g Cl K g Na g Cl g g g = 1/R Più la membrana è permeabile ad uno ione, maggiore è la conduttanza di membrana a quello ione Em = E Na g Na E k g k g Na g K
29 La conduttanza della membrana è una misura della facilità con cui una corrente ionica può attraversarla Le differenze esistenti tra Permeabilità e Conduttanza permeabilità elevata in presenza di pochi ioni = debole corrente ionica = G modesta K K K Permeabilità elevata in presenza di molti ioni = elevata corrente ionica = G alta K K K K K K Permeabilità e conduttanza, benché direttamente correlate, non sono la stessa cosa. La permeabilità dà una misura della velocità con cui lo ione passa la membrana. La conduttanza della membrana ad uno ione dipende sia dalla permeabilità che dal numero di ioni disponibili in soluzione.
30
31 Equivalente elettrico della membrana La membrana cellulare manifesta una differenza di potenziale negativa verso il lato citoplasmatico della membrana. In termini elettrici è come se le due superfici della membrana corrispondessero ai due poli di una pila elettrica, il cui polo negativo è situato all interno della cellula e quello positivo verso l esterno. Il doppio strato fosfolipidico, impermeabile agli ioni, agendo come isolante conferisce alla membrana una capacità elettrica, pertanto può essere assimilato ad un condensatore le cui armature sono rappresentate dalle superfici della membrana rivolte rispettivamente verso il lato extracellulare ed intracellulare. N.B. La capacità del condensatore è un indice della facilità con la quale cariche separate possono essere conservate Il condensatore è l elemento di un circuito che opera da immagazzinatore e «rilasciatore» di cariche.
32 Equivalente elettrico della membrana I canali ionici attraverso cui passano le cariche elettriche dotano la membrana di una propria conduttanza elettrica. Infatti, la permeabilità del canale nei confronti dello ione può essere rappresentato da un punto di vista elettrico con un resistore ovvero con il suo inverso la conduttanza. Queste proprietà elettriche della membrana possono essere convenientemente rappresentate tramite un circuito equivalente in cui un condensatore è collegato in parallelo con una resistenza.
33 Pertanto, un canale e il gradiente di concentrazione dello ione permeante che lo attraversa possono essere rappresentati da un punto di vista elettrico come costituiti rispettivamente da un resistore e da una batteria in serie Se sulla membrana esistono più canali ciascuno selettivo per un certo ione, il circuito elettrico equivalente sarà del tipo: esterno Na Cl 1/g Na 1/g K 1/g Cl K E Na E K E Cl interno
34 Circuito elettrico equivalente di una membrana biologica che presenta le conduttanze del Na e del K. Tutte le rimanenti conduttanze sono sommate insieme come 1/g T. I gradienti di concentrazione del Na e del K Le pile di concentrazione E Na e E K sono in serie alle rispettive conduttanze e con polarità opposte extracellulare 1 1 g Na g K Cm 1 g T Vm E Na E K intracellulare
La pompa sodio-potassio
 a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 La pompa sodio-potassio 14/3/2006 Efficienza del cuore Dipende dall ordinata sequenza di eccitazione e di contrazione che procede
a.a. 2005/2006 Laurea Specialistica in Fisica Corso di Fisica Medica 1 La pompa sodio-potassio 14/3/2006 Efficienza del cuore Dipende dall ordinata sequenza di eccitazione e di contrazione che procede
Potenziale di membrana: Differenza di potenziale elettrico a cavallo della membrana cellulare dovuta ad una diversa distribuzione ionica ai due lati
 Potenziale di membrana: Differenza di potenziale elettrico a cavallo della membrana cellulare dovuta ad una diversa distribuzione ionica ai due lati della membrana. Il potenziale di membrana (negativo
Potenziale di membrana: Differenza di potenziale elettrico a cavallo della membrana cellulare dovuta ad una diversa distribuzione ionica ai due lati della membrana. Il potenziale di membrana (negativo
Scaricato da
 -Equilibrio diffusivo (chimico): in seguito alla diffusione la concentrazione delle molecole è uguale in tutte le parti del sistema C 1 Equilibrio diffusivo Le membrane cellulari sono selettivamente permeabili,
-Equilibrio diffusivo (chimico): in seguito alla diffusione la concentrazione delle molecole è uguale in tutte le parti del sistema C 1 Equilibrio diffusivo Le membrane cellulari sono selettivamente permeabili,
Trasporto di membrana
 Trasporto di membrana CdL Tecnici di Lab Biomedico AA. 2011/12 Prof.ssa Frabetti Trasporto di membrana molecole piccole molecole grosse trasporto passivo trasporto attivo (con pompe o cotrasportatori)
Trasporto di membrana CdL Tecnici di Lab Biomedico AA. 2011/12 Prof.ssa Frabetti Trasporto di membrana molecole piccole molecole grosse trasporto passivo trasporto attivo (con pompe o cotrasportatori)
ELETTROCHIMICA. Zn(s) + Cu +2 Zn +2 + Cu. Ossidazione: perdita di elettroni Riduzione: acquisto di elettroni. +2e
 ELETTROCHIMICA Branca della chimica che studia le trasformazioni chimiche in cui sono coinvolti flussi di elettroni. Reazioni con trasferimento di elettroni (ossido riduzione) 2e Zn(s) + Cu +2 Zn +2 +
ELETTROCHIMICA Branca della chimica che studia le trasformazioni chimiche in cui sono coinvolti flussi di elettroni. Reazioni con trasferimento di elettroni (ossido riduzione) 2e Zn(s) + Cu +2 Zn +2 +
Reazioni redox ed elettrochimica Nelle reazioni di ossidoriduzione degli elettroni vengono trasferiti da un reagente ad un altro reagente.
 Reazioni redox ed elettrochimica Nelle reazioni di ossidoriduzione degli elettroni vengono trasferiti da un reagente ad un altro reagente. Ossidazione corrisponde a perdita di elettroni, per cui il reagente
Reazioni redox ed elettrochimica Nelle reazioni di ossidoriduzione degli elettroni vengono trasferiti da un reagente ad un altro reagente. Ossidazione corrisponde a perdita di elettroni, per cui il reagente
Lezione 39: la legge di Ohm e i circuiti elettrici
 Lezione 39 - pag.1 Lezione 39: la legge di Ohm e i circuiti elettrici 39.1. Il circuito elementare Nella scorsa lezione abbiamo rappresentato in modo più o meno realistico alcuni circuiti elettrici particolarmente
Lezione 39 - pag.1 Lezione 39: la legge di Ohm e i circuiti elettrici 39.1. Il circuito elementare Nella scorsa lezione abbiamo rappresentato in modo più o meno realistico alcuni circuiti elettrici particolarmente
Corso di Laurea in Scienza dei Materiali Laboratorio di Fisica II ESPERIENZA DC3. Circuiti in corrente continua
 Corso di Laurea in Scienza dei Materiali Laboratorio di Fisica II Scopo dell'esperienza ESPERIENZA DC3 Circuiti in corrente continua 1. Determinazione della caratteristica I/V di un conduttore non ohmico:
Corso di Laurea in Scienza dei Materiali Laboratorio di Fisica II Scopo dell'esperienza ESPERIENZA DC3 Circuiti in corrente continua 1. Determinazione della caratteristica I/V di un conduttore non ohmico:
I compartimenti liquidi corporei
 I compartimenti liquidi corporei Il mantenimento di un volume relativamente costante e di una composizione stabile dei liquidi corporei è essenziale per l omeostasi. In condizioni di equilibrio, l assunzione
I compartimenti liquidi corporei Il mantenimento di un volume relativamente costante e di una composizione stabile dei liquidi corporei è essenziale per l omeostasi. In condizioni di equilibrio, l assunzione
DIODO. La freccia del simbolo indica il verso della corrente.
 DIODO Si dice diodo un componente a due morsetti al cui interno vi è una giunzione P-N. Il terminale del diodo collegato alla zona P si dice anodo; il terminale collegato alla zona N si dice catodo. Il
DIODO Si dice diodo un componente a due morsetti al cui interno vi è una giunzione P-N. Il terminale del diodo collegato alla zona P si dice anodo; il terminale collegato alla zona N si dice catodo. Il
Il neurone. I neuroni trasmettono l informazione ad altri neuroni o alle cellule effettrici (cellule muscolari) attraverso le sinapsi.
 Il neurone I neuroni trasmettono l informazione ad altri neuroni o alle cellule effettrici (cellule muscolari) attraverso le sinapsi. Trasmissione sinaptica Ingresso: segnali sinaptici Integrazione: segnali
Il neurone I neuroni trasmettono l informazione ad altri neuroni o alle cellule effettrici (cellule muscolari) attraverso le sinapsi. Trasmissione sinaptica Ingresso: segnali sinaptici Integrazione: segnali
Bioingegneria Elettronica I
 Bioingegneria Elettronica I Cenni alla fisiologia delle cellule e dei sistemi biologici A. Bonfiglio La cellula struttura generale La cellula Struttura generale della cellula Composizione dei liquidi intracellulare
Bioingegneria Elettronica I Cenni alla fisiologia delle cellule e dei sistemi biologici A. Bonfiglio La cellula struttura generale La cellula Struttura generale della cellula Composizione dei liquidi intracellulare
I segnali elettrici generati nei neuroni sono modificazioni del potenziale di riposo determinate dall apertura o chiusura di canali ionici:
 I segnali elettrici generati nei neuroni sono modificazioni del potenziale di riposo determinate dall apertura o chiusura di canali ionici: Potenziali graduati (risposte passive): modulabili in ampiezza,
I segnali elettrici generati nei neuroni sono modificazioni del potenziale di riposo determinate dall apertura o chiusura di canali ionici: Potenziali graduati (risposte passive): modulabili in ampiezza,
Dipartimento di Farmacia
 Dipartimento di Farmacia 1) L esame è diviso in: PARTE A (Elementi di Biologia, Anatomia e Fisiologia Generale); PARTE B (Fisiopatologia della Nutrizione); 2) PARTE A e PARTE B possono essere sostenute
Dipartimento di Farmacia 1) L esame è diviso in: PARTE A (Elementi di Biologia, Anatomia e Fisiologia Generale); PARTE B (Fisiopatologia della Nutrizione); 2) PARTE A e PARTE B possono essere sostenute
SOLUZIONI. Soluzione diluita: è costituita da un liquido (solvente) in cui è disciolta una piccola quantità di un altra sostanza (soluto).
 SOLUZIONI Soluzione diluita: è costituita da un liquido (solvente) in cui è disciolta una piccola quantità di un altra sostanza (soluto). Concentrazione di una soluzione: Molarità: Frazione molare: 1 SOLUZIONI
SOLUZIONI Soluzione diluita: è costituita da un liquido (solvente) in cui è disciolta una piccola quantità di un altra sostanza (soluto). Concentrazione di una soluzione: Molarità: Frazione molare: 1 SOLUZIONI
ESERCIZIO SOLUZIONE. 13 Aprile 2011
 ESERCIZIO Un corpo di massa m è lasciato cadere da un altezza h sull estremo libero di una molla di costante elastica in modo da provocarne la compressione. Determinare: ) la velocità del corpo all impatto
ESERCIZIO Un corpo di massa m è lasciato cadere da un altezza h sull estremo libero di una molla di costante elastica in modo da provocarne la compressione. Determinare: ) la velocità del corpo all impatto
Ruolo del calcio nella cellula
 Ruolo del calcio nella cellula I meccanismi evolutivi hanno attribuito agli ioni fosfato un importanza fondamentale poiché sono necessari per sintetizzare ATP. Per questo motivo la loro concentrazione
Ruolo del calcio nella cellula I meccanismi evolutivi hanno attribuito agli ioni fosfato un importanza fondamentale poiché sono necessari per sintetizzare ATP. Per questo motivo la loro concentrazione
ESERCIZI PER LE VACANZE ESTIVE
 Opera Monte Grappa ESERCIZI PER LE VACANZE ESTIVE Claudio Zanella 14 2 ESERCIZI: Calcolo della resistenza di un conduttore filiforme. 1. Calcola la resistenza di un filo di rame lungo 100m e della sezione
Opera Monte Grappa ESERCIZI PER LE VACANZE ESTIVE Claudio Zanella 14 2 ESERCIZI: Calcolo della resistenza di un conduttore filiforme. 1. Calcola la resistenza di un filo di rame lungo 100m e della sezione
Molti sali contengono un anione o un catione che possono reagire con acqua rendendo le loro soluzioni ACIDE o BASICHE
 Molti sali contengono un anione o un catione che possono reagire con acqua rendendo le loro soluzioni ACIDE o BASICHE Molti sali reagiscono con l acqua alterando il suo rapporto molare tra [H] e [OH] -
Molti sali contengono un anione o un catione che possono reagire con acqua rendendo le loro soluzioni ACIDE o BASICHE Molti sali reagiscono con l acqua alterando il suo rapporto molare tra [H] e [OH] -
BILANCIO IDROLETTROLITICO (Alfonso Siani. ISA CNR) ACQUA
 BILANCIO IDROLETTROLITICO (Alfonso Siani. ISA CNR) ACQUA L acqua rappresenta il maggiore costituente dell organismo umano, e rappresenta all incirca il 60% del peso corporeo di un adulto. Il contenuto
BILANCIO IDROLETTROLITICO (Alfonso Siani. ISA CNR) ACQUA L acqua rappresenta il maggiore costituente dell organismo umano, e rappresenta all incirca il 60% del peso corporeo di un adulto. Il contenuto
Capacità. Capacità elettrica Condensatore Condensatore = sistema per immagazzinare energia (elettrica) Fisica II CdL Chimica
 Capacità Capacità elettrica Condensatore Condensatore = sistema per immagazzinare energia (elettrica) Definizione Capacità La capacità è una misura di quanta carica debba possedere un certo tipo di condensatore
Capacità Capacità elettrica Condensatore Condensatore = sistema per immagazzinare energia (elettrica) Definizione Capacità La capacità è una misura di quanta carica debba possedere un certo tipo di condensatore
Fisiologia Renale 6. Bilancio idro-elettrolitico I. Carlo Capelli Fisiologia Corso di Laurea in Scienze Motorie Università di Verona
 Fisiologia Renale 6. Bilancio idro-elettrolitico I Carlo Capelli Fisiologia Corso di Laurea in Scienze Motorie Università di Verona Obiettivi Acqua corporea totale: volume e distribuzione Distretti intra
Fisiologia Renale 6. Bilancio idro-elettrolitico I Carlo Capelli Fisiologia Corso di Laurea in Scienze Motorie Università di Verona Obiettivi Acqua corporea totale: volume e distribuzione Distretti intra
LEZIONE 4. Le soluzioni
 LEZIONE 4 Le soluzioni Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il componente delle
LEZIONE 4 Le soluzioni Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il componente delle
La corrente alternata
 La corrente alternata Corrente continua e corrente alternata Le correnti continue sono dovute ad un generatore i cui poli hanno sempre lo stesso segno e pertanto esse percorrono un circuito sempre nello
La corrente alternata Corrente continua e corrente alternata Le correnti continue sono dovute ad un generatore i cui poli hanno sempre lo stesso segno e pertanto esse percorrono un circuito sempre nello
ESERCITAZIONI FISICA PER FARMACIA A.A. 2012/2013 ELETTROMAGNETISMO - OTTICA
 ESERCITAZIONI FISICA PER FARMACIA A.A. 2012/2013 ELETTROMAGNETISMO - OTTICA Esercizio 1 Due cariche q 1 e q 2 sono sull asse x, una nell origine e l altra nel punto x = 1 m. Si trovi il campo elettrico
ESERCITAZIONI FISICA PER FARMACIA A.A. 2012/2013 ELETTROMAGNETISMO - OTTICA Esercizio 1 Due cariche q 1 e q 2 sono sull asse x, una nell origine e l altra nel punto x = 1 m. Si trovi il campo elettrico
ESPONENZIALI E LOGARITMI. chiameremo logaritmica (e si legge il logaritmo in base a di c è uguale a b ).
 ESPONENZIALI E LOGARITMI Data una espressione del tipo a b = c, che chiameremo notazione esponenziale (e dove a>0), stabiliamo di scriverla anche in un modo diverso: log a c = b che chiameremo logaritmica
ESPONENZIALI E LOGARITMI Data una espressione del tipo a b = c, che chiameremo notazione esponenziale (e dove a>0), stabiliamo di scriverla anche in un modo diverso: log a c = b che chiameremo logaritmica
Corso di Laurea in FARMACIA
 Corso di Laurea in FARMACIA 2015 simulazione 1 FISICA Cognome nome matricola a.a. immatric. firma N Evidenziare le risposte esatte Una sferetta è appesa con una cordicella al soffitto di un ascensore fermo.
Corso di Laurea in FARMACIA 2015 simulazione 1 FISICA Cognome nome matricola a.a. immatric. firma N Evidenziare le risposte esatte Una sferetta è appesa con una cordicella al soffitto di un ascensore fermo.
IL CIRCUITO ELETTRICO RESISTENZE IN PARALLELO
 Laboratorio di.... Scheda n. 4 Livello: Medio A.S.... Classe. NOME..... DATA... Prof.... IL CIRCUITO ELETTRICO RESISTENZE IN PARALLELO R1 R2 Conoscenze - Conoscere le grandezze elettriche che caratterizzano
Laboratorio di.... Scheda n. 4 Livello: Medio A.S.... Classe. NOME..... DATA... Prof.... IL CIRCUITO ELETTRICO RESISTENZE IN PARALLELO R1 R2 Conoscenze - Conoscere le grandezze elettriche che caratterizzano
Attrito statico e attrito dinamico
 Forza di attrito La presenza delle forze di attrito fa parte dell esperienza quotidiana. Se si tenta di far scorrere un corpo su una superficie, si sviluppa una resistenza allo scorrimento detta forza
Forza di attrito La presenza delle forze di attrito fa parte dell esperienza quotidiana. Se si tenta di far scorrere un corpo su una superficie, si sviluppa una resistenza allo scorrimento detta forza
Corso di Laurea in Scienza dei Materiali Laboratorio di Fisica II ESPERIENZA DC1. Circuiti in corrente continua
 Corso di Laurea in Scienza dei Materiali Laboratorio di Fisica II ESPERIENZA DC1 Circuiti in corrente continua Scopo dell'esperienza 1. Utilizzo di voltmetro ed amperometro; 2. verifica della validità
Corso di Laurea in Scienza dei Materiali Laboratorio di Fisica II ESPERIENZA DC1 Circuiti in corrente continua Scopo dell'esperienza 1. Utilizzo di voltmetro ed amperometro; 2. verifica della validità
FISIOLOGIA RENALE 2. Funzioni tubulari, riassorbimento obbligatorio dell acqua
 FISIOLOGIA RENALE 2. Funzioni tubulari, riassorbimento obbligatorio dell acqua Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie Università degli Studi Verona Obiettivi Funzioni
FISIOLOGIA RENALE 2. Funzioni tubulari, riassorbimento obbligatorio dell acqua Fisiologia Generale e dell Esercizio Carlo Capelli Facoltà di Scienze Motorie Università degli Studi Verona Obiettivi Funzioni
Le proprietà colligative delle soluzioni Sappiamo dall esperienza quotidiana che una soluzione ha caratteristiche diverse dal solvente puro.
 Le proprietà colligative delle soluzioni Sappiamo dall esperienza quotidiana che una soluzione ha caratteristiche diverse dal solvente puro. Molte delle sue proprietà, come il sapore, il colore, l odore,
Le proprietà colligative delle soluzioni Sappiamo dall esperienza quotidiana che una soluzione ha caratteristiche diverse dal solvente puro. Molte delle sue proprietà, come il sapore, il colore, l odore,
5.10 Grazie alle proteine, la membrana plasmatica svolge molteplici funzioni
 5.10 Grazie alle proteine, la membrana plasmatica svolge molteplici funzioni Molte proteine della membrana plasmatica sono enzimi appartenenti a squadre di catalizzatori che agiscono nella catena di montaggio
5.10 Grazie alle proteine, la membrana plasmatica svolge molteplici funzioni Molte proteine della membrana plasmatica sono enzimi appartenenti a squadre di catalizzatori che agiscono nella catena di montaggio
FORZA DI ACIDI E BASI HA + :B HB + + A
 FORZA DI ACIDI E BASI n La forza di un acido è la misura della tendenza di una sostanza a cedere un protone. n La forza di una base è una misura dell'affinità di un composto ad accettare un protone. n
FORZA DI ACIDI E BASI n La forza di un acido è la misura della tendenza di una sostanza a cedere un protone. n La forza di una base è una misura dell'affinità di un composto ad accettare un protone. n
ATOMI E MOLECOLE. Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti).
 1 ATOMI E MOLECOLE Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti). Un elemento (es. il mercurio) è una sostanza che non può
1 ATOMI E MOLECOLE Tutte le varie forme di materia esistenti sono costituite da sostanze semplici (elementi) e da sostanze composte (composti). Un elemento (es. il mercurio) è una sostanza che non può
Funzioni Pari e Dispari
 Una funzione f : R R si dice Funzioni Pari e Dispari PARI: se f( ) = f() R In questo caso il grafico della funzione è simmetrico rispetto all asse DISPARI: se f( ) = f() R In questo caso il grafico della
Una funzione f : R R si dice Funzioni Pari e Dispari PARI: se f( ) = f() R In questo caso il grafico della funzione è simmetrico rispetto all asse DISPARI: se f( ) = f() R In questo caso il grafico della
= 300mA. Applicando la legge di Ohm su R4 si calcola facilmente V4: V4 = R4
 AI SEZIONE DI GENOVA orso di teoria per la patente di radioamatore, di Giulio Maselli IZASP Soluzioni degli Esercizi su resistenze, condensatori, induttanze e reattanze ) a) Le tre resistenze sono collegate
AI SEZIONE DI GENOVA orso di teoria per la patente di radioamatore, di Giulio Maselli IZASP Soluzioni degli Esercizi su resistenze, condensatori, induttanze e reattanze ) a) Le tre resistenze sono collegate
Graficazione qualitativa del luogo delle radici
 .. 5.3 1 Graficazione qualitativa del luogo delle radici Esempio. Si faccia riferimento al seguente sistema retroazionato: d(t) G(s) r(t) e(t) K 1(s 1) s(s + 1)(s + 8s + 5) y(t) Per una graficazione qualitativa
.. 5.3 1 Graficazione qualitativa del luogo delle radici Esempio. Si faccia riferimento al seguente sistema retroazionato: d(t) G(s) r(t) e(t) K 1(s 1) s(s + 1)(s + 8s + 5) y(t) Per una graficazione qualitativa
Ultima verifica pentamestre. 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!
 Ultima verifica pentamestre 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!) 2) gruppi dal IV al VIII 3) differenza tra massa atomica e massa atomica
Ultima verifica pentamestre 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!) 2) gruppi dal IV al VIII 3) differenza tra massa atomica e massa atomica
CORSO DI FISICA ASPERIMENTALE II ESERCIZI SU RESISTENZE IN SERIE E PARALLELO Docente: Claudio Melis
 CORSO DI FISICA ASPERIMENTALE II ESERCIZI SU RESISTENZE IN SERIE E PARALLELO Docente: Claudio Melis 1) Un generatore di tensione reale da 20 V provvisto di resistenza interna r pari a 2 Ω è connesso in
CORSO DI FISICA ASPERIMENTALE II ESERCIZI SU RESISTENZE IN SERIE E PARALLELO Docente: Claudio Melis 1) Un generatore di tensione reale da 20 V provvisto di resistenza interna r pari a 2 Ω è connesso in
Generatori di tensione
 Correnti alternate Generatori di tensione Sinora come generatore di forza elettromotrice abbiamo preso in considerazione soltanto la pila elettrica. Questo generatore ha la caratteristica di fornire sempre
Correnti alternate Generatori di tensione Sinora come generatore di forza elettromotrice abbiamo preso in considerazione soltanto la pila elettrica. Questo generatore ha la caratteristica di fornire sempre
RELÈ di TERRA PER TENSIONE CONTINUA M79
 RELÈ di TERRA PER TENSIONE CONTINUA M79 1 di 6 GENERALITÀ Il relè statico M79 è utilizzato nelle reti di distribuzione in corrente continua, bilanciate verso massa, per monitorare rilevare e segnalare
RELÈ di TERRA PER TENSIONE CONTINUA M79 1 di 6 GENERALITÀ Il relè statico M79 è utilizzato nelle reti di distribuzione in corrente continua, bilanciate verso massa, per monitorare rilevare e segnalare
Processi ossido-riduttivi chimici ed elettrochimici
 Processi ossido-riduttivi chimici ed elettrochimici Le reazioni ossidoriduttive comportano la variazione dello stato di ossidazione di almeno un elemento in seguito alla conversione dei reagenti nei prodotti
Processi ossido-riduttivi chimici ed elettrochimici Le reazioni ossidoriduttive comportano la variazione dello stato di ossidazione di almeno un elemento in seguito alla conversione dei reagenti nei prodotti
COSTRUZIONE DI UN VOLTMETRO A DIVERSE PORTATE; MISURA DELLA RESISTENZA INTERNA E VARIAZIONE DELLA PORTATA DI UN VOLTMETRO
 COSTRUZIONE DI UN VOLTMETRO A DIVERSE PORTATE; MISURA DELLA RESISTENZA INTERNA E VARIAZIONE DELLA PORTATA DI UN VOLTMETRO L esercitazione è divisa in due parti. Nella prima parte si costruisce un voltmetro
COSTRUZIONE DI UN VOLTMETRO A DIVERSE PORTATE; MISURA DELLA RESISTENZA INTERNA E VARIAZIONE DELLA PORTATA DI UN VOLTMETRO L esercitazione è divisa in due parti. Nella prima parte si costruisce un voltmetro
Le componenti del sistema nervoso. Sistema efferente motorio Sistema afferente sensoriale
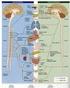 Le componenti del sistema nervoso Sistema efferente motorio Sistema afferente sensoriale Un neurone sensoriale Il corpuscolo di Pacini Recettore fasico che privato della capsula si comporta come un recettore
Le componenti del sistema nervoso Sistema efferente motorio Sistema afferente sensoriale Un neurone sensoriale Il corpuscolo di Pacini Recettore fasico che privato della capsula si comporta come un recettore
1. Le teorie sugli acidi e sulle basi 2. La ionizzazione dell acqua 3. Il ph 4. La forza degli acidi e delle basi 5. Come calcolare il ph di
 Unità 19 Acidi e basi si scambiano protoni 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione dell acqua 3. Il ph 4. La forza degli acidi e delle basi 5. Come calcolare il ph di soluzioni acide e
Unità 19 Acidi e basi si scambiano protoni 1. Le teorie sugli acidi e sulle basi 2. La ionizzazione dell acqua 3. Il ph 4. La forza degli acidi e delle basi 5. Come calcolare il ph di soluzioni acide e
INTERPRETAZIONE CINEMATICA DELLA DERIVATA
 INTERPRETAZIONE CINEMATICA DELLA DERIVATA Consideriamo un punto mobile sopra una qualsiasi linea Fissiamo su tale linea un punto O, come origine degli archi, e un verso di percorrenza come verso positivo;
INTERPRETAZIONE CINEMATICA DELLA DERIVATA Consideriamo un punto mobile sopra una qualsiasi linea Fissiamo su tale linea un punto O, come origine degli archi, e un verso di percorrenza come verso positivo;
Robotica industriale. Richiami di statica del corpo rigido. Prof. Paolo Rocco
 Robotica industriale Richiami di statica del corpo rigido Prof. Paolo Rocco (paolo.rocco@polimi.it) Sistemi di forze P 1 P 2 F 1 F 2 F 3 F n Consideriamo un sistema di forze agenti su un corpo rigido.
Robotica industriale Richiami di statica del corpo rigido Prof. Paolo Rocco (paolo.rocco@polimi.it) Sistemi di forze P 1 P 2 F 1 F 2 F 3 F n Consideriamo un sistema di forze agenti su un corpo rigido.
LA FORZA...SIA CON TE!
 LA FORZA...SIA CON TE! CHE COS'E' LA FORZA? E' UNA GRANDEZZA FISICA VETTORIALE. L'UNITA' DI MISURA NEL S.I. E' IL "NEWTON" ( N ), DAL CELEBRE SCIENZIATO INGLESE ISAAC NEWTON, CHE NE HA STUDIATO LE LEGGI,
LA FORZA...SIA CON TE! CHE COS'E' LA FORZA? E' UNA GRANDEZZA FISICA VETTORIALE. L'UNITA' DI MISURA NEL S.I. E' IL "NEWTON" ( N ), DAL CELEBRE SCIENZIATO INGLESE ISAAC NEWTON, CHE NE HA STUDIATO LE LEGGI,
I RADICALI QUADRATICI
 I RADICALI QUADRATICI 1. Radici quadrate Definizione di radice quadrata: Si dice radice quadrata di un numero reale positivo o nullo a, e si indica con a, il numero reale positivo o nullo (se esiste) che,
I RADICALI QUADRATICI 1. Radici quadrate Definizione di radice quadrata: Si dice radice quadrata di un numero reale positivo o nullo a, e si indica con a, il numero reale positivo o nullo (se esiste) che,
Le proprietà colligative delle soluzioni
 1 Approfondimento 1.3 Le proprietà colligative delle soluzioni In un solvente puro, cioè senza soluti disciolti in esso, le molecole sono libere di interagire tra loro, attraendosi. L aggiunta di un soluto
1 Approfondimento 1.3 Le proprietà colligative delle soluzioni In un solvente puro, cioè senza soluti disciolti in esso, le molecole sono libere di interagire tra loro, attraendosi. L aggiunta di un soluto
Energia elettrica. L atomo nel suo complesso è neutro perché ha l equilibrio tra protoni ed elettroni presenti nello stesso numero.
 Energia elettrica Si fonda sulla costituzione dell atomo che è costituito da particelle più piccole : neutroni (carica neutra) e protoni (carica +) che costituiscono il nucleo ed elettroni (carica negativa)
Energia elettrica Si fonda sulla costituzione dell atomo che è costituito da particelle più piccole : neutroni (carica neutra) e protoni (carica +) che costituiscono il nucleo ed elettroni (carica negativa)
IN UN ATOMO SI DISTINGUE UN NUCLEO CARICO POSITIVAMENTE ATTORNO AL QUALE RUOTANO PARTICELLE CARICHE NEGATIVAMENTE: GLI ELETTRONI (e - ) (-)
 LA VITA, LA CHIMICA E L ACQUA PER INIZIARE QUALCHE CENNO DI CHIMICA LA MATERIA E FATTA DI COMBINAZIONI DI ELEMENTI. GLI ELEMENTI SONO COMPOSTI DA SINGOLI ATOMI, LE PIU PICCOLE UNITA CHE MANTENGONO LE PROPRIETA
LA VITA, LA CHIMICA E L ACQUA PER INIZIARE QUALCHE CENNO DI CHIMICA LA MATERIA E FATTA DI COMBINAZIONI DI ELEMENTI. GLI ELEMENTI SONO COMPOSTI DA SINGOLI ATOMI, LE PIU PICCOLE UNITA CHE MANTENGONO LE PROPRIETA
Figura 1. Indicando con f la forza elettromotrice della batteria e con I la corrente elettrica che circola nel circuito, si ha
 Realizzando circuiti resistivi con batterie da 4,5 V e lampadine da 1,5 W è interessante interpretare i cambiamenti in termini di luminosità delle lampadine che si osservano nelle varie configurazioni
Realizzando circuiti resistivi con batterie da 4,5 V e lampadine da 1,5 W è interessante interpretare i cambiamenti in termini di luminosità delle lampadine che si osservano nelle varie configurazioni
PRINCIPI FISICI DEI FENOMENI ELETTRICI
 PRINCIPI FISICI DEI FENOMENI ELETTRICI STRUTTURA DELLA MATERIA Con il nome elettricità si intendono tutti quei fenomeni fisici nei quali intervengono cariche elettriche, sia ferme sia in movimento. Per
PRINCIPI FISICI DEI FENOMENI ELETTRICI STRUTTURA DELLA MATERIA Con il nome elettricità si intendono tutti quei fenomeni fisici nei quali intervengono cariche elettriche, sia ferme sia in movimento. Per
 positiva, endotermico (la soluzione si raffredda) negativa, esotermico (la soluzione si scalda). DH sol = E ret + E solv concentrazione Molare Esempio: Preparare mezzo litro (0,5 l) di soluzione acquosa
positiva, endotermico (la soluzione si raffredda) negativa, esotermico (la soluzione si scalda). DH sol = E ret + E solv concentrazione Molare Esempio: Preparare mezzo litro (0,5 l) di soluzione acquosa
STATICA DEI FLUIDI (Giuseppe Frangiamore con la collaborazione di Michele Sorce)
 STATICA DEI FLUIDI (Giuseppe Frangiamore con la collaborazione di Michele Sorce) Definizione Di Pressione In questo capitolo si analizzeranno le caratteristiche meccaniche dei fluidi in condizioni di equilibrio
STATICA DEI FLUIDI (Giuseppe Frangiamore con la collaborazione di Michele Sorce) Definizione Di Pressione In questo capitolo si analizzeranno le caratteristiche meccaniche dei fluidi in condizioni di equilibrio
PROTEINE E TRASPORTO TRANSMEMBRANALE
 PROTEINE E TRASPORTO TRANSMEMBRANALE Il glucoso ed il galattoso, gli aminoacidi e gli ioni utilizzano apposite proteine per attraversare la MP. L'H 2 O può attraversare con difficoltà lo strato lipidico
PROTEINE E TRASPORTO TRANSMEMBRANALE Il glucoso ed il galattoso, gli aminoacidi e gli ioni utilizzano apposite proteine per attraversare la MP. L'H 2 O può attraversare con difficoltà lo strato lipidico
Elettrochimica. Studia la relazione fra variazione di energia libera e flussi di cariche in una reazione chimica.
 Elettrochimica Studia la relazione fra variazione di energia libera e flussi di cariche in una reazione chimica. Fornisce il modo per ricavare lavoro elettrico da una reazione spontanea = cella galvanica
Elettrochimica Studia la relazione fra variazione di energia libera e flussi di cariche in una reazione chimica. Fornisce il modo per ricavare lavoro elettrico da una reazione spontanea = cella galvanica
4 FORZE FONDAMENTALI
 FORZA 4! QUANTE FORZE? IN NATURA POSSONO ESSERE OSSERVATE TANTE TIPOLOGIE DI FORZE DIVERSE: GRAVITA' O PESO, LA FORZA CHE SI ESERCITA TRA DUE MAGNETI O TRA DUE CORPI CARICHI, LA FORZA DEL VENTO O DELL'ACQUA
FORZA 4! QUANTE FORZE? IN NATURA POSSONO ESSERE OSSERVATE TANTE TIPOLOGIE DI FORZE DIVERSE: GRAVITA' O PESO, LA FORZA CHE SI ESERCITA TRA DUE MAGNETI O TRA DUE CORPI CARICHI, LA FORZA DEL VENTO O DELL'ACQUA
Tensioni e corrente variabili
 Tensioni e corrente variabili Spesso, nella pratica, le tensioni e le correnti all interno di un circuito risultano variabili rispetto al tempo. Se questa variabilità porta informazione, si parla spesso
Tensioni e corrente variabili Spesso, nella pratica, le tensioni e le correnti all interno di un circuito risultano variabili rispetto al tempo. Se questa variabilità porta informazione, si parla spesso
ing. Patrizia Ferrara I Condensatori
 I Condensatori Definizione Il condensatore è un componente elettrico caratterizzato da un ben determinato valore di capacità Struttura I condensatori sono in genere strutturati da 2 superfici parallele
I Condensatori Definizione Il condensatore è un componente elettrico caratterizzato da un ben determinato valore di capacità Struttura I condensatori sono in genere strutturati da 2 superfici parallele
La pressione è una grandezza fisica, definita come il rapporto tra la forza agente normalmente su una superficie e la superficie stessa.
 Pressione La pressione è una grandezza fisica, definita come il rapporto tra la forza agente normalmente su una superficie e la superficie stessa. E originata dallo scambio di forze fra le molecole del
Pressione La pressione è una grandezza fisica, definita come il rapporto tra la forza agente normalmente su una superficie e la superficie stessa. E originata dallo scambio di forze fra le molecole del
Rs Afe. δ1 δ2 δ3 Rs. Vs R1
 Dato il circuito in figura funzionante in regime stazionario, sono noti: Rs = 7.333 Ω, R = 2 Ω, R3 = 7 Ω, δ = mm, δ2 =.3 mm, δ3 =.5 mm, Α = 8 cm 2, N = 00, = 500, V = 30 V. Si consideri la permeabilità
Dato il circuito in figura funzionante in regime stazionario, sono noti: Rs = 7.333 Ω, R = 2 Ω, R3 = 7 Ω, δ = mm, δ2 =.3 mm, δ3 =.5 mm, Α = 8 cm 2, N = 00, = 500, V = 30 V. Si consideri la permeabilità
LA CORRENTE ELETTRICA
 LA CORRENTE ELETTRICA Giuseppe Frangiamore con la collaborazione di Antonino Palumbo Definizione di corrente elettrica La corrente elettrica è un qualsiasi moto ordinato di cariche elettriche, definita
LA CORRENTE ELETTRICA Giuseppe Frangiamore con la collaborazione di Antonino Palumbo Definizione di corrente elettrica La corrente elettrica è un qualsiasi moto ordinato di cariche elettriche, definita
quadrilatero generico parallelogramma rombo rettangolo quadrato
 Pavimentare 1. Quali forme di quadrilateri puoi costruire? Schizza tutte le forme possibili e scrivi il loro nome. 2. Cosa rappresentano i piccoli punti rossi sui lati del quadrilatero? 3. a) Costruisci
Pavimentare 1. Quali forme di quadrilateri puoi costruire? Schizza tutte le forme possibili e scrivi il loro nome. 2. Cosa rappresentano i piccoli punti rossi sui lati del quadrilatero? 3. a) Costruisci
IL LEGAME CHIMICO. Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
 IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
IL LEGAME CIMICO Come dagli atomi si costruiscono le molecole 02/19/08 0959 PM 1 Per descrivere come gli elettroni si distribuiscono nell atomo attorno al nucleo si può far riferimento al MODELLO A GUSCI
LE ASSICURAZIONI VITA
 I PRODOTTI VITA MULTIRAMO Il contesto prolungato di bassi tassi d interesse ha stimolato, non solo in Italia, la ricerca di soluzioni di investimento aggiuntive o alternative alle tradizionali forme di
I PRODOTTI VITA MULTIRAMO Il contesto prolungato di bassi tassi d interesse ha stimolato, non solo in Italia, la ricerca di soluzioni di investimento aggiuntive o alternative alle tradizionali forme di
Studio delle trasformazioni dell energia chimica e dell energia elettrica
 ELETTROCHIMICA Studio delle trasformazioni dell energia chimica e dell energia elettrica Conduttori elettrolitici: soluzioni di acidi, di basi e di sali, nonché sali fusi. Ioni che partecipano alle reazioni
ELETTROCHIMICA Studio delle trasformazioni dell energia chimica e dell energia elettrica Conduttori elettrolitici: soluzioni di acidi, di basi e di sali, nonché sali fusi. Ioni che partecipano alle reazioni
Committente: Crivellari & Zebini SpA Via Roma, Zelo di Giacciano con Baruchella (RO) data: 25/01/2010
 Determinazione dei valori termici di progetto del blocco in laterizio porizzato ZS portante ad incastro 30 x 25 x 19 e di una parete in muratura da esso costituita ai sensi della Norma UNI EN 1745/2005
Determinazione dei valori termici di progetto del blocco in laterizio porizzato ZS portante ad incastro 30 x 25 x 19 e di una parete in muratura da esso costituita ai sensi della Norma UNI EN 1745/2005
Fenomeni magnetici fondamentali
 Fenomeni magnetici fondamentali 1. La forza magnetica e le linee del campo magnetico Già ai tempi di Talete (VI sec. a.c.) era noto che la magnetite, un minerale di ferro, attrae piccoli oggetti di ferro:
Fenomeni magnetici fondamentali 1. La forza magnetica e le linee del campo magnetico Già ai tempi di Talete (VI sec. a.c.) era noto che la magnetite, un minerale di ferro, attrae piccoli oggetti di ferro:
COMPITO A DI CHIMICA DEL 15-09-09
 COMPITO A DI CHIMICA DEL 15-09-09 1A) 3,447 g di anidride arsenica (As 2 O 5 ) solida e 6,278 g di zinco metallico vengono fatti reagire con un eccesso di acido solforico. Si calcoli il volume di arsina
COMPITO A DI CHIMICA DEL 15-09-09 1A) 3,447 g di anidride arsenica (As 2 O 5 ) solida e 6,278 g di zinco metallico vengono fatti reagire con un eccesso di acido solforico. Si calcoli il volume di arsina
Le reazioni redox e l elettrochimica Capitolo 18
 Le reazioni redox e l elettrochimica Capitolo 18 I processi elettrochimici sono reazioni di ossido-riduzione in cui: l energia rilasciata da una reazione spontanea è convertita in elettricità oppure l
Le reazioni redox e l elettrochimica Capitolo 18 I processi elettrochimici sono reazioni di ossido-riduzione in cui: l energia rilasciata da una reazione spontanea è convertita in elettricità oppure l
Misure di ph e titolazione acidobase con metodo potenziometrico
 - Laboratorio di Chimica 1 Misure di ph e titolazione acidobase con metodo potenziometrico PAS A.A. 2013-14 Obiettivi 2 Uso di un ph-metro per la misura del ph Titolazione acido-base: costruzione della
- Laboratorio di Chimica 1 Misure di ph e titolazione acidobase con metodo potenziometrico PAS A.A. 2013-14 Obiettivi 2 Uso di un ph-metro per la misura del ph Titolazione acido-base: costruzione della
Il modello strutturale dell atomo
 Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
Il modello strutturale dell atomo Gli atomi sono costituiti dal nucleo e dagli elettroni Proprietà dell atomo dipendono dal nucleo (fisica nucleare) e dagli elettroni (chimica). Il nucleo contiene protoni
La separazione elettrolitica di un metallo. Scheda di Laboratorio
 La separazione elettrolitica di un metallo Scheda di Laboratorio Premessa Destinatari: classe seconda di un istituto tecnico commerciale, nell insegnamento di scienze della materia. Argomento proposto:
La separazione elettrolitica di un metallo Scheda di Laboratorio Premessa Destinatari: classe seconda di un istituto tecnico commerciale, nell insegnamento di scienze della materia. Argomento proposto:
METODI PER LA MISURA DELLE RESISTENZE. Metodo strumentale.
 METODI PER LA MISURA DELLE RESISTENZE 1)Metodo strumentale. 2)Metodo Volt-Amperometrico. 3)Metodo del ponte di WHEATSTONE. Metodo strumentale. Per metodo strumentale si intende un metodo che prevede l
METODI PER LA MISURA DELLE RESISTENZE 1)Metodo strumentale. 2)Metodo Volt-Amperometrico. 3)Metodo del ponte di WHEATSTONE. Metodo strumentale. Per metodo strumentale si intende un metodo che prevede l
Funzioni goniometriche
 Funzioni goniometriche In questa dispensa vengono introdotte le definizioni delle funzioni goniometriche. Preliminarmente si introducono le convenzioni sull orientazione degli angoli e sulla loro rappresentazione
Funzioni goniometriche In questa dispensa vengono introdotte le definizioni delle funzioni goniometriche. Preliminarmente si introducono le convenzioni sull orientazione degli angoli e sulla loro rappresentazione
Chimica Fisica dei Materiali
 Chimica Fisica dei Materiali Dr. Sergio Brutti Elettrochimica di base Cella elettrochimica Una cella elettrochimica è un dispositivo nel quale l energia elettrica è convertita in energia chimica (e viceversa)
Chimica Fisica dei Materiali Dr. Sergio Brutti Elettrochimica di base Cella elettrochimica Una cella elettrochimica è un dispositivo nel quale l energia elettrica è convertita in energia chimica (e viceversa)
Risultati: Comportamento Statico e Dinamico Del Sistema Muscolo
 Capitolo 3 Risultati: Comportamento Statico e Dinamico Del Sistema Muscolo 47 3.1 Introduzione Il modello è stato validato cercando di replicare una serie di risultati sperimentali riguardanti : i) le
Capitolo 3 Risultati: Comportamento Statico e Dinamico Del Sistema Muscolo 47 3.1 Introduzione Il modello è stato validato cercando di replicare una serie di risultati sperimentali riguardanti : i) le
Lezione 6. Forze attive e passive. L interazione gravitazionale. L interazione elettromagnetica. WWW.SLIDETUBE.IT
 Lezione 6 Forze attive e passive. L interazione gravitazionale. L interazione elettromagnetica. Classificazione delle Forze Distinguiamo tra: Forze attive Forze passive Forze attive Le 4 forze fondamentali:
Lezione 6 Forze attive e passive. L interazione gravitazionale. L interazione elettromagnetica. Classificazione delle Forze Distinguiamo tra: Forze attive Forze passive Forze attive Le 4 forze fondamentali:
La quantità chimica LA MOLE
 La quantità chimica LA MOLE 1 QUANTO PESA UN ATOMO? Se lo misurassimo in grammi, l atomo di H, il più piccolo, avrebbe una massa di 1,6 x10-24 g. Per convenzione, si assegna un valore arbitrario (12) alla
La quantità chimica LA MOLE 1 QUANTO PESA UN ATOMO? Se lo misurassimo in grammi, l atomo di H, il più piccolo, avrebbe una massa di 1,6 x10-24 g. Per convenzione, si assegna un valore arbitrario (12) alla
FOCUS SU EQUILIBRI ACIDO-BASE
 1 Ci sono varie definizioni di acidi e basi, tra le quali meritano di essere ricordate quella di Bronsted e quella di Lewis. Per i nostri fini pratici, ovvero gli esercizi, ci basta però ricordare le definizioni
1 Ci sono varie definizioni di acidi e basi, tra le quali meritano di essere ricordate quella di Bronsted e quella di Lewis. Per i nostri fini pratici, ovvero gli esercizi, ci basta però ricordare le definizioni
Convertitori Tensione / Frequenza. Author: Ing. Sebastiano Giannitto (ITIS M.BARTOLO PACHINO)
 Convertitori Tensione / Frequenza Author: Ing. Sebastiano Giannitto (ITIS M.BARTOLO PACHINO) I convertitori tensione-frequenza (VFC: voltage to frequency converter) sono circuiti elettronici che forniscono
Convertitori Tensione / Frequenza Author: Ing. Sebastiano Giannitto (ITIS M.BARTOLO PACHINO) I convertitori tensione-frequenza (VFC: voltage to frequency converter) sono circuiti elettronici che forniscono
Il trasporto di membrana e le proprietà elettriche delle membrane. www.fisiokinesiterapia.biz
 Il trasporto di membrana e le proprietà elettriche delle membrane www.fisiokinesiterapia.biz Membrana cellulare barriera al passaggio della maggior parte delle molecole polari Permette alla cellula di
Il trasporto di membrana e le proprietà elettriche delle membrane www.fisiokinesiterapia.biz Membrana cellulare barriera al passaggio della maggior parte delle molecole polari Permette alla cellula di
Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da
 Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da acidi forti (solforico, cloridrico e fosforico) prodotti
Le variazioni di ph nei liquidi organici devono mantenute entro limiti molto ristretti (mammiferi tra 6.8 7.8). La stabilità del ph è insidiata da acidi forti (solforico, cloridrico e fosforico) prodotti
EFFETTO MAGNETICO DELLA CORRENTE
 IL CAMPO MAGNETICO E GLI EFFETTI MAGNETICI DELLA CORRENTE 1 EFFETTO MAGNETICO DELLA CORRENTE Ogni conduttore percorso da corrente crea intorno a sé un campo magnetico (H), cioè una perturbazione di tipo
IL CAMPO MAGNETICO E GLI EFFETTI MAGNETICI DELLA CORRENTE 1 EFFETTO MAGNETICO DELLA CORRENTE Ogni conduttore percorso da corrente crea intorno a sé un campo magnetico (H), cioè una perturbazione di tipo
SENSORE PER LA MISURA DEL RUMORE (IL FONOMETRO)
 SENSORE PER LA MISURA DEL RUMORE (IL FONOMETRO) Il fonometro è un dispositivo elettroacustico per la misura del livello di pressione sonora. La sua funzione principale p è quella di convertire un segnale
SENSORE PER LA MISURA DEL RUMORE (IL FONOMETRO) Il fonometro è un dispositivo elettroacustico per la misura del livello di pressione sonora. La sua funzione principale p è quella di convertire un segnale
ESERCITAZIONE 11 SOLUZIONI DI ELETTROLITI
 ESERCITAZIONE 11 SOLUZIONI DI ELETTROLITI Sono elettroliti gli acidi, le basi e i sali. Quando sono in soluzione le loro molecole sono parzialmente o totalmente scisse in particelle dotate di carica (ioni).
ESERCITAZIONE 11 SOLUZIONI DI ELETTROLITI Sono elettroliti gli acidi, le basi e i sali. Quando sono in soluzione le loro molecole sono parzialmente o totalmente scisse in particelle dotate di carica (ioni).
Determinazione del calore di combustione specifico di un pellet vegetale
 Determinazione del calore di combustione specifico di un pellet vegetale La bomba calorimetrica di Mahler è un apparecchio che consente la determinazione del potere calorifico superiore di un combustibile
Determinazione del calore di combustione specifico di un pellet vegetale La bomba calorimetrica di Mahler è un apparecchio che consente la determinazione del potere calorifico superiore di un combustibile
1 L estrazione di radice
 1 L estrazione di radice Consideriamo la potenza 3 2 = 9 di cui conosciamo: Esponente 3 2 = 9 Valore della potenza Base L operazione di radice quadrata consiste nel chiedersi qual è quel numero x che elevato
1 L estrazione di radice Consideriamo la potenza 3 2 = 9 di cui conosciamo: Esponente 3 2 = 9 Valore della potenza Base L operazione di radice quadrata consiste nel chiedersi qual è quel numero x che elevato
Dr. Stefano Sarti Dipartimento di Fisica
 UNIVERSITÀ DI ROMA LA SAPIENZA FACOLTÀ DI INGEGNERIA Corso di Laurea in Ingegneria per l Ambiente e il Territorio ESAME DI FISICA GENERALE II DM 270) Data: 8/9/202. In un disco uniformemente carico di
UNIVERSITÀ DI ROMA LA SAPIENZA FACOLTÀ DI INGEGNERIA Corso di Laurea in Ingegneria per l Ambiente e il Territorio ESAME DI FISICA GENERALE II DM 270) Data: 8/9/202. In un disco uniformemente carico di
pressione esercitata dalle molecole di gas in equilibrio con Si consideri una soluzione di B in A. Per una soluzione ideale
 PROPRIETA COLLIGATIVE Proprietà che dipendono solo dal numero di particelle presenti in soluzione 1. TENSIONE DI VAPORE 2. INNALZAMENTO EBULLIOSCOPICO 3. ABBASSAMENTO CRIOSCOPICO 4. PRESSIONE OSMOTICA
PROPRIETA COLLIGATIVE Proprietà che dipendono solo dal numero di particelle presenti in soluzione 1. TENSIONE DI VAPORE 2. INNALZAMENTO EBULLIOSCOPICO 3. ABBASSAMENTO CRIOSCOPICO 4. PRESSIONE OSMOTICA
Analogamente,sfruttando la variabilità della resistenza in funzione degli sforzi meccanici di trazione o di compressione,si realizzano gli
 SENSORI fig. 7 In un sistema di acquisizione dati i sensori costituiscono le interfacce fisiche tra i dispositivi di elaborazione dei segnali elettrici acquisiti e le corrispondenti grandezze fisiche da
SENSORI fig. 7 In un sistema di acquisizione dati i sensori costituiscono le interfacce fisiche tra i dispositivi di elaborazione dei segnali elettrici acquisiti e le corrispondenti grandezze fisiche da
LE CELLE ELETTROCHIMICHE
 asdf LE CELLE ELETTROCHIMICHE 14 December 2011 Premessa all'articolo In questo articolo ci proponiamo di fare una breve esposizione delle celle elettrochimiche passando per la distinzione tra celle galvaniche
asdf LE CELLE ELETTROCHIMICHE 14 December 2011 Premessa all'articolo In questo articolo ci proponiamo di fare una breve esposizione delle celle elettrochimiche passando per la distinzione tra celle galvaniche
Dipartimento Scientifico-Tecnologico
 ISTITUTO TECNICO STATALE LUIGI STURZO Castellammare di Stabia - NA Anno scolastico 2012-13 Dipartimento Scientifico-Tecnologico CHIMICA, FISICA, SCIENZE E TECNOLOGIE APPLICATE Settore Economico Indirizzi:
ISTITUTO TECNICO STATALE LUIGI STURZO Castellammare di Stabia - NA Anno scolastico 2012-13 Dipartimento Scientifico-Tecnologico CHIMICA, FISICA, SCIENZE E TECNOLOGIE APPLICATE Settore Economico Indirizzi:
BREADBOARD. saldare tutti i collegamenti, rendendo: estremamente laboriosa la modifica dei cablaggi, spesso non riutilizzabile la basetta.
 Breadboard BREADBOARD La costruzione di circuiti elettronici passa spesso per la costruzione di prototipi che possono richiedere più tentativi di cablaggio e messa a punto. Se il circuito prototipo fosse
Breadboard BREADBOARD La costruzione di circuiti elettronici passa spesso per la costruzione di prototipi che possono richiedere più tentativi di cablaggio e messa a punto. Se il circuito prototipo fosse
Fisica II. 3 Esercitazioni
 etem Esercizi svolti Esercizio 3. alcolare le componenti cartesiane del campo elettrico generato da un dipolo p orientato lungo l asse x in un punto lontano rispetto alle dimensioni del dipolo. Soluzione:
etem Esercizi svolti Esercizio 3. alcolare le componenti cartesiane del campo elettrico generato da un dipolo p orientato lungo l asse x in un punto lontano rispetto alle dimensioni del dipolo. Soluzione:
2.11. Misura del potenziale redox Come si misura E h
 Analisi chimica strumentale.11 Misura del potenziale redox Per potenziale redox (o di ossidoriduzione) di una soluzione si intende il potenziale assunto da un elettrodo inerte (in genere, d oro o di platino)
Analisi chimica strumentale.11 Misura del potenziale redox Per potenziale redox (o di ossidoriduzione) di una soluzione si intende il potenziale assunto da un elettrodo inerte (in genere, d oro o di platino)
