Allegato II. Conclusioni scientifiche e motivazioni della variazione dei termini delle autorizzazioni all immissione in commercio
|
|
|
- Albana Dini
- 7 anni fa
- Visualizzazioni
Transcript
1 Allegato II Conclusioni scientifiche e motivazioni della variazione dei termini delle autorizzazioni all immissione in commercio 17
2 Conclusioni scientifiche Sintesi generale della valutazione scientifica su Zinacef e denominazioni associate (Vedere Allegato I) Zinacef contiene cefuroxime sodico, una cefalosporina di seconda generazione. Cefuroxime esercita la sua azione battericida inibendo gli enzimi necessari alla sintesi della parete cellulare batterica (sintesi di peptidoglicani), causando quindi la morte cellulare. Zinacef è stato approvato per la prima volta in Europa all inizio degli anni ottanta ed è disponibile sotto forma di formulazioni parenterali. Zinacef è stato incluso nell elenco dei prodotti per cui deve essere effettuata un armonizzazione dei riassunti delle caratteristiche del prodotto (RCP) in quanto le decisioni nazionali assunte dagli Stati membri relativamente all autorizzazione del prodotto sopra citato sono divergenti. È stato quindi stabilito un deferimento ai sensi dell articolo 30(2) della direttiva 2001/83/CE per risolvere queste divergenze e armonizzare le informazioni sul prodotto in tutta l UE. Paragrafo 4.1 Indicazioni terapeutiche Il CHMP ha osservato l ampio livello di divergenza nelle indicazioni approvate a livello nazionale e ha quindi riesaminato i dati disponibili a supporto di ciascuna indicazione e delle fasce di età dei pazienti. Polmonite comunitaria Il CHMP ha osservato che, sebbene sia stato presentato un solo studio in doppio cieco, sono stati presentati anche diversi altri studi randomizzati e controllati con comparatore, dei quali molti sono stati effettuati recentemente e hanno mostrato un efficacia adeguata di cefuroxime. Il CHMP ha quindi concluso che vi sono dati sufficienti a supporto dell indicazione negli adulti e che i dati di efficacia negli adulti possono essere estrapolati alla popolazione pediatrica. Il CHMP ha considerato l indicazione accettabile per tutte le popolazioni. Esacerbazioni acute della bronchite cronica Il CHMP ha esaminato lo studio randomizzato, comparativo, in doppio cieco, presentato e ne ha considerato adeguato il disegno. Poiché lo studio ha dimostrato la non inferiorità di cefuroxime, il CHMP ha considerato l indicazione accettabile. Infezioni del tratto respiratorio superiore Il CHMP ha considerato la dicitura dell'indicazione proposta troppo generale e ha osservato che la maggior parte delle infezioni del tratto respiratorio superiore risponde bene alla terapia orale o si risolve spontaneamente. Il CHMP ha riesaminato gli studi clinici presentati ma ha considerato i dati insufficienti. Il CHMP ha anche osservato che non sono disponibili studi comparativi, controllati verso placebo o in doppio cieco per l indicazione relativa a infezioni gravi di orecchio, naso e gola. Il CHMP ha quindi raccomandato la rimozione di questa indicazione. Infezioni del tratto urinario Il CHMP ha considerato i dati presentati, costituiti da undici piccoli studi non comparativi e due studi comparativi in aperto. Il CHMP ha osservato l ampia esperienza clinica a supporto dell uso di cefuroxime per questa indicazione. Il CHMP ha anche osservato che esistono poche opzioni terapeutiche disponibili per le donne in gravidanza affette da pielonefrite. Concludendo, il CHMP ha considerato accettabile l indicazione infezioni complicate del tratto urinario, compresa la pielonefrite. Infezioni cutanee e dei tessuti molli Il CHMP ha riesaminato i dati presentati e ha concordato che gli stafilococchi e gli streptococchi, le specie batteriche più frequentemente coinvolte nelle infezioni cutanee e dei tessuti molli, sono sensibili a cefuroxime. In base ai dati forniti, il CHMP ha considerato accettabile l indicazione infezioni dei tessuti molli: celluliti, erisipele e infezioni di ferite. Infezioni delle ossa e delle articolazioni 18
3 Dopo aver riesaminato i dati disponibili, costituiti da piccoli studi non comparativi, il CHMP ha considerato tali dati molto limitati e dalla metodologia discutibile. Il CHMP ha considerato che i dati sulla penetrazione ossea non bilanciano la mancanza di dati clinici a supporto. Il CHMP ha quindi raccomandato la rimozione di questa indicazione. Infezioni ostetriche e ginecologiche Il CHMP ha riesaminato i due studi in aperto presentati ma ha affermato che cefuroxime non è attivo nei confronti di molte delle specie batteriche isolate nelle infezioni ostetriche e ginecologiche, a causa di resistenze intrinseche o di resistenze acquisite. Il CHMP ha considerato questa indicazione non adeguatamente supportata e ha quindi raccomandato la sua rimozione. Gonorrea Il CHMP ha riesaminato gli studi presentati, la maggioranza dei quali ha impiegato cefuroxime in associazione a probenecid e non in monoterapia. Il CHMP ha anche osservato che, sebbene il patogeno coesistente più frequentemente nei pazienti affetti da gonorrea sia Chlamydia trachomatis, non sono stati presentati dati sulla terapia di associazione (cefuroxime con altri antibiotici) per il trattamento dei pazienti coinfettati da N. gonorrhoeae e C. trachomatis, o da N. gonorrhoeae e batteri anaerobi. Il CHMP ha considerato che i dati disponibili non supportano tale indicazione e ha quindi raccomandato la sua rimozione. Setticemia e meningite Il CHMP ha riesaminato gli studi sulla setticemia che erano datati, non comparativi e includevano un numero limitato di pazienti. Gli studi sono stati condotti in un periodo in cui la resistenza acquisita non rappresentava un problema fondamentale. Per quanto riguarda la meningite, il CHMP ha osservato che la maggior parte degli studi aveva identificato H. influenzae, N. meningitidis, S. pneumonia e S. aureus (non-mrsa) come le specie batteriche predominanti, il che non rispecchia la situazione europea attuale, in cui i batteri aerobi Gram-negativi sono sempre più importanti come agenti causali. Il CHMP ha concluso che i dati clinici e i dati del Comitato europeo sui test di suscettibilità antimicrobica (EUCAST) non supportavano il trattamento della meningite. Concludendo, il CHMP ha giudicato i dati insufficienti per supportare le indicazioni di setticemia e meningite e ha quindi raccomandato la loro rimozione. Infezioni intraddominali Il CHMP ha riesaminato i dati presentati e ha considerato che la distribuzione delle infezioni nei due più ampi studi presentati può supportare l indicazione proposta, anche se cefuroxime non è adatto al trattamento delle infezioni causate da batteri Gram-negativi non fermentanti. Concludendo, il CHMP ha considerato accettabile l indicazione. Profilassi Dopo aver riesaminato tutti i dati presentati a supporto delle varie indicazioni profilattiche proposte per cefuroxime, il CHMP ha considerato accettabile l indicazione Profilassi delle infezioni in chirurgia gastrointestinale (inclusa la chirurgia esofagea), ortopedica, cardiovascolare e ginecologica (incluso il taglio cesareo)". Indicazione nei neonati Il CHMP ha riesaminato i dati sui neonati, inclusi i dati sull intervallo posologico e l intervallo tra le somministrazioni. Il CHMP ha definito i neonati come bambini di età inferiore a 3 settimane, inclusi i bambini appena nati, e ha concordato che cefuroxime è stato utilizzato per molti anni nei neonati senza alcun problema grave di sicurezza. Il CHMP ha concordato che ai neonati può essere somministrata una dose giornaliera totale simile a quella raccomandata per i lattanti (da 30 a 100 mg/kg/giorno) ma a una frequenza giornaliera ridotta di 2 o 3 dosi suddivise, a causa della maggiore emivita sierica. Concludendo, il CHMP ha adottato le seguenti indicazioni armonizzate e la seguente formulazione del paragrafo 4.1: 19
4 Zinacef è indicato per il trattamento delle infezioni sotto elencate negli adulti e nei bambini, inclusi i neonati (dal momento della nascita) (vedere paragrafi 4.4 e 5.1). Polmonite comunitaria. Esacerbazioni acute della bronchite cronica. Infezioni complicate del tratto urinario, inclusa pielonefrite. Infezioni dei tessuti molli: celluliti, erisipele e infezioni delle ferite. Infezioni intraddominali (vedere paragrafo 4.4). Profilassi delle infezioni in chirurgia gastrointestinale (inclusa chirurgia esofagea), ortopedica, cardiovascolare e ginecologica (incluso taglio cesareo). Nel trattamento e nella prevenzione di infezioni in cui è molto probabile che si riscontrino organismi anaerobi, cefuroxime deve essere somministrato insieme ad altri medicinali antibatterici appropriati. Si devono prendere in considerazione le indicazioni ufficiali sull'uso appropriato dei medicinali antibatterici. Paragrafo 4.2 Posologia e modo di somministrazione Il CHMP ha osservato l ampio livello di divergenza nelle posologie e nelle raccomandazioni approvate a livello nazionale e ha quindi riesaminato i dati disponibili a supporto del paragrafo armonizzato 4.2. Il CHMP ha riesaminato le raccomandazioni posologiche per ciascuna indicazione. Il CHMP ha concordato che i regimi posologici endovenosi e intramuscolari comunemente utilizzati (ad es. da 750 mg a 1500 mg ogni 8 ore) dovrebbero dimostrarsi efficaci nei confronti di organismi con concentrazioni inibitorie minime (MIC) pari o inferiori a 8 μg/ml. Il CHMP ha considerato che per il cefuroxime somministrato per via parenterale, i batteri meno suscettibili includono principalmente Enterobacteriaceae (cioè E. coli, P. mirabilis e Klebsiella spp). Il CHMP ha quindi concordato con i punti di rottura dell'eucast per le Enterobacteriaceae (pari a 8 μg/ml) per raccomandare un regime posologico di 1500 mg ogni 8 ore per il trattamento delle infezioni causate dai batteri di cui sopra. Il CHMP ha raccomandato la rimozione dell opzione rappresentata da una terapia sequenziale parenterale-orale per tutti i pazienti, a causa della riduzione significativa dell esposizione al farmaco attivo con il passaggio alla formulazione orale. Per quanto riguarda i pazienti con compromissione della funzionalità renale, il CHMP ha riesaminato i dati e ha considerato accettabili le linee guida proposte per la posologia. Per i pazienti con compromissione della funzionalità epatica, il CHMP ha dichiarato che la disfunzione epatica non dovrebbe influenzare la farmacocinetica di cefuroxime. Per quanto riguarda il modo di somministrazione, il CHMP ha dichiarato che Zinacef deve essere somministrato mediante iniezione endovenosa per un periodo di 3-5 minuti direttamente in una vena o attraverso un tubo di gocciolamento o mediante infusione di minuti o mediante iniezione intramuscolare. Concludendo, il CHMP ha adottato una formulazione armonizzata del paragrafo 4.2. Divergenze minori in altri paragrafi del RCP, dell etichettatura e del foglio illustrativo Il CHMP ha anche adottato una formulazione armonizzata per i rimanenti paragrafi del RCP di Zinacef e ha adeguato l etichettatura e il foglio illustrativo al RCP armonizzato adottato. Motivazioni della modifica del riassunto delle caratteristiche del prodotto, dell etichettatura e del foglio illustrativo La ragione della procedura di deferimento era l armonizzazione del riassunto delle caratteristiche del prodotto, dell etichettatura e del foglio illustrativo. Dopo aver considerato i dati presentati dal titolare dell autorizzazione all immissione in commercio, le relazioni di valutazione del relatore e del co-relatore e le discussioni scientifiche all interno del Comitato, il CHMP ha ritenuto che il rapporto rischi-benefici di Zinacef e denominazioni associate è favorevole. Tenendo conto che: 20
5 Il Comitato ha preso in considerazione il deferimento ai sensi dell articolo 30 della direttiva 2001/83/CE Il Comitato ha preso in considerazione le divergenze identificate per Zinacef e denominazioni associate relativamente ai paragrafi riguardanti le indicazioni terapeutiche, la posologia e i modi di somministrazione, oltre ai restanti paragrafi del RCP Il Comitato ha riesaminato i dati presentati dal titolare dell autorizzazione all immissione in commercio, inclusi i dati di studi clinici, la letteratura pubblicata e la documentazione clinica, che giustificano le informazioni sul prodotto armonizzate proposte Il Comitato ha concordato con l armonizzazione del riassunto delle caratteristiche del prodotto, dell etichettatura e del foglio illustrativo proposto dai titolari dell autorizzazione all immissione in commercio, il CHMP ha raccomandato la variazione dei termini delle autorizzazioni all immissione in commercio per le quali il riassunto delle caratteristiche del prodotto, l'etichettatura e il foglio illustrativo sono definiti nell'allegato III di Zinacef e denominazioni associate (vedere Allegato I). 21
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) Agosto 2012 Comunicazione diretta agli operatori sanitari sull associazione tra
I medici non devono più prescrivere medicinali contenenti calcitonina in forma di spray nasale per il trattamento dell'osteoporosi.
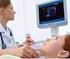 20 Luglio 2012 EMA/CHMP/483874/2012 L Agenzia Europea del Medicinali raccomanda la limitazione dell uso a lungo termine di medicinali a base di calcitonina Ritiro della formulazione intranasale per il
20 Luglio 2012 EMA/CHMP/483874/2012 L Agenzia Europea del Medicinali raccomanda la limitazione dell uso a lungo termine di medicinali a base di calcitonina Ritiro della formulazione intranasale per il
Conclusioni scientifiche
 Allegato II Conclusioni scientifiche e motivi per la modifica del riassunto delle caratteristiche del prodotto, dell etichettatura e del foglio illustrativo presentati dall Agenzia europea per i medicinali
Allegato II Conclusioni scientifiche e motivi per la modifica del riassunto delle caratteristiche del prodotto, dell etichettatura e del foglio illustrativo presentati dall Agenzia europea per i medicinali
Allegato II. Conclusioni scientifiche e motivi della variazione dei termini dell autorizzazione all'immissione in commercio
 Allegato II Conclusioni scientifiche e motivi della variazione dei termini dell autorizzazione all'immissione in commercio 11 Conclusioni scientifiche Riassunto generale della valutazione scientifica di
Allegato II Conclusioni scientifiche e motivi della variazione dei termini dell autorizzazione all'immissione in commercio 11 Conclusioni scientifiche Riassunto generale della valutazione scientifica di
Allegato II. Conclusioni scientifiche
 Allegato II Conclusioni scientifiche 5 Conclusioni scientifiche Beclometasone dipropionato (BDP) è un glucocorticoide e un profarmaco del metabolita attivo, beclometasone-17-monopropionato. Il beclometasone
Allegato II Conclusioni scientifiche 5 Conclusioni scientifiche Beclometasone dipropionato (BDP) è un glucocorticoide e un profarmaco del metabolita attivo, beclometasone-17-monopropionato. Il beclometasone
SINTESI GENERALE DELLA VALUTAZIONE SCIENTIFICA DI AUGMENTIN E DENOMINAZIONI ASSOCIATE (V. ALLEGATO I)
 ALLEGATO II CONCLUSIONI SCIENTIFICHE E MOTIVI DELLA MODIFICA DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, DELL ETICHETTATURA E DEL FOGLIO ILLUSTRATIVO PRESENTATI DALL EMEA 23 CONCLUSIONI SCIENTIFICHE
ALLEGATO II CONCLUSIONI SCIENTIFICHE E MOTIVI DELLA MODIFICA DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, DELL ETICHETTATURA E DEL FOGLIO ILLUSTRATIVO PRESENTATI DALL EMEA 23 CONCLUSIONI SCIENTIFICHE
Il pediatra di famiglia nell approccio alle infezioni respiratorie nella pratica quotidiana. Massimo Landi Pediatria di gruppo - Torino
 Il pediatra di famiglia nell approccio alle infezioni respiratorie nella pratica quotidiana Massimo Landi Pediatria di gruppo - Torino Rapporto pediatria 2003 Campione Arno Dei 645 principi attivi i primi
Il pediatra di famiglia nell approccio alle infezioni respiratorie nella pratica quotidiana Massimo Landi Pediatria di gruppo - Torino Rapporto pediatria 2003 Campione Arno Dei 645 principi attivi i primi
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA)
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Comunicazione diretta agli operatori sanitari relativa a reazioni avverse gravi conseguenti
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Comunicazione diretta agli operatori sanitari relativa a reazioni avverse gravi conseguenti
Obiettivo della terapia è guarire l infezione in atto in collaborazione col sistema immunocompetente.
 La profilassi non è una terapia Anna Maria Marata La profilassi non è una terapia Obiettivo della terapia è guarire l infezione in atto in collaborazione col sistema immunocompetente. Obiettivo della profilassi
La profilassi non è una terapia Anna Maria Marata La profilassi non è una terapia Obiettivo della terapia è guarire l infezione in atto in collaborazione col sistema immunocompetente. Obiettivo della profilassi
TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE
 FARMACOVIGILANZA TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono
FARMACOVIGILANZA TIMECEF 1 G/4 ML POLVERE E SOLVENTE PER SOLUZIONE INIETTABILE PER USO INTRAMUSCOLARE Variazioni degli stampati relativamente agli aspetti della sicurezza Le modifiche agli stampati sono
Allegato III. Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo
 Allegato III Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo Nota: Il Riassunto delle caratteristiche del prodotto, l'etichettatura e il foglio
Allegato III Emendamenti ai paragrafi pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio Illustrativo Nota: Il Riassunto delle caratteristiche del prodotto, l'etichettatura e il foglio
Conclusioni scientifiche
 ALLEGATO II CONCLUSIONI SCIENTIFICHE E MOTIVI PER LA RICHIESTA DI MODIFICA DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, DELL'ETICHETTATURA E DEL FOGLIO ILLUSTRATIVO PRESENTATA DALL'AGENZIA EUROPEA
ALLEGATO II CONCLUSIONI SCIENTIFICHE E MOTIVI PER LA RICHIESTA DI MODIFICA DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, DELL'ETICHETTATURA E DEL FOGLIO ILLUSTRATIVO PRESENTATA DALL'AGENZIA EUROPEA
Farmaci biologici nel trattamento della psoriasi: differenze nei criteri di valutazione tra USA e UE.
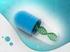 Farmaci biologici nel trattamento della psoriasi: differenze nei criteri di valutazione tra USA e UE. Renato Bertini Malgarini, Giuseppe Pimpinella, Luca Pani 10 dicembre 2012- Istituto Superiore di Sanità
Farmaci biologici nel trattamento della psoriasi: differenze nei criteri di valutazione tra USA e UE. Renato Bertini Malgarini, Giuseppe Pimpinella, Luca Pani 10 dicembre 2012- Istituto Superiore di Sanità
RACCOMANDAZIONI AZIENDALI SULLA PROFILASSI ANTIMICROBICA IN CHIRURGIA
 Presidio Ospedaliero Nord Servizio di Farmacia Tel.: 0773/6553077-6553076- Fax.: 0773/6553074. Latina, 20/11/2006 RACCOMANDAZIONI AZIENDALI SULLA PROFILASSI ANTIMICROBICA IN CHIRURGIA La profilassi chirurgica
Presidio Ospedaliero Nord Servizio di Farmacia Tel.: 0773/6553077-6553076- Fax.: 0773/6553074. Latina, 20/11/2006 RACCOMANDAZIONI AZIENDALI SULLA PROFILASSI ANTIMICROBICA IN CHIRURGIA La profilassi chirurgica
Allegato II. Conclusioni scientifiche e motivi della variazione dei termini dell autorizzazione all immissione in commercio
 Allegato II Conclusioni scientifiche e motivi della variazione dei termini dell autorizzazione all immissione in commercio 7 Conclusioni scientifiche Riassunto generale della valutazione scientifica di
Allegato II Conclusioni scientifiche e motivi della variazione dei termini dell autorizzazione all immissione in commercio 7 Conclusioni scientifiche Riassunto generale della valutazione scientifica di
Allegato II. Conclusioni scientifiche e motivi per il parere favorevole
 Allegato II Conclusioni scientifiche e motivi per il parere favorevole 3 Conclusioni scientifiche Riassunto generale della valutazione scientifica di Tobramycin VVB e denominazioni associate (vedere Allegato
Allegato II Conclusioni scientifiche e motivi per il parere favorevole 3 Conclusioni scientifiche Riassunto generale della valutazione scientifica di Tobramycin VVB e denominazioni associate (vedere Allegato
Presentazione dei dati
 Presentazione dei dati Per ogni principio attivo, per il quale è stato possibile reperire informazioni riguardanti il passaggio nel latte materno, è stata creata una scheda monografica con informazioni
Presentazione dei dati Per ogni principio attivo, per il quale è stato possibile reperire informazioni riguardanti il passaggio nel latte materno, è stata creata una scheda monografica con informazioni
SINTESI GENERALE DELLA VALUTAZIONE SCIENTIFICA DI LOSEC E DENOMINAZIONI ASSOCIATE (VEDERE ALLEGATO I)
 ALLEGATO II CONCLUSIONI SCIENTIFICHE E MOTIVI DELLA MODIFICA DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, DELL ETICHETTATURA E DEL FOGLIO ILLUSTRATIVO PRESENTATI DALL EMEA 20 CONCLUSIONI SCIENTIFICHE
ALLEGATO II CONCLUSIONI SCIENTIFICHE E MOTIVI DELLA MODIFICA DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, DELL ETICHETTATURA E DEL FOGLIO ILLUSTRATIVO PRESENTATI DALL EMEA 20 CONCLUSIONI SCIENTIFICHE
Allegato II. Conclusioni scientifiche e motivi della variazione dei termini delle autorizzazioni all immissione in commercio
 Allegato II Conclusioni scientifiche e motivi della variazione dei termini delle autorizzazioni all immissione in commercio 20 Conclusioni scientifiche Riassunto generale della valutazione scientifica
Allegato II Conclusioni scientifiche e motivi della variazione dei termini delle autorizzazioni all immissione in commercio 20 Conclusioni scientifiche Riassunto generale della valutazione scientifica
AIFA - Agenzia Italiana del Farmaco
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Luglio 2013 Restrizione della popolazione target e limitazione della durata del trattamento
LA SCELTA DEI FARMACI empirica e razionale. Mariateresa Sasanelli
 LA SCELTA DEI FARMACI empirica e razionale Mariateresa Sasanelli Premessa La terapia empirica Perché utilizzare un antibiotico in un animale malato? Il paziente ha una infezione batterica trattabile? Il
LA SCELTA DEI FARMACI empirica e razionale Mariateresa Sasanelli Premessa La terapia empirica Perché utilizzare un antibiotico in un animale malato? Il paziente ha una infezione batterica trattabile? Il
RoActemra. tocilizumab. Che cos è RoActemra? Per che cosa si usa RoActemra? Riassunto destinato al pubblico
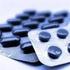 EMA/18167/2014 EMEA/H/C/000955 Riassunto destinato al pubblico tocilizumab Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
EMA/18167/2014 EMEA/H/C/000955 Riassunto destinato al pubblico tocilizumab Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
Allegato III. Modifiche ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo
 Allegato III Modifiche ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Queste modifiche ai paragrafi pertinenti del Riassunto delle Caratteristiche
Allegato III Modifiche ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Queste modifiche ai paragrafi pertinenti del Riassunto delle Caratteristiche
Antibatterici attivi sulla sintesi degli acidi nucleici
 Antibiotici Antibatterici attivi sulla sintesi degli acidi nucleici Chinoloni Cumarine Inibitori della diidrofolato reduttasi Sulfonamidi Rifamicine Inibitori della sintesi proteica Tetracicline Macrolidi
Antibiotici Antibatterici attivi sulla sintesi degli acidi nucleici Chinoloni Cumarine Inibitori della diidrofolato reduttasi Sulfonamidi Rifamicine Inibitori della sintesi proteica Tetracicline Macrolidi
01.0 DENOMINAZIONE DEL MEDICINALE 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA
 01.0 DENOMINAZIONE DEL MEDICINALE AUREOMICINA 3% Unguento Tubo 14,2 g 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 g di unguento contiene: Principio attivo: Clortetraciclina cloridrato mg 30 03.0 FORMA
01.0 DENOMINAZIONE DEL MEDICINALE AUREOMICINA 3% Unguento Tubo 14,2 g 02.0 COMPOSIZIONE QUALITATIVA E QUANTITATIVA 1 g di unguento contiene: Principio attivo: Clortetraciclina cloridrato mg 30 03.0 FORMA
Conclusioni scientifiche e motivi delle conclusioni
 Allegato II Conclusioni scientifiche e motivi della variazione dei termini delle autorizzazioni all immissione in commercio e spiegazione dettagliata delle differenze rispetto alla raccomandazione del
Allegato II Conclusioni scientifiche e motivi della variazione dei termini delle autorizzazioni all immissione in commercio e spiegazione dettagliata delle differenze rispetto alla raccomandazione del
Prima dei 15 anni il dosaggio di paracetamolo dipende dal peso del bambino e deve essere compreso tra i 10 e i 15 mg/kg/dose; l intervallo tra una
 1 2 Prima dei 15 anni il dosaggio di paracetamolo dipende dal peso del bambino e deve essere compreso tra i 10 e i 15 mg/kg/dose; l intervallo tra una dose e l altra deve essere sempre almeno di 4 ore.
1 2 Prima dei 15 anni il dosaggio di paracetamolo dipende dal peso del bambino e deve essere compreso tra i 10 e i 15 mg/kg/dose; l intervallo tra una dose e l altra deve essere sempre almeno di 4 ore.
Allegato III Modifiche al riassunto delle caratteristiche del prodotto e al foglio illustrativo
 Allegato III Modifiche al riassunto delle caratteristiche del prodotto e al foglio illustrativo Nota: le modifiche di questo riassunto delle caratteristiche del prodotto e del foglio illustrativo sono
Allegato III Modifiche al riassunto delle caratteristiche del prodotto e al foglio illustrativo Nota: le modifiche di questo riassunto delle caratteristiche del prodotto e del foglio illustrativo sono
Scelta dei farmaci antimicrobici
 Antibiotici Gram + Gram - Scelta dei farmaci antimicrobici Identita agente infettante Sensibilita ad un dato farmaco Sede dell infezione Fattori legati al paziente Sicurezza della terapia Costo della terapia
Antibiotici Gram + Gram - Scelta dei farmaci antimicrobici Identita agente infettante Sensibilita ad un dato farmaco Sede dell infezione Fattori legati al paziente Sicurezza della terapia Costo della terapia
AIFA Agenzia Italiana Del Farmaco Nota Informnativa Importante su Tachipirina e Medicinali Contenenti Paracetamolo da Solo e/o in Associazione
 AIFA - Tachipirina e Paracetamolo 20/01/2010 (Livello 2) AIFA Agenzia Italiana Del Farmaco Nota Informnativa Importante su Tachipirina e Medicinali Contenenti Paracetamolo da Solo e/o in Associazione Nota
AIFA - Tachipirina e Paracetamolo 20/01/2010 (Livello 2) AIFA Agenzia Italiana Del Farmaco Nota Informnativa Importante su Tachipirina e Medicinali Contenenti Paracetamolo da Solo e/o in Associazione Nota
AZIENDA OSPEDALIERA S. CROCE E CARLE - CUNEO. Il protocollo vaccinale per la malattia invasiva da Streptococcus pneumoniae
 AZIENDA OSPEDALIERA S. CROCE E CARLE - CUNEO Il protocollo vaccinale per la malattia invasiva da Streptococcus pneumoniae A cura del C.I.O. (C. Bonada, P.Pellegrino, G. Raineri) giugno 2015 Condizioni
AZIENDA OSPEDALIERA S. CROCE E CARLE - CUNEO Il protocollo vaccinale per la malattia invasiva da Streptococcus pneumoniae A cura del C.I.O. (C. Bonada, P.Pellegrino, G. Raineri) giugno 2015 Condizioni
Farmaci utilizzati nelle malattie infettive
 Farmaci utilizzati nelle malattie infettive Concetti generali β-lattamine Ott 2002 Concetti generali Antibiosi, antibiotici Effetto batteriostatico / battericida Spettro d azione Resistenza Rapporto sito
Farmaci utilizzati nelle malattie infettive Concetti generali β-lattamine Ott 2002 Concetti generali Antibiosi, antibiotici Effetto batteriostatico / battericida Spettro d azione Resistenza Rapporto sito
LA PROFILASSI ANTIBIOTICA PERI-OPERATORIA
 LA PROFILASSI ANTIBIOTICA PERI-OPERATORIA Dott.ssa A. Passariello Coordinamento Farmaceutico Ospedaliero ex Ce1 PROFILASSI PERI-OPERATORIA La somministrazione di chemioterapici secondo modalità ben definite,
LA PROFILASSI ANTIBIOTICA PERI-OPERATORIA Dott.ssa A. Passariello Coordinamento Farmaceutico Ospedaliero ex Ce1 PROFILASSI PERI-OPERATORIA La somministrazione di chemioterapici secondo modalità ben definite,
Le terapia della CAP secondo LG. Oreste CAPELLI, M.D.
 Le terapia della CAP secondo LG Oreste CAPELLI, M.D. LG ATS/IDSA (2007) e BTS (2009) Eziologia della CAP Sia per i pazienti trattati a domicilio che per i pazienti ricoverati l agente eziologico più frequente
Le terapia della CAP secondo LG Oreste CAPELLI, M.D. LG ATS/IDSA (2007) e BTS (2009) Eziologia della CAP Sia per i pazienti trattati a domicilio che per i pazienti ricoverati l agente eziologico più frequente
Sintesi generale della valutazione scientifica dei medicinali contenenti nimesulide (formulazioni sistemiche) (cfr. allegato I)
 Allegato II Conclusioni scientifiche e motivi della modifica del riassunto delle caratteristiche del prodotto, dell etichettatura e del foglio illustrativo presentati dall EMA 41 Conclusioni scientifiche
Allegato II Conclusioni scientifiche e motivi della modifica del riassunto delle caratteristiche del prodotto, dell etichettatura e del foglio illustrativo presentati dall EMA 41 Conclusioni scientifiche
CEFODIE Cefonicid. Categoria farmacoterapeutica Antibiotico iniettabile.
 Foglio illustrativo CEFODIE Cefonicid Denominazione del medicinale CEFODIE 500 mg/2 ml polvere e solvente per soluzione iniettabile per uso intramuscolare. CEFODIE 1 g/2,5 ml polvere e solvente per soluzione
Foglio illustrativo CEFODIE Cefonicid Denominazione del medicinale CEFODIE 500 mg/2 ml polvere e solvente per soluzione iniettabile per uso intramuscolare. CEFODIE 1 g/2,5 ml polvere e solvente per soluzione
Allegato. Modifiche alle specifiche sezioni del Riassunto delle caretteristiche del prodotto e del foglio illustrativo
 Allegato Modifiche alle specifiche sezioni del Riassunto delle caretteristiche del prodotto e del foglio illustrativo Nota: Il Riassunto delle caratteristiche del prodotto, l'etichettatura e il foglio
Allegato Modifiche alle specifiche sezioni del Riassunto delle caretteristiche del prodotto e del foglio illustrativo Nota: Il Riassunto delle caratteristiche del prodotto, l'etichettatura e il foglio
vaccino pneumococcico polisaccaridico coniugato (13-valente, adsorbito)
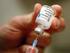 EMA/90006/2015 EMEA/H/C/001104 Riassunto destinato al pubblico vaccino pneumococcico polisaccaridico coniugato (13-valente, adsorbito) Questo è il riassunto della relazione pubblica europea di valutazione
EMA/90006/2015 EMEA/H/C/001104 Riassunto destinato al pubblico vaccino pneumococcico polisaccaridico coniugato (13-valente, adsorbito) Questo è il riassunto della relazione pubblica europea di valutazione
LO STREPTOCOCCO AGALACTIAE IN
 LO STREPTOCOCCO AGALACTIAE IN GRAVIDANZA: FATTORI DI RISCHIO E RESISTENZE AGLI ANTIBIOTICI. Chiara Matani Alice Matteini Marco Tanini Corrado Catalani I STUDIO Studio di prevalenza della resistenza di
LO STREPTOCOCCO AGALACTIAE IN GRAVIDANZA: FATTORI DI RISCHIO E RESISTENZE AGLI ANTIBIOTICI. Chiara Matani Alice Matteini Marco Tanini Corrado Catalani I STUDIO Studio di prevalenza della resistenza di
Gli antibiotici in medicina generale
 Gli antibiotici in medicina generale Anna Maria Marata Olbia 11 ottobre 2008 gli antibiotici quale posto nella prescrizione territoriale? Rapporto OSMED 2007: www.agenziafarmaco.it la prescrizione nella
Gli antibiotici in medicina generale Anna Maria Marata Olbia 11 ottobre 2008 gli antibiotici quale posto nella prescrizione territoriale? Rapporto OSMED 2007: www.agenziafarmaco.it la prescrizione nella
GAZZETTA UFFICIALE DELLA REPUBBLICA ITALIANA Serie generale n. 115
 AGENZIA ITALIANA DEL FARMACO DETERMINAZIONE 9 Maggio 2007 Modifica degli stampati dei medicinali contenenti farmaci antinfiammatori non steroidei (FANS) non selettivi per uso sistemico - ATC M01A. omissis
AGENZIA ITALIANA DEL FARMACO DETERMINAZIONE 9 Maggio 2007 Modifica degli stampati dei medicinali contenenti farmaci antinfiammatori non steroidei (FANS) non selettivi per uso sistemico - ATC M01A. omissis
Dati microbiologici I semestre Azienda Ospedaliera S.Orsola-Malpighi AREA INTERNISTICA
 Dati microbiologici I semestre 2015 Azienda Ospedaliera S.Orsola-Malpighi AREA INTERNISTICA Dott. Simone Ambretti U.O.Microbiologia simone.ambretti@aosp.bo.it Come interpretare i dati TIPI DI TABELLE 1.
Dati microbiologici I semestre 2015 Azienda Ospedaliera S.Orsola-Malpighi AREA INTERNISTICA Dott. Simone Ambretti U.O.Microbiologia simone.ambretti@aosp.bo.it Come interpretare i dati TIPI DI TABELLE 1.
Allegato II. Conclusioni scientifiche e motivazioni per la variazione dei termini delle autorizzazioni all immissione in commercio
 Allegato II Conclusioni scientifiche e motivazioni per la variazione dei termini delle autorizzazioni all immissione in commercio 7 Conclusioni scientifiche Introduzione Flolan contiene epoprostenolo sodico,
Allegato II Conclusioni scientifiche e motivazioni per la variazione dei termini delle autorizzazioni all immissione in commercio 7 Conclusioni scientifiche Introduzione Flolan contiene epoprostenolo sodico,
Allegato II. Conclusioni scientifiche e motivi per il rifiuto presentati dall Agenzia europea per i medicinali
 Allegato II Conclusioni scientifiche e motivi per il rifiuto presentati dall Agenzia europea per i medicinali 5 Conclusioni scientifiche Riassunto generale della valutazione scientifica di etinilestradiolo-drospirenone
Allegato II Conclusioni scientifiche e motivi per il rifiuto presentati dall Agenzia europea per i medicinali 5 Conclusioni scientifiche Riassunto generale della valutazione scientifica di etinilestradiolo-drospirenone
Via polmonare Via trans mucosa Distribuzione dei farmaci Biotrasformazione dei farmaci Che caratteristiche hanno gli enzimi? Eliminazione dei farmaci
 Indice Prefazione di Sergio Bova 1 CONCETTI INTRODUTTIVI Terminologia essenziale Origine dei farmaci Nomi dei farmaci Tutti i farmaci sono potenzialmente tossici per l organismo Uso terapeutico della tossina
Indice Prefazione di Sergio Bova 1 CONCETTI INTRODUTTIVI Terminologia essenziale Origine dei farmaci Nomi dei farmaci Tutti i farmaci sono potenzialmente tossici per l organismo Uso terapeutico della tossina
HALT 2. Health-care associated infections and antimicrobial use in European Long-term care facilities. 1 Prof.ssa Carla M. Zotti
 HALT 2 Health-care associated infections and antimicrobial use in European Long-term care facilities Dott.ssa 1 Michela Stillo Prof.ssa Carla M. Zotti Andamento della popolazione giovane e anziana nel
HALT 2 Health-care associated infections and antimicrobial use in European Long-term care facilities Dott.ssa 1 Michela Stillo Prof.ssa Carla M. Zotti Andamento della popolazione giovane e anziana nel
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Afugerm 2% crema 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni grammo contiene 20 mg di acido fusidico. Eccipienti: La crema
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO 1. DENOMINAZIONE DEL MEDICINALE Afugerm 2% crema 2. COMPOSIZIONE QUALITATIVA E QUANTITATIVA Ogni grammo contiene 20 mg di acido fusidico. Eccipienti: La crema
Approccio Terapeutico all iperglicemia a digiuno e postprandiale. Irene Brandolin S.C. Medicina Interna E.O. Ospedali Galliera Savona, 23 Marzo 2013
 Approccio Terapeutico all iperglicemia a digiuno e postprandiale Irene Brandolin S.C. Medicina Interna E.O. Ospedali Galliera Savona, 23 Marzo 2013 La triade glicemica nella gestione del diabete Glicemia
Approccio Terapeutico all iperglicemia a digiuno e postprandiale Irene Brandolin S.C. Medicina Interna E.O. Ospedali Galliera Savona, 23 Marzo 2013 La triade glicemica nella gestione del diabete Glicemia
Gli Italiani, gli antibiotici l antibioticoresistenza
 Gli Italiani, gli antibiotici l antibioticoresistenza Roma, 11 novembre 2007 Conferenza stampa Auditorium Lungotevere Ripa Ministero del Lavoro, della Salute e delle Politiche Sociali La Giornata Europea
Gli Italiani, gli antibiotici l antibioticoresistenza Roma, 11 novembre 2007 Conferenza stampa Auditorium Lungotevere Ripa Ministero del Lavoro, della Salute e delle Politiche Sociali La Giornata Europea
Meningite Cosa c è da sapere.
 Meningite Cosa c è da sapere www.salute.gov.it Ecco dieci cose da sapere sulla meningite in Italia, soprattutto sulla forma più aggressiva, quella di natura batterica, e sulle vaccinazioni disponibili
Meningite Cosa c è da sapere www.salute.gov.it Ecco dieci cose da sapere sulla meningite in Italia, soprattutto sulla forma più aggressiva, quella di natura batterica, e sulle vaccinazioni disponibili
RIASSUNTO GENERALE DELLA VALUTAZIONE SCIENTIFICA DI PROTIUM E DENOMINAZIONI ASSOCIATE (VEDERE ALLEGATO I)
 ALLEGATO II CONCLUSIONI SCIENTIFICHE E MOTIVI DELLA MODIFICA DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, DELL ETICHETTATURA E DEL FOGLIO ILLUSTRATIVO PRESENTATI DALL EMEA 21 CONCLUSIONI SCIENTIFICHE
ALLEGATO II CONCLUSIONI SCIENTIFICHE E MOTIVI DELLA MODIFICA DEL RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, DELL ETICHETTATURA E DEL FOGLIO ILLUSTRATIVO PRESENTATI DALL EMEA 21 CONCLUSIONI SCIENTIFICHE
RICERCA E SVILUPPO DI NUOVI FARMACI
 RICERCA E SVILUPPO DI NUOVI FARMACI In passato le scoperte dei farmaci erano occasionali. Si trattava di sostanze di derivazione vegetale o animale STRATEGIE DI RICERCA: Quali sono i fattori che influenzano
RICERCA E SVILUPPO DI NUOVI FARMACI In passato le scoperte dei farmaci erano occasionali. Si trattava di sostanze di derivazione vegetale o animale STRATEGIE DI RICERCA: Quali sono i fattori che influenzano
Il trattamento con EXJADE deve essere iniziato e mantenuto da medici esperti nel trattamento del sovraccarico cronico di ferro.
 A LLEGATO Inserimento, in accordo all articolo 12, comma 5 della Legge 189/2012, in apposita sezione (denominata Classe C (nn)) dedicata ai farmaci non ancora valutati ai fini della rimborsabilità nelle
A LLEGATO Inserimento, in accordo all articolo 12, comma 5 della Legge 189/2012, in apposita sezione (denominata Classe C (nn)) dedicata ai farmaci non ancora valutati ai fini della rimborsabilità nelle
UNIVERSITA DEGLI STUDI DI PALERMO FACOLTA DI MEDICINA E CHIRURGIA
 UNIVERSITA DEGLI STUDI DI PALERMO FACOLTA DI MEDICINA E CHIRURGIA CDL IN TECNICHE DI LABORATORIO BIOMEDICO (abilitante all esercizio della professione di Tecnico di Laboratorio Biomedico) Presidente: Prof.
UNIVERSITA DEGLI STUDI DI PALERMO FACOLTA DI MEDICINA E CHIRURGIA CDL IN TECNICHE DI LABORATORIO BIOMEDICO (abilitante all esercizio della professione di Tecnico di Laboratorio Biomedico) Presidente: Prof.
Allegato II. Conclusioni scientifiche e motivi della variazione dei termini dell'autorizzazione all'immissione in commercio
 Allegato II Conclusioni scientifiche e motivi della variazione dei termini dell'autorizzazione all'immissione in commercio 10 Conclusioni scientifiche Sintesi generale della valutazione scientifica di
Allegato II Conclusioni scientifiche e motivi della variazione dei termini dell'autorizzazione all'immissione in commercio 10 Conclusioni scientifiche Sintesi generale della valutazione scientifica di
Raccomandazioni più stringenti sul rischio di gravi reazioni da ipersensibilità con Rienso (ferumoxitolo)*
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) 31gennaio 2014 Raccomandazioni più stringenti sul rischio di gravi reazioni da
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON L AGENZIA EUROPEA DEI MEDICINALI (EMA) E L AGENZIA ITALIANA DEL FARMACO (AIFA) 31gennaio 2014 Raccomandazioni più stringenti sul rischio di gravi reazioni da
Humira. adalimumab. Che cos è Humira? Per che cosa si usa Humira? Riassunto destinato al pubblico
 EMA/65420/2013 EMEA/H/C/000481 Riassunto destinato al pubblico adalimumab Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
EMA/65420/2013 EMEA/H/C/000481 Riassunto destinato al pubblico adalimumab Questo è il riassunto della relazione pubblica europea di valutazione (EPAR) per. Illustra il modo in cui il comitato per i medicinali
SCHEDA DI VALUTAZIONE PER L INSERIMENTO DI FARMACI NON PRESENTI NEL PTR DAPTOMICINA
 RICHIESTA DI INSERIMENTO IN PTR DI ATC J01XX09 (CUBICIN ) Presentata da : Commissione Prontuario terapeutico provinciale Cagliari In data novembre 2007 Per le seguenti motivazioni : La daptomicina possiede
RICHIESTA DI INSERIMENTO IN PTR DI ATC J01XX09 (CUBICIN ) Presentata da : Commissione Prontuario terapeutico provinciale Cagliari In data novembre 2007 Per le seguenti motivazioni : La daptomicina possiede
Foglio illustrativo: informazioni per il paziente
 Foglio illustrativo: informazioni per il paziente Enterogermina 2 miliardi / 5 ml sospensione orale Enterogermina 2 miliardi capsule rigide Spore di Bacillus clausii poliantibiotico resistente Uso orale
Foglio illustrativo: informazioni per il paziente Enterogermina 2 miliardi / 5 ml sospensione orale Enterogermina 2 miliardi capsule rigide Spore di Bacillus clausii poliantibiotico resistente Uso orale
Risk Management e Antibiotico terapia
 P.O. San Francesco Nuoro Risk Management e Antibiotico terapia Antonio M. Pinna Risk Manager Errori di terapia Ogni evento prevenibile nel quale l uso di un farmaco ha dato come risultato un effetto indesiderato
P.O. San Francesco Nuoro Risk Management e Antibiotico terapia Antonio M. Pinna Risk Manager Errori di terapia Ogni evento prevenibile nel quale l uso di un farmaco ha dato come risultato un effetto indesiderato
AIFA - Agenzia Italiana del Farmaco
 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) 31 gennaio 2011 Importanti informazioni di sicurezza su Optimark (gadoversetamide) e fibrosi
NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITÀ REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) 31 gennaio 2011 Importanti informazioni di sicurezza su Optimark (gadoversetamide) e fibrosi
AIFA - Agenzia Italiana del Farmaco
 Giugno 2013 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Limitazioni all uso di TROBALT (retigabina) il trattamento può comportare
Giugno 2013 NOTA INFORMATIVA IMPORTANTE CONCORDATA CON LE AUTORITA REGOLATORIE EUROPEE E L AGENZIA ITALIANA DEL FARMACO (AIFA) Limitazioni all uso di TROBALT (retigabina) il trattamento può comportare
Meningite Cosa c è da sapere.
 Meningite Cosa c è da sapere www.salute.gov.it Ecco dieci cose da sapere sulla meningite in Italia, soprattutto sulla forma più aggressiva, quella di natura batterica, e sulle vaccinazioni disponibili
Meningite Cosa c è da sapere www.salute.gov.it Ecco dieci cose da sapere sulla meningite in Italia, soprattutto sulla forma più aggressiva, quella di natura batterica, e sulle vaccinazioni disponibili
AIFA Agenzia Italiana del Farmaco Benfluorex
 AIFA - Benfluorex 18/12/2009 (Livello 2) AIFA Agenzia Italiana del Farmaco Benfluorex Comunicato EMEA Domande e Risposte (FAQ) file:///c /documenti/ben950.htm [18/12/2009 15.50.04] 18 December 2009 EMA/CHM/815033/2009
AIFA - Benfluorex 18/12/2009 (Livello 2) AIFA Agenzia Italiana del Farmaco Benfluorex Comunicato EMEA Domande e Risposte (FAQ) file:///c /documenti/ben950.htm [18/12/2009 15.50.04] 18 December 2009 EMA/CHM/815033/2009
RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO
 1. DENOMINAZIONE DEL MEDICINALE RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO CEFTRIAXONE DOC Generici 500 mg/2 ml polvere e solvente per soluzione iniettabile per uso intramuscolare. CEFTRIAXONE DOC Generici
1. DENOMINAZIONE DEL MEDICINALE RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO CEFTRIAXONE DOC Generici 500 mg/2 ml polvere e solvente per soluzione iniettabile per uso intramuscolare. CEFTRIAXONE DOC Generici
L UTILITÀ E I LIMITI DEL VACCINO PNEUMOCOCCICO MULTIVALENTE IN ETÀ ADULTA E PEDIATRICA
 L UTILITÀ E I LIMITI DEL VACCINO PNEUMOCOCCICO MULTIVALENTE IN ETÀ ADULTA E PEDIATRICA ORDINE DEI MEDICI DI TORINO SALA RIVA ROCCI TORINO, 5 OTTOBRE 2006 CHE COSA DICE LA LETTERATURA? LA VACCINAZIONE
L UTILITÀ E I LIMITI DEL VACCINO PNEUMOCOCCICO MULTIVALENTE IN ETÀ ADULTA E PEDIATRICA ORDINE DEI MEDICI DI TORINO SALA RIVA ROCCI TORINO, 5 OTTOBRE 2006 CHE COSA DICE LA LETTERATURA? LA VACCINAZIONE
AULA ROSSA STUDI CLINICI IN CORSO
 Terza Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche AULA ROSSA STUDI CLINICI IN CORSO Che cosa è uno studio clinico e a cosa serve? Si definisce sperimentazione clinica,
Terza Giornata Fiorentina dedicata ai pazienti con malattie mieloproliferative croniche AULA ROSSA STUDI CLINICI IN CORSO Che cosa è uno studio clinico e a cosa serve? Si definisce sperimentazione clinica,
N cartella N ricovero Cognome Nome Data di nascita DICHIARAZIONE DI AVVENUTA INFORMAZIONE ED ESPRESSIONE DEL CONSENSO A TRATTAMENTO CHEMIOTERAPICO
 Io sottoscritto/a, nato/a il a nel pieno possesso delle mie facoltà dichiaro di essere stato/a informato/a in modo dettagliato, chiaro e comprensibile, dal Dottor, sui seguenti punti: 1. diagnosi : La
Io sottoscritto/a, nato/a il a nel pieno possesso delle mie facoltà dichiaro di essere stato/a informato/a in modo dettagliato, chiaro e comprensibile, dal Dottor, sui seguenti punti: 1. diagnosi : La
Allegato III. Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo
 Allegato III Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Gli emendamenti al riassunto delle caratteristiche del prodotto e al foglio
Allegato III Emendamenti ai paragrafi pertinenti del riassunto delle caratteristiche del prodotto e del foglio illustrativo Nota: Gli emendamenti al riassunto delle caratteristiche del prodotto e al foglio
A. ETICHETTATURA TEMPLATE ETICHETTA/FOGLIO ILLUSTRATIVO
 A. ETICHETTATURA TEMPLATE ETICHETTA/FOGLIO ILLUSTRATIVO (Tutte le confezioni registrate in Italia presentano un unico template contenente tutte le informazioni previste dal foglio illustrativo ed etichetta)
A. ETICHETTATURA TEMPLATE ETICHETTA/FOGLIO ILLUSTRATIVO (Tutte le confezioni registrate in Italia presentano un unico template contenente tutte le informazioni previste dal foglio illustrativo ed etichetta)
CLORAMFENICOLO. Isolato per la prima volta nel 1947 da un ceppo di Streptomyces venezuelae
 CLRAMFEICL Isolato per la prima volta nel 1947 da un ceppo di Streptomyces venezuelae Cl 2 C C 136 D(-) treo attivo 2 D(-) treo-1-(p-nitrofenil)-2-dicloroacetamido-1,3-propandiolo Cl 2 C C 2 136 D(-) treo
CLRAMFEICL Isolato per la prima volta nel 1947 da un ceppo di Streptomyces venezuelae Cl 2 C C 136 D(-) treo attivo 2 D(-) treo-1-(p-nitrofenil)-2-dicloroacetamido-1,3-propandiolo Cl 2 C C 2 136 D(-) treo
Chemioterapici antibatterici e antibiotici
 Chemioterapici antibatterici e antibiotici Farmacologia Speciale Paziente infetto Strategia terapeutica campione per identificazione e sensibilità Risposta laboratorio con le sensibilità Terapia empirica
Chemioterapici antibatterici e antibiotici Farmacologia Speciale Paziente infetto Strategia terapeutica campione per identificazione e sensibilità Risposta laboratorio con le sensibilità Terapia empirica
MEDICINALI PER USO UMANO- APPROVATI CON PROCEDURA CENTRALIZZATA IL DIRETTORE GENERALE
 1+99 /2014 l CLASSIFICAZIONE Al SENSI DELL'ART.12 COMMA 5 LEGGE 8 NOVEMBRE 2012 N. 189 DI MEDICINALI PER USO UMANO- APPROVATI CON PROCEDURA CENTRALIZZATA IL DIRETTORE GENERALE Visti gli articoli 8 e 9
1+99 /2014 l CLASSIFICAZIONE Al SENSI DELL'ART.12 COMMA 5 LEGGE 8 NOVEMBRE 2012 N. 189 DI MEDICINALI PER USO UMANO- APPROVATI CON PROCEDURA CENTRALIZZATA IL DIRETTORE GENERALE Visti gli articoli 8 e 9
Dati microbiologici I semestre Azienda Ospedaliera S.Orsola-Malpighi AREA PEDIATRICA
 Dati microbiologici I semestre 2015 Azienda Ospedaliera S.Orsola-Malpighi AREA PEDIATRICA Dott. Simone Ambretti U.O.Microbiologia simone.ambretti@aosp.bo.it Come interpretare i dati 2 TIPI DI TABELLE 1.
Dati microbiologici I semestre 2015 Azienda Ospedaliera S.Orsola-Malpighi AREA PEDIATRICA Dott. Simone Ambretti U.O.Microbiologia simone.ambretti@aosp.bo.it Come interpretare i dati 2 TIPI DI TABELLE 1.
Il bambino con disordine funzionale gastrointestinale
 Il bambino con disordine funzionale gastrointestinale (vomito ricorrente, probabile o improbabile reflusso gastroesofageo, dolore addominale ricorrente, sindrome dell intestino irritabile) Dalla letteratura:
Il bambino con disordine funzionale gastrointestinale (vomito ricorrente, probabile o improbabile reflusso gastroesofageo, dolore addominale ricorrente, sindrome dell intestino irritabile) Dalla letteratura:
Allegato III. Emendamenti alle sezioni pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio illustrativo
 Allegato III Emendamenti alle sezioni pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio illustrativo Nota: Il Riassunto delle Caratteristiche del Prodotto, l etichettatura e il foglio
Allegato III Emendamenti alle sezioni pertinenti del Riassunto delle Caratteristiche del Prodotto e del Foglio illustrativo Nota: Il Riassunto delle Caratteristiche del Prodotto, l etichettatura e il foglio
Prof.ssa D. De Vito Ordinario di Igiene Università degli Studi di Bari
 Prof.ssa D. De Vito Ordinario di Igiene Università degli Studi di Bari Meticillina Meropenem Penicillina G Amoxicillina Ciprofloxacina Invasione batterica delle vie urinarie inferiori I batteri possono
Prof.ssa D. De Vito Ordinario di Igiene Università degli Studi di Bari Meticillina Meropenem Penicillina G Amoxicillina Ciprofloxacina Invasione batterica delle vie urinarie inferiori I batteri possono
Allegato II. Conclusioni scientifiche e motivazioni della sospensione delle autorizzazioni all immissione in commercio
 Allegato II Conclusioni scientifiche e motivazioni della sospensione delle autorizzazioni all immissione in commercio 8 Conclusioni scientifiche Sintesi generale della valutazione scientifica di prodotti
Allegato II Conclusioni scientifiche e motivazioni della sospensione delle autorizzazioni all immissione in commercio 8 Conclusioni scientifiche Sintesi generale della valutazione scientifica di prodotti
 SCHEDA PER LA PRESCRIZIONE DI ENBREL nella PSORIASI Farmaco H REGIONE LAZIO Paziente (Nome /Cognome) Codice Fiscale Data di Nascita sesso M F Regione di residenza dell assistito Azienda USL Domicilio:
SCHEDA PER LA PRESCRIZIONE DI ENBREL nella PSORIASI Farmaco H REGIONE LAZIO Paziente (Nome /Cognome) Codice Fiscale Data di Nascita sesso M F Regione di residenza dell assistito Azienda USL Domicilio:
Studio Specialistico di Otorinolaringoiatria del Dott. Fabio Colaboni. Via Suor Maria Mazzarello 31 Roma Tel.: 06/
 Studio Specialistico di Otorinolaringoiatria del Dott. Fabio Colaboni Via Suor Maria Mazzarello 31 Roma Tel.: 06/7880547 Antibiotici Si/No - Quando Come - Quali - Per quanto tempo Gli antibiotici sono
Studio Specialistico di Otorinolaringoiatria del Dott. Fabio Colaboni Via Suor Maria Mazzarello 31 Roma Tel.: 06/7880547 Antibiotici Si/No - Quando Come - Quali - Per quanto tempo Gli antibiotici sono
Documento PTR n. 119 relativo a:
 Direzione Generale Sanità e Politiche Sociali Commissione Regionale del Farmaco (D.G.R. 1540/2006, 2129/2010 e 490/2011) Documento PTR n. 119 relativo a: MEDICINALI ORIGINATOR E BIOSIMILARI DELL ERITROPOIETINA
Direzione Generale Sanità e Politiche Sociali Commissione Regionale del Farmaco (D.G.R. 1540/2006, 2129/2010 e 490/2011) Documento PTR n. 119 relativo a: MEDICINALI ORIGINATOR E BIOSIMILARI DELL ERITROPOIETINA
Dott.. EMILIO MONTALDO IL MEDICO DI MEDICINA GENERALE E L INFLUENZA PANDEMICA
 Dott.. EMILIO MONTALDO IL MEDICO DI MEDICINA GENERALE E L INFLUENZA PANDEMICA LA GESTIONE DELL INFLUENZA 1) TEST RAPIDO 2) USO DI ANTIVIRALI 3) USO DI ANTIBIOTICI 4) USO DI ANTINFIAMMATORI/ANTIPIRETICI
Dott.. EMILIO MONTALDO IL MEDICO DI MEDICINA GENERALE E L INFLUENZA PANDEMICA LA GESTIONE DELL INFLUENZA 1) TEST RAPIDO 2) USO DI ANTIVIRALI 3) USO DI ANTIBIOTICI 4) USO DI ANTINFIAMMATORI/ANTIPIRETICI
Le sostanze candidate alla sostituzione e la valutazione comparativa degli agrofarmaci
 Le sostanze candidate alla sostituzione e la valutazione comparativa degli agrofarmaci La legislazione dei prodotti fitosanitari Regolamento 1107/2009 sull immissione sul mercato dei prodotti fitosanitari
Le sostanze candidate alla sostituzione e la valutazione comparativa degli agrofarmaci La legislazione dei prodotti fitosanitari Regolamento 1107/2009 sull immissione sul mercato dei prodotti fitosanitari
Tutto sull amoxicillina
 Tutto sull amoxicillina Dr.ssa Garazzino Silvia SC Pediatria 2U, Università degli Studi di Torino AO Città della Salute e della Scienza di Torino Presidio Ospedale Infantile Regina Margherita Lancet Infect
Tutto sull amoxicillina Dr.ssa Garazzino Silvia SC Pediatria 2U, Università degli Studi di Torino AO Città della Salute e della Scienza di Torino Presidio Ospedale Infantile Regina Margherita Lancet Infect
Modalità di presentazione e tipologia dei dati da inserire nelle banche dati per il monitoraggio della terapia genica e cellulare somatica
 Modalità di presentazione e tipologia dei dati da inserire nelle banche dati per il monitoraggio della terapia genica e cellulare somatica IL PRESIDENTE DELL ISTITUTO SUPERIORE DI SANITÀ VISTO il decreto
Modalità di presentazione e tipologia dei dati da inserire nelle banche dati per il monitoraggio della terapia genica e cellulare somatica IL PRESIDENTE DELL ISTITUTO SUPERIORE DI SANITÀ VISTO il decreto
Importante!! I m.o. patogeni responsabili di I.O. sono nel 70% dei casi resistenti a uno o più antibiotici
 La maggior parte delle infezioni della ferita chirurgica viene acquisita durante l intervento: se una ferita è pulita e asciutta, infatti, nell arco di poche ore dall intervento non è più suscettibile
La maggior parte delle infezioni della ferita chirurgica viene acquisita durante l intervento: se una ferita è pulita e asciutta, infatti, nell arco di poche ore dall intervento non è più suscettibile
Questa tabella riporta le principali classi di FANS e le rispettive molecole di riferimento.
 1 2 Questa tabella riporta le principali classi di FANS e le rispettive molecole di riferimento. 3 Per quanto la classe dei FANS sia molto ampia e articolata, come si evince da questa tabella, il loro
1 2 Questa tabella riporta le principali classi di FANS e le rispettive molecole di riferimento. 3 Per quanto la classe dei FANS sia molto ampia e articolata, come si evince da questa tabella, il loro
ALLEGATO III RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, ETICHETTATURA E FOGLIO ILLUSTRATIVO
 ALLEGATO III RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, ETICHETTATURA E FOGLIO ILLUSTRATIVO Nota: il presente riassunto delle caratteristiche del prodotto, l etichettatura e il foglio illustrativo rispecchiano
ALLEGATO III RIASSUNTO DELLE CARATTERISTICHE DEL PRODOTTO, ETICHETTATURA E FOGLIO ILLUSTRATIVO Nota: il presente riassunto delle caratteristiche del prodotto, l etichettatura e il foglio illustrativo rispecchiano
MODELLO DI COMUNICAZIONE AL RICHIEDENTE DELLA DECISIONE DEL COMITATO ETICO RELATIVA AL PARERE UNICO 1
 Appendice 6 MODELLO DI COMUNICAZIONE AL RICHIEDENTE DELLA DECISIONE DEL COMITATO ETICO RELATIVA AL PARERE UNICO 1 Il presente parere del comitato etico è stato compilato e stampato dal sito internet dell
Appendice 6 MODELLO DI COMUNICAZIONE AL RICHIEDENTE DELLA DECISIONE DEL COMITATO ETICO RELATIVA AL PARERE UNICO 1 Il presente parere del comitato etico è stato compilato e stampato dal sito internet dell
MODULO PER LA RICHIESTA DI INSERIMENTO IN PRONTUARIO ASL AL
 Sede legale: Viale Giolitti,2 15033 Casale Monferrato (AL) Partita IVA/Codice Fiscale n. 02190140067 Alla Segreteria Scientifica della COMMISSIONE TERAPEUTICA AZIENDALE Presidente Dr.ssa Elide AZZAN Te.
Sede legale: Viale Giolitti,2 15033 Casale Monferrato (AL) Partita IVA/Codice Fiscale n. 02190140067 Alla Segreteria Scientifica della COMMISSIONE TERAPEUTICA AZIENDALE Presidente Dr.ssa Elide AZZAN Te.
FOGLIETTO ILLUSTRATIVO. Baytril flavour 25 mg/ml sospensione orale per gatti
 FOGLIETTO ILLUSTRATIVO Baytril flavour 25 mg/ml sospensione orale per gatti 1. NOME E INDIRIZZO DEL TITOLARE DELL'AUTORIZZAZIONE ALL'IMMISSIONE IN COMMERCIO E NOME E INDIRIZZO DEL TITOLARE DELL AUTORIZZAZIONE
FOGLIETTO ILLUSTRATIVO Baytril flavour 25 mg/ml sospensione orale per gatti 1. NOME E INDIRIZZO DEL TITOLARE DELL'AUTORIZZAZIONE ALL'IMMISSIONE IN COMMERCIO E NOME E INDIRIZZO DEL TITOLARE DELL AUTORIZZAZIONE
Allegato II. Conclusioni scientifiche
 Allegato II Conclusioni scientifiche 26 Conclusioni scientifiche Informazioni generali Il cerotto transdermico Durogesic contiene fentanil, un potente analgesico oppiaceo sintetico appartenente ai derivati
Allegato II Conclusioni scientifiche 26 Conclusioni scientifiche Informazioni generali Il cerotto transdermico Durogesic contiene fentanil, un potente analgesico oppiaceo sintetico appartenente ai derivati
I CARDINI DELLA TERAPIA ANTIBIOTICA
 I CARDINI DELLA TERAPIA ANTIBIOTICA Quali sono le regole fondamentali che tutti i medici dovrebbero sapere sugli antibiotici? Il limite della maggior parte dei testi di antibioticoterapia è quello di perdersi
I CARDINI DELLA TERAPIA ANTIBIOTICA Quali sono le regole fondamentali che tutti i medici dovrebbero sapere sugli antibiotici? Il limite della maggior parte dei testi di antibioticoterapia è quello di perdersi
VARICELLA SCHEDA INFORMATIVA PER PERSONALE INFIERMERISTICO E AUSILIARIO WHAT YOU NEED TO KNOW
 VARICELLA SCHEDA INFORMATIVA PER PERSONALE INFIERMERISTICO E AUSILIARIO WHAT YOU NEED TO KNOW SEI SICURO DI USARE MISURE DI PREVENZIONE ADEGUATE PER PROTEGGERTI DALLA VARICELLA? INFORMATI! VACCINATI! PROTETTI!
VARICELLA SCHEDA INFORMATIVA PER PERSONALE INFIERMERISTICO E AUSILIARIO WHAT YOU NEED TO KNOW SEI SICURO DI USARE MISURE DI PREVENZIONE ADEGUATE PER PROTEGGERTI DALLA VARICELLA? INFORMATI! VACCINATI! PROTETTI!
Dati microbiologici I semestre Azienda Ospedaliera S.Orsola-Malpighi
 Dati microbiologici I semestre 2016 Azienda Ospedaliera S.Orsola-Malpighi AREA CHIRURGICA Dott. Simone Ambretti U.O.Microbiologia simone.ambretti@aosp.bo.it Come interpretare i dati TIPI DI TABELLE 1.
Dati microbiologici I semestre 2016 Azienda Ospedaliera S.Orsola-Malpighi AREA CHIRURGICA Dott. Simone Ambretti U.O.Microbiologia simone.ambretti@aosp.bo.it Come interpretare i dati TIPI DI TABELLE 1.
Dati microbiologici I semestre Azienda Ospedaliera S.Orsola-Malpighi AREA CRITICA
 Dati microbiologici I semestre 2015 Azienda Ospedaliera S.Orsola-Malpighi AREA CRITICA Dott. Simone Ambretti U.O.Microbiologia simone.ambretti@aosp.bo.it Come interpretare i dati TIPI DI TABELLE 1. TABELLA
Dati microbiologici I semestre 2015 Azienda Ospedaliera S.Orsola-Malpighi AREA CRITICA Dott. Simone Ambretti U.O.Microbiologia simone.ambretti@aosp.bo.it Come interpretare i dati TIPI DI TABELLE 1. TABELLA
Sicurezza e utilità dei fitoterapici in età pediatrica. Introduce Donatella Del Gaizo
 Sicurezza e utilità dei fitoterapici in età pediatrica Introduce Donatella Del Gaizo Premessa La Fitoterapia è una disciplina scientifica che definisce, con criteri scientifici rigorosi, l utilizzo delle
Sicurezza e utilità dei fitoterapici in età pediatrica Introduce Donatella Del Gaizo Premessa La Fitoterapia è una disciplina scientifica che definisce, con criteri scientifici rigorosi, l utilizzo delle
1,2 mg + 70 mg pastiglie con vitamina C 2,4 diclorobenzil alcool, acido ascorbico
 1,2 mg + 70 mg pastiglie con vitamina C 2,4 diclorobenzil alcool, acido ascorbico Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni per lei. Usi
1,2 mg + 70 mg pastiglie con vitamina C 2,4 diclorobenzil alcool, acido ascorbico Legga attentamente questo foglio prima di usare questo medicinale perché contiene importanti informazioni per lei. Usi
Supplemento ordinario n. 210 alla GAZZETTA UFFICIALE Serie generale - n. 202
 Supplemento ordinario n. 210 alla GZZETT UFFICILE Serie generale - n. 202 DETERMINZIONE 6 agosto 2010. Regime di rimborsabilità e prezzo di vendita del medicinale «ranesp» (darbepoetina alfa) - autorizzata
Supplemento ordinario n. 210 alla GZZETT UFFICILE Serie generale - n. 202 DETERMINZIONE 6 agosto 2010. Regime di rimborsabilità e prezzo di vendita del medicinale «ranesp» (darbepoetina alfa) - autorizzata
Il consumo di antibiotici in Europa, in Italia, in Emilia-Romagna Carlo Gagliotti - ASSR Emilia-Romagna
 Il consumo di antibiotici in Europa, in Italia, in Emilia-Romagna Carlo Gagliotti - ASSR Emilia-Romagna Appropriatezza nell antibioticoterapia Convegno SIMPIOS - Baggiovara 8 Marzo 2011 Fonti informative
Il consumo di antibiotici in Europa, in Italia, in Emilia-Romagna Carlo Gagliotti - ASSR Emilia-Romagna Appropriatezza nell antibioticoterapia Convegno SIMPIOS - Baggiovara 8 Marzo 2011 Fonti informative
