Tutte le reazioni che avvengono nelle cellule sono reazioni catalizzate I catalizzatori di tali reazioni prendono il nome di enzimi Gli enzimi sono
|
|
|
- Rita Novelli
- 8 anni fa
- Visualizzazioni
Transcript
1 Tutte le reazioni che avvengono nelle cellule sono reazioni catalizzate I catalizzatori di tali reazioni prendono il nome di enzimi Gli enzimi sono grosse molecole proteine e ribozimi (RNA)
2 TEORIA DELLE COLLISIONI H la velocità di una reazione, misurata come quantità di prodotto ottenuto in un tempo definito, dipende dalla energia di attivazione l energia di attivazione è l energia necessaria per: allineare i gruppi reagenti formare cariche transitorie instabili riorganizzare legami operare tutte le trasformazioni necessarie per far avvenire una reazione gli enzimi modificano solo la velocità della reazione e non gli equilibri
3 L energia di attivazione può essere abbassata aggiungendo un catalizzatore In presenza di un catalizzatore, la reazione raggiunge l equilibrio molto più rapidamente perché la velocità della reazione è molto superiore alla norma. La reazione è scomposta in più tappe caratterizzate da valori di G* inferiori nelle quali si ha formazione e scomparsa di specie chimiche transitorie (ES, EP)
4 DIFFERENZE TRA ENZIMI E CATALIZZATORI INORGANICI Peso molecolare I catalizzatori chimici sono composti molto semplici spesso anche semplici atomi, mentre gli enzimi sono molecole proteiche e, quindi, espressione dei geni. Sono caratterizzati da un peso molecolare molto alto. Capacità di regolazione: controllo allosterico; modificazione covalente degli enzimi; variazione della quantità di enzima sintetizzato Specificità Capacità catalitica Diversamente dai catalizzatori inorganici che catalizzano numerose reazioni anche molto diverse tra loro, gli enzimi sono altamente specifici. La maggior parte di enzimi agisce su di un unico substrato o su un numero molto limitato di composti. Gli enzimi accelerano le reazioni da un milione fino a volte.
5 Caratteristiche enzimi 1. La maggior parte sono proteine che svolgono un attività catalitica nei sistemi biologici accelerando le reazioni ( volte) 2. Ogni cellula contiene alcune migliaia di enzimi diversi e sono localizzati in determinati punti della cellula a seconda della funzione da svolgere 3. Sono altamente specifici 4. Non influenzano l equilibrio di una reazione chimica 5. Sono efficaci in piccole quantità, e funzionano anche dopo essere stati estratti da essa 6. Ogni enzima ha una capacità catalitica espressa dal numero di turnover cioè dal numero di molecole di substrato che viene convertito in prodotto nell unità di tempo da una singola molecola enzimatica in condizioni ideali
6 Capacità catalitica:
7 SPECIFICITA DEGLI ENZIMI S intende la discriminazione che un enzima opera tra diversi substrati in competizione per il sito attivo Assoluta, l enzima catalizza solo una reazione; (glucochinasi: fosforila solo glucosio) Di gruppo, l enzima catalizza substrati con lo stesso gruppo funzionale (esochinasi: fosforila glucosio, mannosio e fruttosio) Di legame, la capacità di riconoscere un tipo particolare di legame (peptidica, acetalico, estereo) Stereospecificità, la capacità di ottenere un solo stereoisomero
8 Classificazione internazionale degli enzimi: a ciascun enzima viene assegnato un numero di classificazione composto di quattro numeri (EC: Enzyme Commission) oppure un nome sistematico che ne identifichi la reazione catalizzata 1 ossidoreduttasi: trasferimento di elettroni 2 transferasi: trasferimento di gruppi funzionali da una molecola ad un'altra 3 idrolasi: reazioni di idrolisi 4 liasi: reazioni di addizione o eliminazione di piccole molecole (CO 2 e H 2 O) 5 isomerasi: reazioni di trasformazione di una molecola nel suo isomero 6 ligasi: reazioni endoergoniche in cui 2 molecole sono unite tra loro
9
10 Per esempio, l'enzima tripeptide amminopeptidasi ha EC i cui numeri indicano: Classe 3: il primo numero identifica la reazione catalizzata dall'enzima: enzimi della famiglia delle idrolasi; Sottoclasse 4: il secondo numero identifica il tipo di legame: idrolasi che agiscono su un legame peptidico Sotto-sottoclasse 11: il terzo numero identifica il tipo di substrato: idrolasi che agiscono su un legame peptidico di un tripeptide Numero seriale 4: indica numero di serie dell'enzima: la posizione dell enzima nella sotto sotto-classe
11 Struttura ENZIMI MONOMERICI: costituiti da una sola catena peptidica (subunità). Ne sono noti pochi (pepsina, tripsina, elastasi, carbossipeptidasi, trombina (E proteolitici), ribonucleasi, lisozima ENZIMI OLIGOMERICI: costituiti da 2 o più subunità, che possono essere uguali o diverse Proteine semplici Proteine coniugate possiedono un gruppo chimico legato alla proteina (gruppo prostetico in maniera covalente) per catalizzare una reazione, in quanto i residui AA non funzionano Proteina coniugata (oloenzima)= apoenzima+cofattore Apoenzima: parte proteica Cofattore: parte non proteica costituita da ioni metallici (Cu, K, Na, Zn, Mg) e altre molecole organiche derivate da vitamine idrosolubili dette coenzimi
12 SITO ATTIVO Gli enzimi sono delle proteine molte grosse pero solo una piccola zona (tasche, fessure, pieghe, solchi) è coinvolta: tale zona è chiamata sito attivo Il sito attivo ha due componenti: il sito catalitico, dove per mezzo dei gruppi R degli amminoacidi avviene la reazione e il sito di legame, dove il substrato si sistema per subire poi la reazione.
13 L enzima si combina chimicamente col substrato Il sito di legame tiene unito il substrato con legami deboli Riconoscimento complementarità per Il substrato viene riconosciuto quando è vicino e orientato correttamente
14 MODELLO D AZIONE Modello chiave-serratura: il substrato si lega al sito attivo come la chiave in una serratura. Modello dell adattamento indotto: la struttura dell enzima si adatta a quella del substrato.
15 I gruppi funzionali catalitici di un enzima interagiscono temporaneamente con un substrato mettendolo nella orientazione favorevole alla reazione: si forma il complesso ES. L interazione tra enzima e substrato è mediata da legami deboli non covalenti. La formazione di tali legami è accompagnata da rilascio di energia che costituisce la principale fonte di energia libera usata dall enzima per abbassare l energia di attivazione della reazione.
16 Funzioni dei cofattori Presenti in 2/3 degli enzimi coniugati 1) si legano al substrato in modo da orientarlo correttamentte per la reazione 2) partecipano a reazioni redox mediante il cambiamento reversibile del numero di ossidazione del metallo 3) stabiliizzano ellettrostaticamentte o protteggono le cariche negative
17 Coenzimi Sono molecole organiche, spesso derivate da vitamine Per diventare coenzima, la vitamina subisce delle trasformazioni che vanno dalla semplice fosforilazione (uno dei casi più comuni) a trasformazioni più complesse. FUNZIONI: Agiscono da ossidanti e da riducenti Attivano i gruppi funzionali per ulteriori reazioni Forniscono un buon nucleofilo/base e permettano la delocalizzazione di elettroni I coenzimi possono essere classificati in gruppi diversi, in base al tipo di reazione catalizzata.
18 Coenzimi trasportatori di idrogeno Coenzimi piridinici (NAD + e NADP + ) Derivano dall acido nicotinico o niacina o vit. B 3 o PP) Sono coenzimi di deidrogenasi La forma ossidata viene indicata come NAD(P) + e quella ridotta NAD(P)H o, per meglio evidenziare il meccanismo della reazione, NAD(P)H + H + Il loro legame all apoenzima è labile, infatti dopo aver funzionato in un senso, si staccano e si legano ad un altra proteina funzionando in senso opposto. Si ha così la possibilità della riossidazione del coenzima
19 Nicotinamide Adenina Dinucleotide NAD + Fungono da accettori di idrogeno nell ossidazione di svariati composti (reazioni di ossido-riduzione). La loro riduzione avviene per trasferimento di uno ione idruro (H - ) dal substrato all anello piridinico del coenzima, con liberazione nel mezzo di un H +
20 FMN Coenzimi flavinici (FMN e FAD) Sono le forme coenzimatiche della riboflavina o vit. B 2. FMN e FAD sono strettamente legati ai propri apoenzimi con un legame covalente Sono coenzimi di ossidoriduzione Flavin adenin dinucleotide (FAD) Ribitolo La molecola, è costituita da 3 anelli condensati, che costituiscono la flavina, il quale è legato al ribosio tramite l'atomo di azoto dell'anello centrale.
21 I coenzimi flavinici, a differenza di quelli piridinici, accettano 2H + e 2e - pertanto le loro forma ridotte sono FMNH 2 e FADH 2
22 Coenzima Q (CoQ o UBICHINONE): è un composto di natura lipidica. Trasporta atomi di H e elettroni
23 I trasportatori di elettroni I trasportatori partecipano alle ossidoriduzioni trasferendo 2 elettroni alla volta
24 Coenzima A (CoA) Coenzimi trasportatori di gruppi Deriva dalla vitamina B5 Catalizza tutte le reazioni di trasporto di acili. Tale trasporto si realizza per la formazione di tioesteri
25 I citocromi sono proteine che contengono il gruppo prostetico eme (coenzima) contenente ferro Sono di 3 classi: a, b, c. Trasferiscono elettroni, mediante oscillazioni del Fe dell eme tra la forma ferrica Fe 3+ (ossidata) e quella ferrosa Fe 2+ (ridotta)
26 Il citocromo c 1
27 Reversibilità delle reazioni enzimatiche L enzima favorisce il raggiungimento dell equilibrio, quindi in teoria potrebbe catalizzare anche la reazione inversa A B Ma, se B è substrato di una reazione successiva, la prima reazione diventa praticamente irreversibile A B C Ciò vale per catene anche molto lunghe di reazioni (catene enzimatiche) A B C D E Anche se le singole reazioni enzimatiche sono reversibili (specie quelle con G 0), in pratica il flusso è unidirezionale perché il prodotto di una reazione funge da substrato per la reazione successiva Spesso il prodotto terminale di una sequenza di reazioni (E) inibisce il deflusso della stessa catena a livello della prima reazione A B L accumulo di E chiude il rubinetto La mancanza di E riapre il rubinetto A B C D E
28 Il buon funzionamento della cellula richiede che le varie attività enzimatiche siano regolate 1) Modulazione dell attività dell enzima (regolazione veloce) secondi o minuti Un certo numero di fattori esterni agisce sull attività degli enzimi accelerando la conversione del substrato in prodotto: Concentrazione del substrato Temperatura ph Inibitori Modulatori positivi e negativi 2) Controllo genico della concentrazione di enzima (regolazione lenta) ore o giorni
29 Equazione di Michaelis-Menten (1913) Leonor Michaelis & Maud Menten Leonor Michaelis (Berlin, January 16, 1875 New York, October 8, 1949). Maud Leonora Menten (Ontario, March 20, 1879 July 26, 1960), among the first women in Canada to earn a medical doctorate. At that time women were not allowed to do research in Canada, therefore she decided to do research in other countries such as the United States and Germany.
30 1 solo substrato Assunzioni di Michaelis-Menten K 1 K E + S ES 3 E + P K 2 L enzima si lega col substrato per formare ES: reazione reversibile e relativamente lenta Il complesso ES subisce il cambiamento conformazionale che induce la formazione di P L enzima rilascia P e torna nello stato iniziale La velocità globale è regolata dalla formazione di ES
31 Curva iperbolica CONCENTRAZIONE DEL SUBSTRATO Si osserva che, nel primo tratto della curva (rettilineo) la V è direttamente proporzionale alla concentrazione di substrato aumentando la concentrazione di S aumenta proporzionalmente il numero di molecole che formano il complesso ES Una volta raggiunta una certa concentrazione di S la v 0 cresce più lentamente fino a raggiungere un valore massimo quando tutto l enzima è saturato dal substrato e pur continuando ad aumentare la concentrazione di S la v 0 rimane costante (Vmax).
32 Cinetiche chimiche vs cinetiche enzimatiche Velocità A B V = k [A] Cinetica chimica Cinetica enzimatica [A]
33 In una reazione enzimatica E + S ES E + P v = V max v V max [S] v = K M V max 2 V 0 = V K max m + [ S] [ S] K M [S]
34 Rappresentazione grafica delle reazioni enzimatiche Grafico di Lineweaver-Burk V 0 1/V 0 V max V max /2 1/V max K M [S] -1/K M 1/[S]
35 effetto della temperatura sulle reazioni catalizzate da enzimi un eccessivo aumento della temperatura provoca la denaturazione degli enzimi con una modificazione irreversibile del sito attivo e una drastica riduzione dell attività catalitica Aumento dovuto alla temperatura ( ogni 10 C) Diminuzione dovuta alla denaturazione della proteina CURVA DI ATTIVAZIONE Velocità CURVA DI DENATURAZIONE Temperatura
36 effetto del ph sulle reazioni catalizzate da enzimi il cambiamento del ph altera il grado di ionizzazione dei diversi gruppi ionizzabili presenti in una molecola enzimatica; si può individuare un ph ottimale e un range di valori di ph entro cui l enzima mostra la massima efficienza
37
38 INIBITORE: Sostanza che può bloccare o rallentare l attività enzimatica REVERSIBILE agisce con una modalità che consente all enzima di recuperare la propria funzionalità biologica 1. competitiva 2. Incompetitiva o acompetitiva 3. non competitiva/mista IRREVERSIBILE si lega con un legame covalente ad un residuo di un amminoacido presente nel sito attivo senza la possibilità di staccarsi quindi l attività dell enzima si annulla Non possono essere rimossi con mezzi semplici e sono utilizzati: - nello studio dei siti catalitici - come farmaci - come antiparassitari
39 INIBIZIONE IRREVERSIBILE Gli inibitori irreversibili legandosi covalentemente con un residuo amminoacidico nel sito attivo inattivano l enzima Generalmente possono essere veleni, tossine oppure farmaci Inibitore Formula Origine Meccanismo Diisopropil fluorofosfato (DFP) H 3 C CH 3 F CH 3 O P O O CH 3 Sintetico Inibisce gli enzimi con serina nel sito attivo CH 3 F Sarin H 3 C Sintetico Come il DFP O P O CH 3 Penicillina R O HN O N S CH 3 CH 3 CH 3 Penicillum Notatum Inibisce gli enzimi della sintesi della parete batterica
40 INIBIZIONE REVERSIBILE Formano con l enzima complessi reversibili: le interazioni leganti sono legami deboli oppure legami forti, ma facilmente reversibili: Legami idrogeno Interazioni dipolo-dipolo Interazioni idrofobiche Legami covalenti facilmente reversibili Legami ionici che possono essere facilmente reversibili per solvatazione degli ioni in acqua
41 Competitiva Non competitiva/mista Incompetitiva o acompetitiva Un inibitore non competitivo è una sostanza che si lega sia all enzima libero sia al complesso ES: la presenza dell inibitore riduce la velocità di formazione del prodotto modificando il sito attivo L entrata del substrato modifica il sito attivo, formando un nuovo sito per l inibitore che può entrare: agisce legandosi e formando il complesso ESI inattivo
42 Esempi di inibizione enzimatica competitiva Alcool deidrogenasi Aldeide deidrogenasi CH 3 -CH 2 OH CH 3 -CHO CH 3 -COO Etanolo Acetaldeide Acetato Coma etilico
43 ENZIMI ALLOSTERICI Un enzima allosterico è una proteina oligomerica (struttura quaternaria) oltre al sito attivo esistono anche siti diversi (allosterici) tali enzimi non seguono la cinetica di Michaelis Menten può esistere in una conformazione ad alta affinità per il substrato R ed in una conformazione a più bassa affinità per il substrato T Effettori sono molecole che interagiscono con i siti allosterici regolando l attività dell enzima modificandone la conformazione 1) Cooperatività: cambiamenti conformazionali di una subunità in risposta al cambiamento conformazionale della subunità adiacente 2) Allosterismo: cambiamenti conformazionali di una subunità in risposta ad un effettore allosterico positivo e negativo
44 MODELLO CONCERTATO MONOD Cooperatività: le subunità enzimatiche esistono in due stati conformazionali definiti T ed R (Teso e Rilassato), in equilibrio tra di loro. Il legame di un substrato modifica l'equilibrio spostandolo verso la forma R più affine.
45 ALLOSTERISMO S intende un cambiamento conformazionale dell enzima e quindi del sito attivo, a seguito dell interazione di un effettore positivo o negativo in un sito allosterico (regolatore)
46
47 Cinetica degli enzimi allosterici e cooperativi Sigmoide, non iperbolico NON-Michaelis-Menten Sempre più efficaci all aumentare del numero di subunità v 0 4 subunità 1 subunità 2 subunità Bassa [SUB] la V cresce lentamente Intermedia [SUB] la V cresce rapidamente Alta [SUB] la V = Vmax [S]
48 INIBIZIONE RETROATTIVA (FEEDBACK) A volte la regolazione allosterica può fungere da controllo retroattivo quando il modulatore allosterico negativo (inibitore) è rappresentato dal prodotto della reazione enzimatica
49
BIOLOGIA GENERALE 22-24 ottobre 2007
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
- CINETICA ENZIMATICA
 - CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
- CINETICA ENZIMATICA ENZIMI: - CATALIZZATORI aumenta la V di una reazione chimica senza subire trasformazioni durante l intero processo - PROTEINE gli enzimi sono proteine di struttura 3 o talora 4 -
Cofattori e vitamine
 Enzimi: concetti di base e meccanismi di catalisi enzimatica a. Classificazione, meccanismo d azione b. Esempi di reazioni catalizzate c. Descrizione di alcune tipiche proteine enzimatiche. Cofattori e
Enzimi: concetti di base e meccanismi di catalisi enzimatica a. Classificazione, meccanismo d azione b. Esempi di reazioni catalizzate c. Descrizione di alcune tipiche proteine enzimatiche. Cofattori e
ENZIMI Alcuni sono costituiti solo da a.a. Altri richiedono per la loro attività catalitica la presenza di COFATTORI
 ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
Metabolismo: Introduzione
 Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
Gli enzimi. L azione degli enzimi è caratterizzata da alcune proprietà fondamentali:
 Gli enzimi Nel metabolismo energetico le cellule producono notevoli quantità di CO 2 che deve essere eliminata con l apparato respiratorio. Il trasferimento della CO 2 dalle cellule al sangue e da esso
Gli enzimi Nel metabolismo energetico le cellule producono notevoli quantità di CO 2 che deve essere eliminata con l apparato respiratorio. Il trasferimento della CO 2 dalle cellule al sangue e da esso
Enzimi. Nomenclatura:
 Enzimi Nelle cellule, ad una temperatura di soli 37 C, avvengono reazioni (di ossidazione, di idrolisi, di sintesi, etc,) a velocità straordinarie, che richiederebbero temperature e pressioni elevate.
Enzimi Nelle cellule, ad una temperatura di soli 37 C, avvengono reazioni (di ossidazione, di idrolisi, di sintesi, etc,) a velocità straordinarie, che richiederebbero temperature e pressioni elevate.
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 17
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 17 Enzimi Concetti chiave: Gli enzimi si differenziano dai catalizzatori chimici di uso comune per velocità, condizioni, specificità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 17 Enzimi Concetti chiave: Gli enzimi si differenziano dai catalizzatori chimici di uso comune per velocità, condizioni, specificità
L adattamento dei batteri. Strategie di adattamento
 L adattamento dei batteri Strategie di adattamento mutazione trasferimento genico orizzontale regolazione dell espressione genica regolazione della trascrizione regolazione della traduzione regolazione
L adattamento dei batteri Strategie di adattamento mutazione trasferimento genico orizzontale regolazione dell espressione genica regolazione della trascrizione regolazione della traduzione regolazione
ENZIMI CINETICA ENZIMATICA
 ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
ENZIMI PERCHE UNA REAZIONE AVVENGA, SI DEVONO SODDISFARE TRE CONDIZIONI I SUBSTRATI DEVONO ENTRARE IN COLLISIONE LA COLLISIONE DEVE AVVENIRE CON ORIENTAMENTO CORRETTO I REAGENTI DEVONO AVERE ENERGIA SUFFICIENTE
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Gli enzimi sono catalizzatori nelle reazioni dei sistemi biologici Essi non sono gli unici catalizzatori biologici, esistono infatti:
 Cinetica enzimatica Gli enzimi sono catalizzatori nelle reazioni dei sistemi biologici Essi non sono gli unici catalizzatori biologici, esistono infatti: ribozimi e abzimi Quasi tutti gli enzimi sono proteine
Cinetica enzimatica Gli enzimi sono catalizzatori nelle reazioni dei sistemi biologici Essi non sono gli unici catalizzatori biologici, esistono infatti: ribozimi e abzimi Quasi tutti gli enzimi sono proteine
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA
 PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Biosintesi non ribosomiale di metaboliti peptidici bioattivi
 Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
Farmaci del sistema nervoso autonomo
 Farmaci del sistema nervoso autonomo Farmaci colinergici Esercitano i loro effetti farmacologici sul sistema nervoso parasimpatico che utilizza Acetilcolina come mediatore chimico L acetilcolina (Ach)
Farmaci del sistema nervoso autonomo Farmaci colinergici Esercitano i loro effetti farmacologici sul sistema nervoso parasimpatico che utilizza Acetilcolina come mediatore chimico L acetilcolina (Ach)
Mediatore chimico. Recettore. Trasduzione del segnale. Risposta della cellula
 Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Attivitá e cinetica enzimatica
 Attivitá e cinetica enzimatica PAS : Classe di insegnamento A60 Biologia e scienze A.A. 2013/2014 09/05/2014 Cinetica Enzimatica La cinetica enzimatica è misurata come velocità di conversione del substrato
Attivitá e cinetica enzimatica PAS : Classe di insegnamento A60 Biologia e scienze A.A. 2013/2014 09/05/2014 Cinetica Enzimatica La cinetica enzimatica è misurata come velocità di conversione del substrato
Respirazione cellulare
 Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2! 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
Respirazione cellulare L equazione generale della respirazione C 6 H 12 O 6 + 6 O 2! 6 CO 2 + 6 H 2 O + 36 ATP 1 molec zucchero 6 molec ossigeno 6 molec anidride carbonica 6 molec acqua + = + + 36 molecole
IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA.
 CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA FACOLTA DI MEDICINA E CHIRURGIA. IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA. Un enzima è una proteina capace di catalizzare una specifica reazione
CORSO DI CHIMICA E PROPEDEUTICA BIOCHIMICA FACOLTA DI MEDICINA E CHIRURGIA. IL MODELLO DI MICHAELIS E MENTEN PER LA CINETICA ENZIMATICA. Un enzima è una proteina capace di catalizzare una specifica reazione
Continua. Peptidasi H 2 O
 Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Elettroforesi. Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita.
 Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
FARMACODINAMICA RECETTORI ED EFFETTORI
 FARMACODINAMICA I recettori per i farmaci Prof. Renato Bernardini RECETTORI ED EFFETTORI Farmaco (Φαρµακον) = principio attivo Recettore = macromolecole deputate alla trasmissione di un segnale chimico
FARMACODINAMICA I recettori per i farmaci Prof. Renato Bernardini RECETTORI ED EFFETTORI Farmaco (Φαρµακον) = principio attivo Recettore = macromolecole deputate alla trasmissione di un segnale chimico
in Terminazione Neurone Dendriti Soma Fessura sinaptica sinaptica Nucleo dendrite Segmento iniziale Sinapsi inibitoria Segmento mielinico Assone
 Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
glicogeno Glucosio 6-P Piruvato Acetil CoA Intermedi del ciclo di Krebs
 PIRUVAT glicogeno Glicogeno sintesi glicogenolisi Glucosio Glucosio 6-P Ribosio 5-P glicolisi Gluconeogenesi Amino acidi Piruvato Acetil CoA lattato Intermedi del ciclo di Krebs Concentrazione di glicogeno
PIRUVAT glicogeno Glicogeno sintesi glicogenolisi Glucosio Glucosio 6-P Ribosio 5-P glicolisi Gluconeogenesi Amino acidi Piruvato Acetil CoA lattato Intermedi del ciclo di Krebs Concentrazione di glicogeno
MODULO 2 ENZIMI CARATTERISTICHE GENERALI
 MODULO 2 ENZIMI CARATTERISTICHE GENERALI Introduzione L elevatissimo numero di reazioni chimiche, che in ogni istante avvengono all interno e all esterno delle cellule che costituiscono i nostri tessuti
MODULO 2 ENZIMI CARATTERISTICHE GENERALI Introduzione L elevatissimo numero di reazioni chimiche, che in ogni istante avvengono all interno e all esterno delle cellule che costituiscono i nostri tessuti
Macromolecole Biologiche. I domini (III)
 I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
Cinetica enzimatica Inibitori enzimatici
 Cinetica enzimatica Inibitori enzimatici CINETICA ENZIMATICA Determinazione della velocità della reazione e di come questa cambia in risposta a modificazioni dei parametri sperimentali E il metodo più
Cinetica enzimatica Inibitori enzimatici CINETICA ENZIMATICA Determinazione della velocità della reazione e di come questa cambia in risposta a modificazioni dei parametri sperimentali E il metodo più
4) PROTEINE FERRO ZOLFO. Contengono Fe e S in quantità equimolecolari; fanno parte dei complessi respiratori. La NADH DH contiene diversi centri Fe-S.
 4) PROTEINE FERRO ZOLFO Contengono Fe e S in quantità equimolecolari; fanno parte dei complessi respiratori. La NADH DH contiene diversi centri Fe-S. Trasportano elettroni attraverso le transizioni Fe
4) PROTEINE FERRO ZOLFO Contengono Fe e S in quantità equimolecolari; fanno parte dei complessi respiratori. La NADH DH contiene diversi centri Fe-S. Trasportano elettroni attraverso le transizioni Fe
ossigeno e ne facilita la diffusione dai capillari all ambiente intracellulare.
 Ricostituzione e attività pseudoenzimatica della mioglobina modificata Giulia Bertelegni e Carolina Ferrari I.I.S. A.Maserati Facoltà di Scienze MM.FF.NN. Dipartimento di Chimica generale Università degli
Ricostituzione e attività pseudoenzimatica della mioglobina modificata Giulia Bertelegni e Carolina Ferrari I.I.S. A.Maserati Facoltà di Scienze MM.FF.NN. Dipartimento di Chimica generale Università degli
Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che
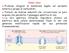 Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro.
![Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro. Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro.](/thumbs/27/12374782.jpg) Prodotto ionico dell acqua e ph Prodotto ionico dell acqua L acqua è un elettrolita debolissimo e si dissocia secondo la reazione: H 2 O H + + OH - La costante di equilibrio dell acqua è molto piccola
Prodotto ionico dell acqua e ph Prodotto ionico dell acqua L acqua è un elettrolita debolissimo e si dissocia secondo la reazione: H 2 O H + + OH - La costante di equilibrio dell acqua è molto piccola
Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica.
 Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Gli enzimi. Proprietà generali Classificazione e nomenclatura Catalisi enzimatica
 Gli enzimi Proprietà generali Classificazione e nomenclatura Catalisi enzimatica En-zima εν ζυμη nel lievito Enzima termine generico per definire un catalizzatore biologico Tranne che diversamente indicato,
Gli enzimi Proprietà generali Classificazione e nomenclatura Catalisi enzimatica En-zima εν ζυμη nel lievito Enzima termine generico per definire un catalizzatore biologico Tranne che diversamente indicato,
Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso a secco.
 Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso a secco. Svolgono funzioni biologiche di fondamentale importanza e possono
Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso a secco. Svolgono funzioni biologiche di fondamentale importanza e possono
Niccolò Taddei Biochimica
 Niccolò Taddei Biochimica VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono
Niccolò Taddei Biochimica VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono
DNA - RNA. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi.
 DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
Valitutti, Taddei, Kreuzer, Massey, Sadava, Hills, Heller, Berenbaum
 Dal carbonio agli OGM VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono evidenziate
Dal carbonio agli OGM VERSO L UNIVERSITÀ Le domande sono tratte dalle prove di ammissione emesse annualmente dal Ministero dell Istruzione, dell Università e della Ricerca (MIUR) e le soluzioni sono evidenziate
Il ciclo dell acido citrico
 Il ciclo dell acido citrico Il catabolismo di proteine, grassi e carboidrati avviene nelle tre fasi della respirazione cellulare Il piruvato viene ossidato ad acetil-coa e CO 2 La decarbossilazione
Il ciclo dell acido citrico Il catabolismo di proteine, grassi e carboidrati avviene nelle tre fasi della respirazione cellulare Il piruvato viene ossidato ad acetil-coa e CO 2 La decarbossilazione
REAZIONI CHIMICHE. Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: I reagenti (substrati) devono entrare in collisione
 ENZIMI 1 REAZIONI CHIMICHE Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: 2 I reagenti (substrati) devono entrare in collisione Le collisione tra le molecole dei reagenti
ENZIMI 1 REAZIONI CHIMICHE Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: 2 I reagenti (substrati) devono entrare in collisione Le collisione tra le molecole dei reagenti
Regolazione del metabolismo del glucosio
 Regolazione del metabolismo del glucosio Regolazione coordinata di glicolisi e gluconeogenesi Glicolisi e gluconeogenesi sono regolate in modo reciproco La regolazione è a livello dei punti di deviazione
Regolazione del metabolismo del glucosio Regolazione coordinata di glicolisi e gluconeogenesi Glicolisi e gluconeogenesi sono regolate in modo reciproco La regolazione è a livello dei punti di deviazione
-uno o più IONI INORGANICI
 Coenzimi e vitamine Alcuni enzimi, per svolgere la loro funzione, hanno bisogno di componenti chimici addizionali, i COFATTORI APOENZIMA + COFATTORE = OLOENZIMA = enzima cataliticamente attivo Il cofattore
Coenzimi e vitamine Alcuni enzimi, per svolgere la loro funzione, hanno bisogno di componenti chimici addizionali, i COFATTORI APOENZIMA + COFATTORE = OLOENZIMA = enzima cataliticamente attivo Il cofattore
SISTEMI ENERGETICI. L ATP privato di uno dei suoi 3 radicali fosforici diventa ADP (adenosindifosfato).
 SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
PROTEINE. Amminoacidi
 PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
SINTESI DELL RNA. Replicazione. Trascrizione. Traduzione
 SINTESI DELL RNA Replicazione Trascrizione Traduzione L RNA ha origine da informazioni contenute nel DNA La TRASCRIZIONE permette la conversione di una porzione di DNA in una molecola di RNA con una sequenza
SINTESI DELL RNA Replicazione Trascrizione Traduzione L RNA ha origine da informazioni contenute nel DNA La TRASCRIZIONE permette la conversione di una porzione di DNA in una molecola di RNA con una sequenza
unità C2. Le trasformazioni energetiche nelle cellule
 unità 2. Le trasformazioni energetiche nelle cellule Il trasporto nelle cellule avviene senza consumo di energia con consumo di energia trasporto passivo trasporto attivo attraverso il doppio strato fosfolipidico
unità 2. Le trasformazioni energetiche nelle cellule Il trasporto nelle cellule avviene senza consumo di energia con consumo di energia trasporto passivo trasporto attivo attraverso il doppio strato fosfolipidico
Regolazione della trascrizione. Operoni catabolici nei procarioti (controllo negativo)
 Regolazione della trascrizione Operoni catabolici nei procarioti (controllo negativo) I geni possono essere accesi e spenti In un organismo pluricellulare adulto, vi sono molti tipi di cellule differenti,
Regolazione della trascrizione Operoni catabolici nei procarioti (controllo negativo) I geni possono essere accesi e spenti In un organismo pluricellulare adulto, vi sono molti tipi di cellule differenti,
PROTEINE. sono COMPOSTI ORGANICI QUATERNARI
 PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas
 1 Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas Capitolo 7 Enzimi, le macchine della vita Piccole macchine regolano la funzione del corpo umano in un orchestrazione perfetta e a velocità
1 Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas Capitolo 7 Enzimi, le macchine della vita Piccole macchine regolano la funzione del corpo umano in un orchestrazione perfetta e a velocità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA
 LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
Il metabolismo dell RNA. Prof. Savino; dispense di Biologia Molecolare, Corso di Laurea in Biotecnologie
 Il metabolismo dell RNA I vari tipi di RNA Il filamento di DNA che dirige la sintesi dello mrna è chiamato filamento stampo o filamento antisenso. L altro filamento che ha sequenza identica a quella dello
Il metabolismo dell RNA I vari tipi di RNA Il filamento di DNA che dirige la sintesi dello mrna è chiamato filamento stampo o filamento antisenso. L altro filamento che ha sequenza identica a quella dello
Acidi e basi. HCl H + + Cl - (acido cloridrico) NaOH Na + + OH - (idrossido di sodio; soda caustica)
 Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
Acidi e basi Per capire che cosa sono un acido e una base dal punto di vista chimico, bisogna riferirsi ad alcune proprietà chimiche dell'acqua. L'acqua, sia solida (ghiaccio), liquida o gassosa (vapore
BIOLOGIA GENERALE. Alessandro Massolo Dip. Biologia Animale e Genetica c/o Prof. F. Dessì-Fulgheri (Via Romana 17) massolo@unifi.
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
Figura 1. Rappresentazione della doppia elica di DNA e struttura delle differenti basi.
 Sommario La molecola di DNA è deputata a conservare le informazioni genetiche necessarie per lo sviluppo ed il funzionamento degli organismi viventi. Poiché contiene le istruzioni per la costruzione delle
Sommario La molecola di DNA è deputata a conservare le informazioni genetiche necessarie per lo sviluppo ed il funzionamento degli organismi viventi. Poiché contiene le istruzioni per la costruzione delle
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione
 REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
REAZIONI CHIMICHE. Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: I reagenti (substrati) devono entrare in collisione
 ENZIMI 1 REAZIONI CHIMICHE Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: 2 I reagenti (substrati) devono entrare in collisione Le collisione tra le molecole dei reagenti
ENZIMI 1 REAZIONI CHIMICHE Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: 2 I reagenti (substrati) devono entrare in collisione Le collisione tra le molecole dei reagenti
Tipi di reazioni. Reazioni chimiche. Di dissociazione. Di sintesi. Di semplice scambio. Di doppio scambio. Reazioni complesse
 Tipi di reazioni Le reazioni chimiche vengono tradizionalmente classificate a seconda del tipo di trasformazione subita dai reagenti: Reazioni chimiche possono essere Di dissociazione Una sostanza subisce
Tipi di reazioni Le reazioni chimiche vengono tradizionalmente classificate a seconda del tipo di trasformazione subita dai reagenti: Reazioni chimiche possono essere Di dissociazione Una sostanza subisce
www.fisiokinesiterapia.biz TRASCRIZIONE
 www.fisiokinesiterapia.biz TRASCRIZIONE TRASCRIZIONE Processo mediante il quale una sequenza di DNA (un gene) viene copiata in una sequenza di RNA Dalla trascrizione derivano gli mrna, che verranno tradotti
www.fisiokinesiterapia.biz TRASCRIZIONE TRASCRIZIONE Processo mediante il quale una sequenza di DNA (un gene) viene copiata in una sequenza di RNA Dalla trascrizione derivano gli mrna, che verranno tradotti
EMOGLOBINA ... www.pianetachimica.it
 EMGLBIA www.pianetachimica.it L'emoglobina è una proteina specializzata nel trasporto di ossigeno, si trova all interno dei globuli rossi del sangue ai quali conferisce il caratteristico colore rosso intenso.
EMGLBIA www.pianetachimica.it L'emoglobina è una proteina specializzata nel trasporto di ossigeno, si trova all interno dei globuli rossi del sangue ai quali conferisce il caratteristico colore rosso intenso.
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici
 I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
La catalasi: un enzima in azione
 Percorso di Didattica laboratoriale La catalasi: un enzima in azione Scuola Secondaria di Secondo Grado IISS - IPSIA E. Majorana Bari Classe IV B Docente: Miralma Serio Organizzatore cognitivo: Le trasformazioni
Percorso di Didattica laboratoriale La catalasi: un enzima in azione Scuola Secondaria di Secondo Grado IISS - IPSIA E. Majorana Bari Classe IV B Docente: Miralma Serio Organizzatore cognitivo: Le trasformazioni
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I
 Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I I TRASPORTI ATTRAVERSO MEMBRANE BIOLOGICHE Movimenti di piccoli soluti attraverso le membrane 2 categorie generali Trasporto
Corso di Laurea Magistrale in Medicina e Chirurgia Biofisica e Fisiologia I I TRASPORTI ATTRAVERSO MEMBRANE BIOLOGICHE Movimenti di piccoli soluti attraverso le membrane 2 categorie generali Trasporto
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 24
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 24 Una panoramica del metabolismo Concetti chiave: Organismi diversi utilizzano strategie differenti per catturare l'energia
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 24 Una panoramica del metabolismo Concetti chiave: Organismi diversi utilizzano strategie differenti per catturare l'energia
Metabolismo degli aminoacidi
 Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
SINTESI PROTEICA. Replicazione. Trascrizione. Traduzione
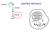 Replicazione SINTESI PROTEICA Trascrizione Traduzione 61 codoni codificanti 3 triplette non senso (STOP) AUG codone di inizio codone per Met Caratteristiche del codice genetico Specificità Il codice genetico
Replicazione SINTESI PROTEICA Trascrizione Traduzione 61 codoni codificanti 3 triplette non senso (STOP) AUG codone di inizio codone per Met Caratteristiche del codice genetico Specificità Il codice genetico
Importanza degli enzimi in Medicina
 ENZIMI Importanza degli enzimi in Medicina 1. Chiave per capire errori del metabolismo 2. Importanti nelle reazioni di detossificazione 3. Targets di chemioterapia 4. Essenziali per formulare il razionale
ENZIMI Importanza degli enzimi in Medicina 1. Chiave per capire errori del metabolismo 2. Importanti nelle reazioni di detossificazione 3. Targets di chemioterapia 4. Essenziali per formulare il razionale
Dissociazione elettrolitica
 Dissociazione elettrolitica Le sostanze ioniche si solubilizzano liberando ioni in soluzione. La dissociazione elettrolitica è il processo con cui un solvente separa ioni di carica opposta e si lega ad
Dissociazione elettrolitica Le sostanze ioniche si solubilizzano liberando ioni in soluzione. La dissociazione elettrolitica è il processo con cui un solvente separa ioni di carica opposta e si lega ad
... corso di chimica elettrochimica 1
 ... corso di chimica elettrochimica 1 CONTENUTI reazioni elettrochimiche pile e celle elettrolitiche potenziale d elettrodo e forza elettromotrice equazione di Nernst elettrolisi leggi di Faraday batterie
... corso di chimica elettrochimica 1 CONTENUTI reazioni elettrochimiche pile e celle elettrolitiche potenziale d elettrodo e forza elettromotrice equazione di Nernst elettrolisi leggi di Faraday batterie
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca
 INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ]
![Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ] Cosa misura il ph: la concentrazione di ioni H +, che si scrive [H + ]. La definizione di ph è: ph = -log 10 [H + ]](/thumbs/34/16945364.jpg) La molecola d acqua è un dipolo perché l atomo di ossigeno è molto elettronegativo ed attira più vicini a sé gli elettroni di legame. Questo, unito alla forma della molecola, produce un accumulo di carica
La molecola d acqua è un dipolo perché l atomo di ossigeno è molto elettronegativo ed attira più vicini a sé gli elettroni di legame. Questo, unito alla forma della molecola, produce un accumulo di carica
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B
 Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
Fosforilazione ossidativa
 Fosforilazione ossidativa La fosforilazione ossidativa rappresenta il culmine del metabolismo energetico negli organismi aerobi E costituita da due fenomeni strettamente accoppiati: 1. I coenzimi ridotti
Fosforilazione ossidativa La fosforilazione ossidativa rappresenta il culmine del metabolismo energetico negli organismi aerobi E costituita da due fenomeni strettamente accoppiati: 1. I coenzimi ridotti
Metalli in medicina. L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il
 Metalli in medicina L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il rame, per esempio, erano utilizzati nella Grecia antica. Già da secoli il Hg 2+ era utilizzato nel trattamento
Metalli in medicina L utilizzo dei metalli in medicina ha radici ben antiche. Il ferro ed il rame, per esempio, erano utilizzati nella Grecia antica. Già da secoli il Hg 2+ era utilizzato nel trattamento
Catena di Trasporto degli elettroni
 Chimica Biologica A.A. 2010-2011 Catena di Trasporto degli elettroni Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Respirazione - il catabolismo di tutti i combustibili
Chimica Biologica A.A. 2010-2011 Catena di Trasporto degli elettroni Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Respirazione - il catabolismo di tutti i combustibili
Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone = C 6 O 6 (H 2 O) 6
 Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
Modello del collasso idrofobico. Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60
 Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
È importante quindi conoscere le proprietà chimiche dell acqua. Le reazioni acido base sono particolari esempi di equilibrio chimico in fase acquosa
 Premessa Le nozioni di acido e di base non sono concetti assoluti ma sono relativi al mezzo in cui tale sostanze sono sciolte. L acqua è il solvente per eccellenza, scelto per studiare le caratteristiche
Premessa Le nozioni di acido e di base non sono concetti assoluti ma sono relativi al mezzo in cui tale sostanze sono sciolte. L acqua è il solvente per eccellenza, scelto per studiare le caratteristiche
Βeta ossidazione degli acidi grassi BETA OSSIDAZIONE DEGLI ACIDI GRASSI 13/12/2013 SEMINARIO. Acidi grassi (2)
 Acidi grassi (1) Mitocondri SEMINARIO BETA OSSIDAZIONE DEGLI ACIDI GRASSI Sono le principali fonti di energia per alcuni tessuti (es. muscolo cardiaco). Si genera molto più energia dall ossidazione degli
Acidi grassi (1) Mitocondri SEMINARIO BETA OSSIDAZIONE DEGLI ACIDI GRASSI Sono le principali fonti di energia per alcuni tessuti (es. muscolo cardiaco). Si genera molto più energia dall ossidazione degli
la struttura tridimensionale può essere ottenuta solo per Un intero dominio in genere da 50 a 300 residui
 Durante la traduzione l informazione di ripiegamento codificata nella sequenza aminoacidica diventa disponibile in maniera vettoriale la struttura tridimensionale può essere ottenuta solo per Un intero
Durante la traduzione l informazione di ripiegamento codificata nella sequenza aminoacidica diventa disponibile in maniera vettoriale la struttura tridimensionale può essere ottenuta solo per Un intero
DIPARTIMENTO DI SCIENZE INTEGRATE CHIMICA FISICA SCIENZE DELLA TERRA - BIOLOGIA
 IISS A. De Pace Lecce A.S. 2012-2013 DIPARTIMENTO DI SCIENZE INTEGRATE FISICA SCIENZE DELLA TERRA - BIOLOGIA PIANI DI STUDIO DELLE DISCIPLINE SECONDO ANNO Piano di studi della disciplina DESCRIZIONE Lo
IISS A. De Pace Lecce A.S. 2012-2013 DIPARTIMENTO DI SCIENZE INTEGRATE FISICA SCIENZE DELLA TERRA - BIOLOGIA PIANI DI STUDIO DELLE DISCIPLINE SECONDO ANNO Piano di studi della disciplina DESCRIZIONE Lo
Le Ig sono glicoproteine costituite da 4 catene polipeptidiche:
 Struttura delle Ig Le Ig sono glicoproteine costituite da 4 catene polipeptidiche: 2 catene pesanti H (heavy( heavy) di P.M. 50.000 D, formate da c/a 450 amminoacidi 2 catene leggere L (light) Di P.M.
Struttura delle Ig Le Ig sono glicoproteine costituite da 4 catene polipeptidiche: 2 catene pesanti H (heavy( heavy) di P.M. 50.000 D, formate da c/a 450 amminoacidi 2 catene leggere L (light) Di P.M.
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 2
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 2 Versatilità del carbonio nel formare legami covalenti La chimica degli organismi viventi è organizzata intorno al
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 2 Versatilità del carbonio nel formare legami covalenti La chimica degli organismi viventi è organizzata intorno al
CELLULE EUCARIOTICHE
 CELLULE EUCARIOTICHE Le cellule eucariotiche sono di maggiori dimensioni, rispetto a quelle procariotiche (almeno 10 volte più grandi) Oltre a: membrana plasmatica, citoplasma, DNA e ribosomi (comuni a
CELLULE EUCARIOTICHE Le cellule eucariotiche sono di maggiori dimensioni, rispetto a quelle procariotiche (almeno 10 volte più grandi) Oltre a: membrana plasmatica, citoplasma, DNA e ribosomi (comuni a
materia atomi miscugli omogenei e eterogenei sostanze elementari composti
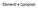 Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
"#$%&'(%!*+,-(+$%)!(%"%'4$.)."#0'0"'"*#,$*'<2.--,-%)*='4$%#.0".='5%33*'"*#,$*-.>'
 "#$%& "#$%&(#)(%)#*"+*"*#,$*-../*$#01020*-.2%34%)#*/*3*2$%3%-.2%-.-,"56010-*3."#0*55$%705-0*#0 "#$%&(%)5.".$02*3."#.)%"%2%34%)#0%$5*"0203*2$%3%-.2%-*$0& 8.)0".)0"#.#026. 9-*)#%3.$0 :-*))0102*+0%"./.0;%-03.$0&
"#$%& "#$%&(#)(%)#*"+*"*#,$*-../*$#01020*-.2%34%)#*/*3*2$%3%-.2%-.-,"56010-*3."#0*55$%705-0*#0 "#$%&(%)5.".$02*3."#.)%"%2%34%)#0%$5*"0203*2$%3%-.2%-*$0& 8.)0".)0"#.#026. 9-*)#%3.$0 :-*))0102*+0%"./.0;%-03.$0&
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Tecnologia e Tradizione nella produzione del vino
 Scuola secondaria di 1 grado A. Moro Mesagne Tecnologia e Tradizione nella produzione del vino BRINDISI DOC Vino rosso a denominazione di origine controllata prodotto nella zona di Mesagne e Brindisi A
Scuola secondaria di 1 grado A. Moro Mesagne Tecnologia e Tradizione nella produzione del vino BRINDISI DOC Vino rosso a denominazione di origine controllata prodotto nella zona di Mesagne e Brindisi A
IDROCARBURI AROMATICI
 IDROCARBURI AROMATICI Idrocarburi ciclici contenenti un sistema di elettroni delocalizzati su tutto il perimetro dell anello BENZENE C 6 H 6 sp 2 angoli 120 coplanarità struttura simmetrica ad esagono
IDROCARBURI AROMATICI Idrocarburi ciclici contenenti un sistema di elettroni delocalizzati su tutto il perimetro dell anello BENZENE C 6 H 6 sp 2 angoli 120 coplanarità struttura simmetrica ad esagono
Ruolo metabolico delle flavine
 Ruolo metabolico delle flavine Deidrogenasi flaviniche che trasferiscono 2 elettroni Acil CoA deidrogenasi (beta ossidazione acidi grassi) Diidrolipoildeidrogenasi (complessi piruvato dh etc.) Glutatione
Ruolo metabolico delle flavine Deidrogenasi flaviniche che trasferiscono 2 elettroni Acil CoA deidrogenasi (beta ossidazione acidi grassi) Diidrolipoildeidrogenasi (complessi piruvato dh etc.) Glutatione
Farmacodinamica II. Mariapia Vairetti. Dipartimento di Medicina Interna e Terapia Sezione di Farmacologia e Tossicologia Cellulare e Molecolare
 Farmacodinamica II Mariapia Vairetti Dipartimento di Medicina Interna e Terapia Sezione di Farmacologia e Tossicologia Cellulare e Molecolare Processo di riconoscimento fra farmaco e recettore TIPI DI
Farmacodinamica II Mariapia Vairetti Dipartimento di Medicina Interna e Terapia Sezione di Farmacologia e Tossicologia Cellulare e Molecolare Processo di riconoscimento fra farmaco e recettore TIPI DI
Trasformazioni materia
 REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
FUNZIONI LINEARI. FUNZIONE VALORE ASSOLUTO. Si chiama funzione lineare (o funzione affine) una funzione del tipo = +
 FUNZIONI LINEARI. FUNZIONE VALORE ASSOLUTO Si chiama funzione lineare (o funzione affine) una funzione del tipo = + dove m e q sono numeri reali fissati. Il grafico di tale funzione è una retta, di cui
FUNZIONI LINEARI. FUNZIONE VALORE ASSOLUTO Si chiama funzione lineare (o funzione affine) una funzione del tipo = + dove m e q sono numeri reali fissati. Il grafico di tale funzione è una retta, di cui
METABOLISMO DEL Glucosio
 METABLISM DEL Glucosio Il metabolismo del glucosio può essere suddiviso nelle seguenti vie metaboliche: Glicolisi ssidazione del glucosio in acido piruvico e acido lattico. Via del pentoso fosfato Via
METABLISM DEL Glucosio Il metabolismo del glucosio può essere suddiviso nelle seguenti vie metaboliche: Glicolisi ssidazione del glucosio in acido piruvico e acido lattico. Via del pentoso fosfato Via
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it
 LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
LA CORRENTE ELETTRICA Prof. Erasmo Modica erasmo@galois.it L INTENSITÀ DELLA CORRENTE ELETTRICA Consideriamo una lampadina inserita in un circuito elettrico costituito da fili metallici ed un interruttore.
CATENA RESPIRATORIA (CR) FOSFORILAZIONE OSSIDATIVA (FO) scaricato da www.sunhope.it
 CATENA RESPIRATORIA (CR) FOSFORILAZIONE OSSIDATIVA (FO) - Decarb. ossid. piruvato - β-ossidazione acidi grassi - Vie ossidative aa - Ciclo di Krebs avvengono tutte nella matrice mitocondriale In tutte
CATENA RESPIRATORIA (CR) FOSFORILAZIONE OSSIDATIVA (FO) - Decarb. ossid. piruvato - β-ossidazione acidi grassi - Vie ossidative aa - Ciclo di Krebs avvengono tutte nella matrice mitocondriale In tutte
NUCLEOTIDI e ACIDI NUCLEICI
 NUCLEOTIDI e ACIDI NUCLEICI Struttura dei nucleotidi Il gruppo fosfato conferisce carica negativa e proprietà acide FUNZIONI DEI NUCLEOTIDI MOLECOLE DI RISERVA DI ENERGIA L idrolisi dei nucleosidi trifosfato
NUCLEOTIDI e ACIDI NUCLEICI Struttura dei nucleotidi Il gruppo fosfato conferisce carica negativa e proprietà acide FUNZIONI DEI NUCLEOTIDI MOLECOLE DI RISERVA DI ENERGIA L idrolisi dei nucleosidi trifosfato
Equilibri di precipitazione
 Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
Equilibri di precipitazione Molte sostanze solide sono caratterizzate da una scarsa solubilità in acqua (ad es. tutti i carbonati e gli idrossidi degli elementi del II gruppo) AgCl (a differenza di NaCl)
